Определение краевых углов смачивания.
Известно, что в большинстве случаев жидкость, нанесенная на твердое тело не растекается, а остается в виде капли, контактирующей с твердой средой под определенным углом. Растекание жидкости по поверхности твердого тела называется ПОЛНЫМ СМАЧИВАНИЕМ и происходит в том случае, когда молекулы жидкости сильнее взаимодействуют с поверхностью твердого тела, чем между собой(например, вода, на поверхности чистого стекла).
Если молекулы жидкости взаимодействуют друг с другом значительно сильнее, чем с молекулами твердого тела, растекание не произойдет. Жидкость соберется на поверхности твердого тела в каплю, которая, если бы не действовала сила тяжести, имела бы почти сферическую форму. Случай, близкий к этому, наблюдается при нанесении капли ртути на стекло.

Между этими двумя крайними случаями в зависимости от соотношения интенсивности молекулярных сил, действующих, с одной стороны, между молекулами жидкости и, с другой - между молекулами жидкости и твердого тела, возможны различные случаи неполного смачивания, когда капля жидкости образует с поверхностью твердого тела определенный равновесный угол, называемый краевым углом, или углом смачивания. Следует иметь в виду, что краевой угол, образуемый каплей на поверхности твердого тела всегда измеряют со стороны жидкости. На рис.1 изображены капли, образующие на твердой подложке острый краевой угол q <900 (а); q =900 (б) и тупой угол q >900 (в).
Рисунок №1
Полного несмачивания, т.е. случая, когда q =1800, практически некогда не наблюдается,
так как между жидкостью и твердым телом всегда действуют силы прятежения, хотя бы и очень малые.
Смачивание жидкостью твердого тела можно объяснить действием сил поверхностного натяжения. Рассмотрим пример полного смачивания, изображенный на рис.2.
Рисунок №2
Очевидно, что окружность капли, являющейся периметром смачивания, является границей взаимодействия трех сред - L - жидкости, S - твердого тела, V - газа(воздуха).
Таким образом на единице длины периметра смачивания действуют три силы Gls, G lv, Gls, силы изображены на рис.2 соответствующими векторами и направленные по касательной к соответствующей поверхности раздела, Gvs - поверхностное натяжение на границе твердое тело - газ, G lv - поверхностное натяжение на границе жидкость - газ, G lv - поверхностное натяжение на границе жидкость - твердое тело. При образовании равновесного угла, растекание капли по поверхности твердого тела прекращается,
следовательно, вдоль поверхности твердого тела все три силы уравновешивают друг друга. Тогда условия равновесия сил выражается уравнением Юнга:

где G lvcos - проекция G lv на плоскость твердого тела. Уравнения Юнга является основным уравнением теории смачивания. Достоинство его в том, что оно связывает между собой значения G lv и cos q - достаточно легко экспериментально измеряемых, со значениями Gvs-Gls -нахождение которых чрезвычайно сложно.
Например, уравнение Юнга позволяет легко рассчитать работу адгезии, характеризующую энергию взаимодействия между поверхностью твердого тела и жидкостью. Работа адгезии Wad, это работа, которую нужно совершить, чтобы оторвать от единицы поверхности твердого тела столбик жидкости.
Рисунок №3
Из рис.3 следует, что работа адгезии равна работе образования поверхности раздела жидкость - газ (Glv) и твердое тело - газ (Gvs) вместо поверхности твердое тело - жидкость, с энергией (Gls). Т.о

но из уравнения Юнга
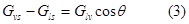
тогда
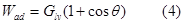
Из всего сказаного выше следует, что жидкость тем лучше смачивает твердое тело, чем меньше взаимодействие между молекулами. Например, углеводороды с поверхностным натяжением порядка 20 - 30 эрг/см практически смачивают все твердые тела(стекло, кварц, неорганические соли), ртуть с поверхностным натяжением 475эрг/см почти все не смачивает (кроме некоторых металлов).
C термодинамической точки зрения смачивание является процессом, при котором в системе из трех соприкасающихся фаз происходит уменьшение свободной энергии.
В самом деле, пусть очень тонкий слой жидкости растекается по поверхности твердого тела, которое находится в газовой среде, и пусть площадь, покрытая жидкостью, в результате этого увеличивается на D S. При этом
1) поверхность твердого тела, граничащая с газом, уменьшается на D S, в результате чего поверхностная энергия системы уменьшится Gтв.т-г 0 D S.
2) поверхность, на которой жидкость соприкасается с газом,увеличивается на D S,
в результате чего, поверхностная энергия системы увеличивается на Gтв-г г 0 D S
3) площадь метефазной поверхности между жидкостью и твердым телом увеличивается
на D S, в результате поверхностная энергия увеличивается на Gж-тв.т г 0 D S.
Т.о. изменение свободной поверхности энергии при растекании будет:

Но жидкость растекается лишь если:
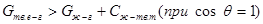
т.е.

отсюда

т.е энергия системы после растяжения F2 меньше энергии системы до растяжения F1.
ХОД ВЫПОЛНЕНИЯ РАБОТЫ.
На предметный столик кладут пластинку из материала смачивание котораго изучается (стекло, тефлон, алюминий и т.д.). На край пласлинки шприцом наносят каплю дистиллированной воды. Размер капли не должен превышать 2-3мм. В этом случае капля может считаться сферической и краевой угол смачивания может быть расчитан по формуле;
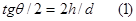
где h - ее высота, d - диаметр контакта капли с поверхностью твердого тела.
Рисунок №4
Значение h и d находятся с помощью микроскопа, объектив которого имеет сетку с делениями. Как следует из формулы (1) величина θ не зависит от размерности h и d, необходимо лишь, чтобы их размерности были одинаковы. Поэтому h и d можно выражать просто в числе делений объектива микроскопа. Т.о нахождение θ сводится к следующему;
1) настраивают микроскоп так, чтобы капля была резко видна в поле зрения микроскопа;
2) поворачивают сетку объектива так, чтобы она распологалась горизонтально, производят отсчет числа делений укладывающихся в d;
3) устраивают сетку объектива вертикально и находят h;
4) по формуле (1) расчитывают θ для данной капли на данном твердом теле;
5) для каждого твердого тела расчитывают значения θ не менее чем для 10 капель. Находят θ средние данного твердого тела, оценивают его точность;
6) опыт повторяют для 3 различных твердых тел.
Исследование эффективности ингибиторов коррозии по измерению краевых углов смачивания их растворов поверхности стали.
Постановка задачи.
При концентрации, равной критической концентрации мицеллообразования ККМ в водном растворе ПАВ произойдет образование плотного монослоя на поверхности любого твердого тела, помещенного в данный раствор. Однако,в том случае, если энергия взаимодействия молекул ПАВ с поверхностью твердого тела будет больше, чем энергия взаимодействия молекул ПАВ между собой, то на поверхности данного твердого тела заполнение монослоя может произойти и при концентрации, меньшей критической концентрации мицеллообразования. В этом случае будет наблюдаться так называемая специфическая адсорбция.
Мы предположили, что наилучшими защитными свойствами будут обладать те ингибиторы коррозии, которые из водных растворов будут в максимальной степени взаимодействовать с поверхностью стали. Об энергии взаимодействия жидкости с поверхностью твердого тела можно судить по энергии адгезии:

Следовательно, если у нас при вводе в воду ингибитора коррозии растет энергия взаимодействия стали с раствором, то этот процесс должен сопровождаться понижением краевого угла смачивания.
Имеется взаимосвязь между оптической плотностью водных растворов ингибиторов коррозии и их защитным эффектом, а оптическая плотность водных растворов и способность ингибиторов коррозии к мицеллообразованию в водной среде определяется частотой максимума, то должна наблюдаться взаимосвязь между защитным эффектом и частотой максимума.
Для повышения эффективности одних реагентов следует снижать у них частоту максимума, а для других реагентов частоту максимума наоборот, следует повышать.
Необходимо провести такую замену растворителя, которая обеспечивала бы повышение мицеллообразование ПАВ в водной среде, в результате достиглась бы более высокая оптическая плотность его растворов в воде. Повысить эффективность ингибитора коррозии помимо замены его растворителем можно в магнитной обработке его товарной формы.
Таким образом еще раз было установлено, что оптическая плотность водного раствора ингибитора коррозии, а следовательно и его способность к мицеллообразованию определяется частотой максимума его товарной формы.
При исследовании работы адгезии водных растворов ингибиторов коррозии к стали было обнаружено, что для большинства исследованных ингибиторов коррозии специфическая адсорбция их на поверхности стали снижаться по мере образования окисной пленки на поверхности стали.
Методика оценки эффективности ингибиторов коррозии.
Обработав стальную пластинку спиртовым шариком, на край пластинки шприцом нанесли каплю воды, измерили h и d, расчитали краевой угол смачивания по формуле (1).
Эти измерения повторили 5 раз и нашли среднее значение краевого угла смачивания для воды. Снова обработав аллюминевую пластинку спиртовым шариком нанесли шприцом каплю реагента ХПК-001и провели те же расчеты,что и для случая с водой.
Для ХПК-002 провели аналогичные расчеты. Затем взяв из работы лучшую смесь провели расчеты для нее.
Занесли полученные данные в таблицу и построили графики зависимости θ от C.
| C | ХПК-001 θ | ХПК-002 θ | Смесь |
| 76,6 | |||







