До нуклеозидів, виділених з нуклеїнових кислот, входять тільки 2 моносахариди D-рибоза і 2-дезокси-D-рибоза.
Ще у 1891 році Коссель вказав на те, що при гідролізі РНК (тоді ще не було цієї назви) утворюється вуглевод, який після 18 років вдалось одержати у кристалічному вигляді та ідентифікувати як новий на той час моносахарид -D-рибозу.
Значні труднощі вдалось подолати при встановлені природи моносахариду, якій входить до складу ДНК. Виявилось, що моносахарид, який в них міститься, є більш лабільним ніж D-рибоза. Однак, у 1929 році з гідролізату гуанінового нуклеозиду вдалось одержати у кристалічному вигляді вуглевод, який був охарактеризований пізніше (після його синтезу) як 2-дезокси-D-рибоза. І тільки у 1954 році було показано, що єдиний моносахарид, який входить до складу ДНК тваринного, рослинного та бактеріального походження є 2-дезокси-D-рибоза.
Розмір оксидного кільця моносахариду
На початку 50-х років було показано, що для рибози та 2-дезокси-D-рибози характерна фуранозна структура.
Формули Фішера для вуглеводів занадто громіздкі та погано відображають просторову форму молекул.
Тому були використані так звані перспективні формули Хеуорса, в яких вуглеводний ланцюг звернений випуклою стороною до спостерігача, а атом кисню фуранозного кільця знаходиться на найбільшій відстані від ока.
Молекулу зображують за законом перспективи, як це показано нижче (приймаючи умовно, що молекула має плоску будову).
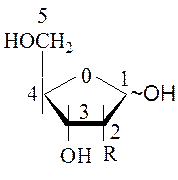
Для вуглеводів, які входять до складу мономерних одиниць нуклеїнових кислот, встановлено, що найчастіше чотири атоми п’ятичленного циклу приблизно копланарні (лежать у одній площині), а п’ятий атом - С2¢ або С3¢ виведений із площини кільця на 0,5-0,6 Å.
При цьому, якщо атоми С2¢ або С3¢ виведені по той же бік ланцюга, що і атом С5¢, такі конформації називаються ендо- конформаціями; якщо атоми С2¢ та С3¢ і атоми С5¢ розміщені по різні боки від площини кільця, маємо екзо- конформації.
Підрахунки показують, що площину зручніше всього проводити через атоми О, С1¢ та С4¢ У цьому випадку відхилення інших атомів вуглеводного кільця від площини мінімальні.
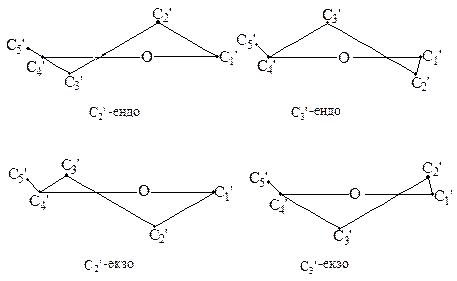
Крім основного (первинного) викривлення фуранозного кільця, також спостерігається його більш слабка вторинна деформація. Так, якщо С2¢- виведено на 0,5-0,6 Å, то С3’ - відхиляється на 0,1 Å у протилежний бік від площини кільця.
Більшість структур нуклеозидів та нуклеотидів, які були вивчені за допомогою рентгеноструктурного аналізу мають С2¢-ендо або С3’ -ендо конформацію вуглеводного залишку.
Винятком є аденозин - 3¢, 5¢ - циклофосфат (цАМФ), який має С4’- екзо- конформацію.
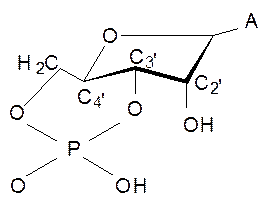
Шестичленний циклофосфат (цАМФ) існує в клітинах у вільному стані та грає ключову роль у регуляції великої кількості біохімічних реакцій (процесів).
Що стосується конформації самого фосфатного залишку, то в нуклеозид-5¢-фосфатах атом фосфору знаходиться, як правило, в транс- положенні по відношенню до атому С4’
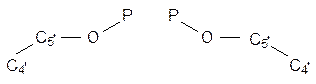
Поява нового асиметричного атому вуглецю (С1’ ) при утворенні рибофуранозного кільця у випадку D-рибози призводить до утворення двох стереоізомерних форм: a - аномера й b - аномера (приєднання аглікона екваторіальне).
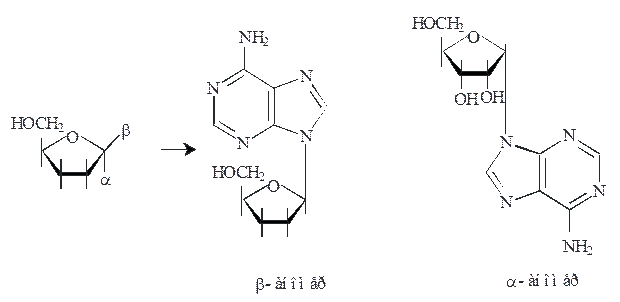 Просторова структура a- і b- аномерів аденозину
Просторова структура a- і b- аномерів аденозину
Отже, у a-глікозидах аглікон знаходиться знизу, а в b-глікозидах - зверху від площини кільця вуглеводу, тобто з однієї сторони з групою СН2ОН.
Встановлення конфігурації глікозидного центру в пуринових і піримідинових нуклеозидах хімічним шляхом було виконано Тоддом і співробітниками. Вони знайшли, що 5¢-о-толуолсульфонільні ефіри (тозильні) рибонуклеозидів при нагрівання швидко підлягають внутрішньомолекулярному алкілуванню. У випадку 2¢,3¢-О- заміщенного аденінового нуклеозида утворюється n-толуолсульфонат N3,5¢-циклоаденін-нуклеозид.
Внутрішньомолекулярна циклізація з елімінуванням тозилат-іону можлива лише за умовою, коли гетероциклічна основа та СН2ОН-група знаходяться з одного боку площини кільця вуглеводу, тобто при b-конфігурації глікозидного центру у вихідному нуклеозиді.
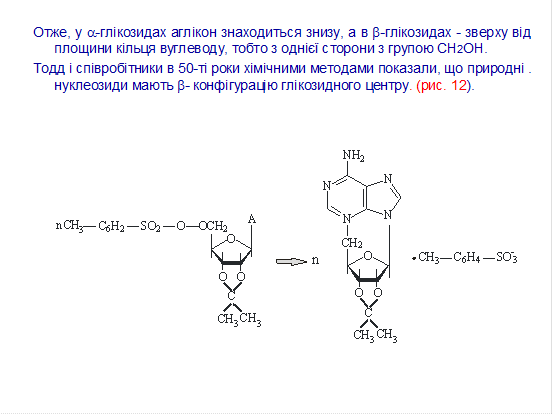
Дані рентгеноструктурного аналізу кристалічного цитидину підтвердили висновок про b-конфігурації глікозидного центру у ньому.
Конфігурацію глікозидного центру можна визначати за допомогою ЯМР спектроскопії, рівняння Карпласа:
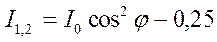
для a-аномерів (Н-екваторіальний) І1,2 » 3-5 гц
для b-аномерів (Н-аксіальний) І1,2 » 7-9 гц
Таким чином в нуклеїнових кислотах основи з’єднані з залишком цукру b-N-глікозидним зв’язком, а залишки рибози чи 2¢-дезоксирибози обов’язково відносяться до D-ряду. Нуклеозиди з’єднуються між собою за допомогою фосфодиефірного зв’язку.
Відносне розміщення залишків гетероциклічних основ та пентози
Найважливішою рисою просторової будови нуклеозидів та нуклеотидів є взаємне розміщення залишків основ та вуглеводу, яке характеризується двома параметрами.
Перший параметр - величина двогранного кута між площинами основи та вуглеводного залишку. Для усіх нуклеозидів та нуклеотидів цей кут наближається до прямого, проте ніколи не досягає його (» 800). Двогранний кут можна визначити тільки за допомогою рентгеноструктурного аналізу.
Другий важливий) параметр, що характеризує взаємне розміщення залишків основ та вуглеводу, - значення кута повороту основи навколо глікозидного зв’язку С1'-N. (Ньюменовські проекції).
Спочатку, можливі конформації нуклеозидів, які утворюються внаслідок обертання залишків основ навколо глікозидного зв’язку С-N були розглянуті на молекулярних моделях за допомогою так званого методу жорстких сфер. Суть цього методу полягає у розрахунку відстаней між певними атомами у залишках основ та вуглеводу як функції кута j. Цим шляхом було знайдено, що у випадку похідних піримідинового ряду найбільші обмеження обертання навколо глікозидного зв’язку спостерігаються внаслідок взаємодії між атомами кисню при С2 та атомом водню при С6 з замісниками при С2’ та С3’ та гетероатомом кисню вуглеводного залишку. У пуриновому ряді обмеження з’являються за рахунок взаємодії N3 з тими ж атомами фуранозного циклу. В цілому обертання залишків основи навколо зв’язку C1’-N у пуринових нуклеозидах утруднено значно менше, ніж у піримідинових.
Детальний аналіз конформацій піримідинових та пуринових нуклеозидів та нуклеотидів цим методом дозволив виявити дві області з найменшою внурішньомолекулярною взаємодією. Перша область знаходиться при значеннях j у районі -300, друга - в районі +1500
Конформації, що відповідають першій області, прийнято називати анти-конформаціями, конформації, які відповідають другій області, - син-конформаціями Ці конформації зручно представляти у вигляді Ньюменовських проекцій. Спосіб зображення полягає в тому, що:
.

Син- і анти- конформації нуклеозидів. R=H – дезоксирибо-, R=ОH – рибонуклеозиди
Згодом, теоретичні висновки були піддані детальній експериментальній перевірці за допомогою різних методів.
Як показав рентгеноструктурний аналіз, піримідинові нуклеозиди та нуклеотиди у кристалічному стані завжди знаходяться в анти- конформації. Для більшості сполук j коливається від -400 до -600.
Більшість вивчених похідних пуринового ряду також знаходилась в анти- конформації. Взаємне розташування залишків основ та вуглеводу у нуклеотидів та нуклеозидів в розчині вивчається головним чином спектрополяриметричними методами та за допомогою ЯМР. У першому випадку вивчають дисперсію оптичного обертання (ДОО) чи круговий дихроїзм (КД) розчинів нуклеозидів у УФ- області, де для цих сполук відмічається характерний ефект Коттона.
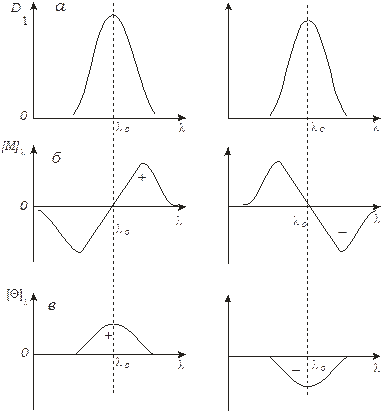
Ефект Коттона в смузі поглинання:
а – смуга поглинання речовини D; б – дисперсія оптичного обертання (ДОО); в – круговий дихроїзм (КД); (+) – позитивний Коттон-ефект; (-) – негативний Коттон-ефект.
Оскільки гетероциклічна основа оптично неактивна, а залишки рибози (чи дезоксирибози) не поглинають УФ - світло в області 230-350 нм, вважають, що знак та величина ефекту Коттона нуклеозидів та нуклеотидів визначається, головним чином, взаємним розташуванням залишків основ та пентози. Піримідинові нуклеозиди та нуклеотиди характеризуються позитивним ефектом Коттона.
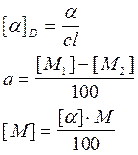
Важливо, що піримідинові нуклеозиди з фіксованою анти-конформацією, наприклад, циклічне похідне уридину, також мають позитивний ефект Коттона.
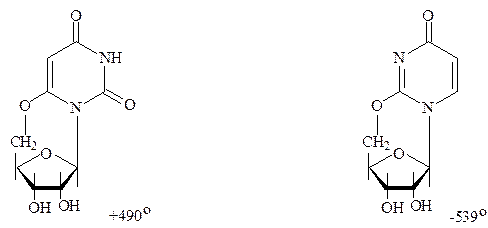
Пуринові нуклеотиди мають негативний ефект Коттона з меншою амплітудою, ніж у піримідинових нуклеотидів. Останній факт говорить про те, що обертання навколо глікозидного зв’язку для пуринових похідних відбувається легше, ніж для піримідинових.
Висновки про син- та анти- конформації мономерних компонентів нуклеїнових кислот у розчині можливо зробити за допомогою методу ЯМР. Тут досить плідним виявився наступний підхід: сучасний рівень розвитку методу дозволяє легко ідентифікувати у спектрах ЯМР піки, які дають протони, зв’язані з певними атомами гетероциклічних ядер. Положення цих піків характеризують величиною хімічного зсуву.
Як вже відзначалося, залежно від того, чи знаходиться сполука в син- або анти-конформації, з атомом С5’ (та з фосфатною групою) в нуклеозид-5¢фосфатах будуть зближені різні протони гетероциклічної основи. Відповідно до цього була вивчена залежність хімічних зсувів для певних протонів основ від рD (в D2О).
Одержані результати для АМФ та його монометилового ефіру наведені на рисунку.
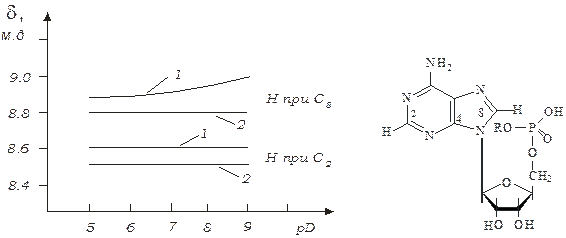
І R = H
II R = CH3 рК2 = 6,5; рК3 = 10,2
Добре видно, що при значеннях pD вище 6, коли починається вторинна дисоціація фосфатної групи, відбувається зміна величини хімічного зсуву тільки для атома водню, зв’язаного з С8 (як і слід чекати, у випадку метилового ефіру аденозин-5¢-фосфата ніяких змін не відбувається). Подібний ефект можна спостерігати лише в випадку, коли АМФ має анти-конформацію.
Аналогічні виміри були зроблені й для інших пуринових та піримідинових нуклеотидів, в усіх випадках було показано, що ці сполуки існують в анти-конформації.
Показано також, що у всіх одноланцюгових та двоспіральних оліго- та полінуклеотидах, структура яких встановлена на сьогодні, нуклеотидні залишки знаходяться тільки в анти-конформації.
Загальноприйняті символи, які використовуються для позначення структурних елементів нуклеїнових кислот.
Строге визначення символів, які описують певні структурні елементи нуклеїнових кислот, має принципове значення. Так як кількість нуклеотидів, що входять до складу нуклеїнових кислот, невелика, а їх формули досить громіздкі, то використання символіки виправдане і її вживання не викликає неоднозначності, значно спрощуючи текст (табл. 1).
Табл..1.
| Основи | Нуклеозиди | Нуклеотиди | |||
| Назва | Назва | Символ | Назва | Символ | |
| Рибонуклеозиди і рибонуклеотиди | |||||
| Аденін | Аденозин | А (А) | Аденілова кислота | 5¢ АМФ або рА | |
| Гуанін | Гуанозин | Г (G) | Гуанілова кислота | 5¢ ГМФ або рГ | |
| Тимін | Тимідин | Т (Т) | Тимідилова кислота | 5¢ ТМФ або рТ | |
| Урацил | Уридин | У(U) | Уриділова кислота | 5¢ УМФ або рУ | |
| Цитозин | Цитидин | Ц(С) | Цитидилова кислота | 5¢ ЦМФ або рЦ | |
Якщо залишок фосфорної кислоти знаходиться в 3¢- положенні вуглеводу, то відповідно символ фосфорної кислоти – р буде стояти після символу нуклеозиду, наприклад Ар – аденозин-3¢-фосфат. Для позначення 2¢-дезоксирибонуклеозидів і 2¢-дезоксирибонуклеотидів використовується символ d, наприклад, рdА - дезоксиаденілова кислота, dЦр – дезоксицитидин - 3¢-фосфат.






