NAD+ и NADP+:

Витамин PP:
1) Роль коферментов NAD+ и NADP+ в реакциях дегидрирования:

| НАД+ (или НАДФ+) – окисленная форма |
| НАДH + H+ (или НАДФH + H+) – восстановленная форма |
| . |
Д H2 + NAD+ Д + NADH + H+
(или NADP+) (или NADPH + H+)
Пример реакции с участием NAD+:

Строение флавиновых коферментов (FMN и FAD):

2) Роль коферментов FAD и FMN в реакциях дегидрирования:

| ФАД (или ФМН) – окисленная форма |
| ФАДH2 (или ФМН H2) – восстановленная форма |
| . |
| . |
(или FMN) (или FMN H2)
Пример реакции с участием FAD:

II. Трансферазы – катализируют реакции переноса функциональных групп с одной молекулы на другую.
Основные подклассы:
1. Киназы – катализируют перенос фосфатной группы, донором которой является АТФ (реже ГТФ).
Примеры:
 1)
1)
 2)
2)
Кофакторы: ионы Mg2+ и Mn2+.
Реакции, которые катализируют киназы, называются р-циями фосфорилирования.
2. Аминотрансферазы – катализируют перенос аминогруппы с аминокислоты на кетокислоту.
Пример:
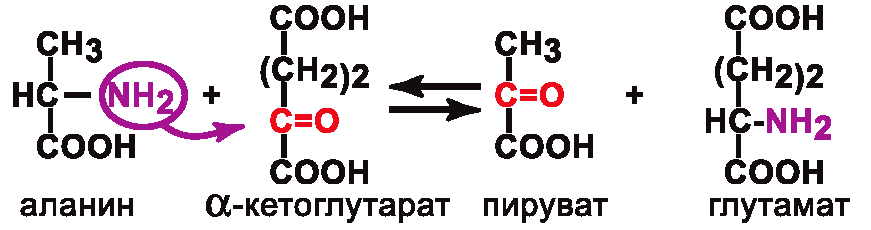
Кофермент: Пиридоксальфосфат, производное витамина B6.
3. Метилтрансферазы – перенос метильной группы.
4. Ацилтрансферазы – перенос ацильной группы.
III. Гидролазы – катализируют реакции разрыва связей в молекуле с участием воды, т.е. путем гидролиза.
Основные подклассы:
1. Фосфатазы – катализируют гидролитическое отщепление фосфатной группы:

Реакции, которые катализируют фосфатазы, называются р-циями дефосфорилирования.
2. Липазы – гидролиз связей в жирах:

Пептидазы
Гликозидазы
Эстеразы
IV. Лиазы.
Существует 2 разновидности лиаз:
1 разновидность: Лиазы, катализирующие реакции разрыва связей способом, отличным от гидролиза и окисления.
Для этой разновидности лиаз существуют подклассы:
1. Декарбоксилазы – катализируют реакции отщепления карбоксильной группы в виде CO2.
Пример:

Кофермент – Пиридоксальфосфат
(Производное витамина B6).
2. Дегидратазы – катализируют реакции отщепления воды от молекулы с образованием двойной связи.
2 разновидность: Лиазы, катализирующие реакции присоединения молекул по двойной связи.
Подклассы: Гидратазы – катализирующие реакции присоединения молекулы воды по двойной связи.

V. Изомеразы – катализируют взаимопревращение изомеров.
Подклассы: изомеразы, мутазы.
Пример:

Кофакторов нет.
VI. Лигазы.
2 разновидности:
1 разновидность: Синтетазы – катализируют реакции соединения 2-х молекул при участии энергии АТФ (реже ГТФ).
Подклассы: Карбоксилазы – катализируют реакции присоединения карбоксильной группы к молекуле в виде CO2.
Пример:
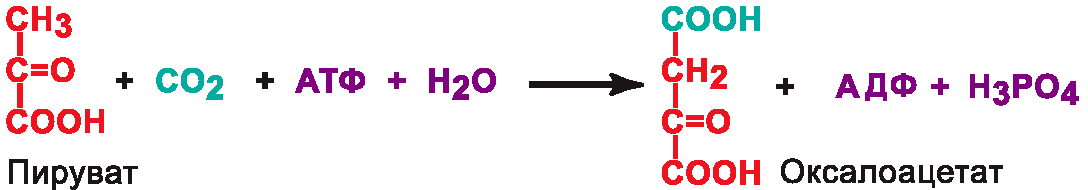
Кофермент: биотин (витамин H).
2 разновидность: Синтазы – катализируют соединение молекул при участии энергии макроэргических связей субстрата.
Активность фермента.






