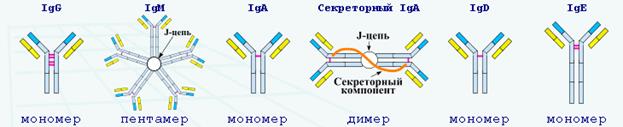
Антитела - иммуноглобулины, продуцируемые В-лимфоцитами (плазматическими клетками). Мономеры иммуноглобулинов состоят из двух тяжелых (Н-цепи) и двух легких (L-цепи) полипептидных цепей, связанных дисульфидной связью. Эти цепи имеют константные (С) и вариабельные (V) участки. Папаин расщепляет молекулу иммуноглобулина на два одинаковых антигенсвязывающих фрагмента - Fab (Fragment anligen binding) и Fc (Fragmenl crislalhzable). По типу тяжелой цепи различают 5 классов иммуноглобулинов IgG, IgM, IgA, IgD, IgE.
Они состоят из полипептидных цепей. В молекуле иммуноглобулина различают четыре структуры:
1) первичную – это последовательность определенных аминокислот. Она строится из нуклеотидных триплетов, генетически детерминируется и определяет основные последующие структурные особенности;
2) вторичную (определяется конформацией полипептидных цепей);
3) третичную (определяет характер расположения отдельных участков цепи, создающих пространственную картину);
4) четвертичную. Из четырех полипептидных цепей возникает биологически активный комплекс. Цепи попарно имеют одинаковую структуру.
Большинство молекул иммуноглобулинов составлено из двух тяжелых (H) цепей и двух легких (L) цепей, соединенных дисульфидными связями. Легкие цепи состоят или из двух k-цепей, или из двух l-цепей. Тяжелые цепи могут быть одного из пяти классов (IgA, IgG, IgM, IgD и IgE).
Каждая цепь имеет два участка:
1) постоянный. Остается постоянным в последовательности аминокислот и антигенности в пределах данного класса иммуноглобулинов;
2) вариабельный. Характеризуется большой непостоянностью последовательности аминокислот; в этой части цепи происходит реакция соединения с антигеном.
Каждая молекула IgG состоит из двух соединенных цепей, концы которых формируют два антигенсвязывающих участка. На вариабельном участке каждой цепи имеются гипервариабельные участки: три в легких цепях и четыре в тяжелых. Разновидности последовательности аминокислот в этих гипервариабельных участках определяют специфичность антитела. При определенных условиях эти гипервариабельные области могут также выступать в роли антигенов (идиотипов).
В молекуле иммуноглобулина меньше двух антигенсвязывающих центров быть не может, но один может быть завернут внутрь молекулы – это неполное антитело. Оно блокирует антиген, и тот не может связаться с полными антителами.
При энзиматическом расщеплении иммуноглобулинов образуются следующие фрагменты:
1) Fc-фрагмент содержит участки обеих постоянных частей; не обладает свойством антитела, но имеет сродство с комплементом;
2) Fab-фрагмент содержит легкую и часть тяжелой цепи с одним антигенсвязывающим участком; обладает свойством антитела;
3) F(ab)Т2-фрагмент состоит из двух связанных между собой Fab-фрагментов.
Другие классы иммуноглобулинов имеют такую же основную структуру. Исключение – IgM: является пентамером (состоит из пяти основных единиц, связанных в области Fc-концов), а IgA – димер.