0,075 г металла вытесняет из раствора соли никеля 0,183 г никеля, а из раствора кислоты – 70 мл водорода, измеренного при нормальных условиях. Определите молярные массы эквивалентов металла и никеля.
Решение.
Эквивалентом называется реальная или условная частица вещества, которая может замещать, присоединять, высвобождать или быть эквивалентна одному иону водорода в обменных или одному электрону в окислительно-восстановительных реакциях.
Масса одного эквивалента называется молярной массой эквивалента. Задачу решают по закону эквивалентов: «Массы (объемы) реагирующих друг с другом веществ пропорциональны молярным массам эквивалентов (объемам)»:
m1: m2 = Мэкв.1 : Мэкв.2.
В условии задачи количество выделившегося водорода дано в объемных единицах. Поэтому в выражении закона эквивалентов масса и молярная масса эквивалента газа заменяются объемом и молярным объемом эквивалента:
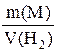 =
= 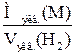 .
.
Молярный объем эквивалента атома водорода (объем, занимаемый молярной массой эквивалента газа при нормальных условиях):
22,4: 2 = 11,2 л/моль.
Рассчитываем молярную массу эквивалента металла:
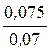 =
= 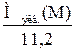 , Мэкв.(M)=
, Мэкв.(M)= 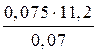 = 12 г/моль.
= 12 г/моль.
Зная молярную массу эквивалента металла, по закону эквивалентов можно определить молярную массу эквивалента никеля:
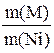 =
= 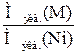 ,
, 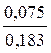 =
= 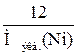 ,
,
Мэкв.(Ni)= 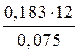
 = 29,35 г/моль.
= 29,35 г/моль.






