1. Место проведения: кафедра СНиАРП
2. Продолжительность: ___ часов (из них самостоятельная аудиторная работа ____часов)
3. Цель занятия: знакомство студентов сосновными принципами ухода за больными после обширных хирургических вмешательств, оценкой боли, видами обезболивания, правилами ухода за роженицами и родильницами.
4. Мотивационная характеристика занятия: Уход является важной составной частью лечения. Уход за больными, оперированными на органах брюшной полости, требует знаний особенностей послеоперационного периода и возможных осложнений. Правильный уход предполагает создание благоприятной бытовой и психологической обстановки на всех этапах лечения. Он строится на принципах охранительного режима, оберегающего и щадящего психику больного. Большое значение имеют создание уюта, поддержание у больного оптимистического настроения, уверенности в благополучном исходе болезни. Организация ухода и выполнение его в условиях больницы или поликлиники - обязательный и ответственный раздел деятельности медперсонала.
В результате занятия
Студент должен знать:
- Основные принципы ухода за больными после обширных хирургических вмешательств
- Оценку боли, виды обезболивания
- Правила ухода за роженицами и родильницами
Студент должен уметь:
- Оценивать уровень боли
- Оценивать темп и характер отделяемого по дренажам, пользоваться вакуум-аспирацией
- Осуществлять уход за родильницами и роженицами
Студент должен ознакомиться:
1. Шкала оценки боли
2. Правила перевязок после операции
3. Правила наблюдения за больным в ближайшем послеоперационном периоде
6.Графологические схемы, таблицы по данной теме, учебные элементы по данной теме:
Специфика хирургии органов брюшной полости обусловлена сложностью анатомии, особенностями физиологии и реакции органов на оперативное вмешательство, высокой потенциальной возможностью плохо контролируемого развития инфекции при возникновении осложнений. Несомненно, операция имеет решающее значение в лечении больного, но, пожалуй, ни в какой другой области хирургии правильно организованный и проведенный послеоперационный период не имеет такого определяющего значения для исхода. Уход за больными, оперированными на органах брюшной полости, требует знаний особенностей послеоперационного периода и возможных осложнений. После операции больного на каталке доставляют в отделение интенсивной терапии или в послеоперационную палату. К возвращению больного из операционной следует подготовить функциональную кровать, застелить ее чистым, предпочтительно стерилизованным бельем. Функциональная кровать позволяет придавать больному любое выгодное положение. В первые часы после операции больного укладывают строго горизонтально без подушки. Это делается для профилактики асфиксии при возможной посленаркозной рвоте и западении языка. Оперированные под наркозом нуждаются в постоянном наблюдении вплоть до полного пробуждения, восстановления самостоятельного дыхания и рефлексов. Когда больной просыпается от посленаркозного сна, его телу придается функционально выгодное положение с поднятым головным концом и слегка согнутыми коленями, что способствует расслаблению мышц брюшной стенки, обеспечивая покой операционной ране и благоприятные условия для дыхания и кровообращения. Если нет противопоказаний, через 2-3 часа больному разрешают согнуть ноги, повернуться на бок. Ранняя активизация больного после операции способствует скорейшему восстановлению функций всех систем организма, предотвращает возникновение осложнений, что в конечном итоге приводит к скорейшему выздоровлению. Однако, двигательный режим больного в послеоперационном периоде определяет врач, поэтому необходимую активизацию больного медсестра проводит строго по назначению лечащего врача. Практически всем больным с первых суток после операций на органах брюшной полости разрешается перемена положения тела в пределах кровати, дыхательные упражнения, массаж. Сразу же после операции на область раны с целью сужения мелких сосудов и предупреждения развития гематомы кладут пузырь со льдом. Кроме того, местное применение холода оказывает обезболивающий эффект.
Вместе с врачом средний и младший медицинский персонал принимает активное участие в наблюдении за оперированным - следят за общим состоянием, внешним видом (цвет кожи), частотой, ритмом, наполнением пульса, артериальным давлением, частотой, глубиной дыхания, мочеиспусканием, количеством мочи, отхождением газов и стула.
После операций на органах брюшной полости наблюдается временное нарушение двигательной функции желудочно-кишечного тракта, поэтому у больных могут возникнуть икота, отрыжка, тошнота, рвота, вздутие кишечника, задержка газов, стула, мочеиспускания. Икота - это внезапный сильный вдох при суженной голосовой щели вследствие судорожного сокращения диафрагмы и дыхательных мышц. Очень мучительная, продолжительная и упорная икота после операции связана с рефлекторным раздражением диафрагмального нерва или непосредственно самой диафрагмы. Уход и лечение направлены на борьбу с основным заболеванием, возможно назначение седативных и нейролептических средств, промывание желудка. Отрыжка - внезапное, непроизвольное выделение через рот газов из желудка или пищевода, иногда вместе с небольшими порциями жидкого содержимого желудка. Основными причинами отрыжки являются избыточное заглатывание воздуха или газообразование в желудке при нарушении его секреторной и двигательной функции. Избыточное количество воздуха вследствие увеличения внутрижелудочного давления рефлекторно вызывает сокращение мышц желудка и расслабление мышц входа в желудок, что и способствует возникновению отрыжки. В этой ситуации следует опорожнить желудок и промыть его с помощью зонда. В послеоперационном периоде наиболее частым и ранним осложнением является нарушение двигательной функции желудка и кишечника, выражающееся в рвоте. Рвота - сложный акт, результатом которого является извержение наружу содержимого желудка: закрывается выход из желудка и открывается вход, содержимое желудка как бы выдавливается опустившейся в результате глубоко вдоха диафрагмой и сократившимися мышцами брюшного пресса. Если состояние больного позволяет, то при возникновении рвоты его следует посадить, поддерживая голову и плечи, подставить таз, обтереть рот и дать воды для полоскания рта. При тяжелом состоянии больного нужно немедленно убрать из-под его головы подушку, опустить головной конец кровати, повернуть голову больного на бок, чтобы рвотные массы не попали в дыхательные пути, и не возникло аспирационной пневмонии или асфиксии. Под угол рта подставляют лоток или подкладывают полотенце. После рвоты больного умывают, полость рта обрабатывают влажным тампоном. В случае кровавой рвоты следует уложить больного на бок, положить холод на живот, запретить прием внутрь пищи, жидкости, лекарств. Рвотные массы не убирать до осмотра врача, которого немедленно поставить в известность о случившемся. Дальнейшие действия производятся по назначению врача.
При возникновении тошноты с целью профилактики рвоты необходимо опорожнить желудок с помощью зонда и промыть его. Для однократной кратковременной интубации желудка (в качестве предоперационной подготовки, при отравлении и т.п.) чаще всего используют толстый желудочный зонд, который вводят через рот. Это позволяет быстро освободить и промыть желудок. Для длительной интубации используют тонкий желудочный или дуоденальный зонд, который, будучи заведенным через нос, причиняет меньше беспокойств больному.
Введение зонда контактному больному облегчается его сотрудничеством в процессе манипуляции (больной делает глотательные движения). Интубация желудка у больного в бессознательном состоянии иногда требует применения прямой ларингоскопии, чтобы избежать сворачивания зонда в глотке и направить его в пищевод. Появление желудочного отделяемого по зонду указывает на правильное положение его конца. Для промывания желудка на конец зонда надевают воронку (кружку Эсмарха) емкостью 0,5 - 1 литр. Воронку держат на уровне колен больного и, наполнив ее водой, медленно поднимают выше рта больного на 25 см. Как только уровень воды в воронке достигнет ее дна, воронку опускают вниз и держат ее в прежнем положении. Содержимое желудка, разбавленное водой, начинает поступать в воронку. После наполнения воронки ее опрокидывают и выливают содержимое в таз. Процедуру выполняют несколько раз до “чистой воды”. Удобней промывание желудка производить с помощью шприца Жане, который позволяет регулировать давление при заполнении и опорожнении желудка.
После операции больные иногда не могут самостоятельно помочиться в связи с рефлекторным спазмом сфинктера и потерей у взрослых пациентов умения мочиться лежа. Поэтому при отсутствии противопоказаний больного надо посадить или поставить на ноги. У большинства пациентов после небольших операций (например, аппендэктомии) это действие приводит к желаемому результату. К мочеиспусканию побуждает льющаяся, журчащая вода (открыть кран с водой в палате), теплое судно, грелка на область мочевого пузыря, введение спазмолитиков и обезболивающих средств.
Если эти меры не оказали влияния, необходимо произвести катетеризацию мочевого пузыря. Эта процедура требует особых предосторожностей, чтобы не внести инфекцию в мочевой пузырь, так как его слизистая оболочка обладает плохой сопротивляемостью к инфекции. Для катетеризации мочевого пузыря в стерильный лоток укладывают стерильные катетеры, пинцет, флакон со стерильным вазелиновым маслом, флакон с дезинфицирующим раствором (риванол, фурацилин и т.п.). Необходимо вымыть руки щетками теплой водой с мылом, обработать спиртом, надеть стерильные перчатки. Половые органы обмывают водой и обрабатывают дезинфицирующим раствором. Закругленный конец резинового катетера держат пинцетом, а конец наружной части фиксируют между 4 и 5 пальцами. Катетер смазывают стерильным вазелиновым маслом. При введении мягкого катетера мужчине встают справа от него, левой рукой дезинфицируют головку полового члена, раскрывают отверстие мочеиспускательного канала, вводят в него закругленный конец катетера, продвигают его пинцетом в мочевой пузырь, несколько вытягивая при этом половой член. При попадании катетера в мочевой пузырь появляется моча. Женщину перед катетеризацией необходимо подмыть. Встают справа от нее, левой рукой раздвигают половые губы, находят отверстие мочеиспускательного канала и дезинфицируют окружность отверстия. Правой рукой вводят катетер до появления мочи. У мужчин пожилого возраста иногда возникают трудности катетеризации мягким катетером из-за препятствия его прохождению на уровне простатического отдела уретры (опухоль предстательной железы). Если не удается провести эластический катетер, применяют металлический. Заведение твердого катетера - это врачебная процедура.
Нарушение двигательной функции кишечника в ближайшем послеоперационном периоде проявляется вздутием живота и прекращением отхождения газов. При метеоризме - скоплении газов в кишечнике - лечебные мероприятия начинают с введения в прямую кишку газоотводной трубки, которая представляет из себя резиновую трубку длиной 30-50 см с диаметром просвета 5-10 мм. Смазав вазелином закругленный конец трубки, ее вводят в прямую кишку на глубину 20-30 см. Перед введением сестре необходимо одеть резиновые перчатки, смазать указательный палец вазелином и при необходимости помочь пальцем проводить трубку. Вводить трубку нужно не спеша, вращательными движениями, без насилия и болезненности. Трубку можно оставлять в кишке на несколько часов. Свободный конец трубки обычно опускают в подкладное судно, так как по ней может вытекать и жидкое содержимое кишечника. После удаления трубки область ануса обтирают влажным тампоном, а в случае раздражения смазывают цинковой мазью. Трубку тщательно моют водой с мылом и кипятят. После операций на органах брюшной полости, особенно по поводу перитонита, у больных наступает атония кишечника, и газоотводная трубка без предшествующей клизмы не ликвидирует вздутия кишечника. В хирургической практике клизмы применяются в основном для стимуляции моторики кишечника и его очищения от каловых масс и газов. С этой целью производят очистительные и сифонные клизмы. При постановке очистительной клизмы опорожняется нижний отдел толстой кишки путем усиления перистальтики и разжижения каловых масс. Если позволяет состояние больного, эта процедура выполняется в специальном помещении (клизменной), имеющем кушетку, стойку-штатив для подвешивания кружки Эсмарха, емкости для наконечников, дезинфицирующих средств, вазелин и т.п. Здесь же должен находиться унитаз. Кружка Эсмарха представляет из себя специальный резервуар емкостью до 1,5 литров. На дне кружки имеется отверстие с соском, на который надевают резиновую трубку длиной 1,5-2 метра и диаметром 1 см, на конце трубки имеется кран, регулирующий поступление жидкости. На свободный конец трубки одевают стеклянный или пластмассовый наконечник длиной 8-10 см. В зависимости от состояния больного укладывают на клеенку на левый бок или на спину. Под ягодицы подставляют подкладное судно. В кружку наливают 1-1,5 литра воды температуры 20-25° С. Кружку приподнимают, затем постепенно опускают трубку, заполняя ее водой и выпуская воздух, заполнив, закрывают кран. Кружку закрепляют на штативе на высоте 1 метр над уровнем больного. Наконечник смазывают вазелином. Левой рукой раздвигают ягодицы больного, правой - вводят наконечник в прямую кишку сначала вперед-назад, а пройдя сфинктер поворачивают несколько назад. Насилие при введении наконечника недопустимо. После этого открывают кран и заполняют кишечник водой. Закончив введение воды, закрывают кран, постепенно вращательными движениями извлекают наконечник из кишки. Желательно, чтобы больной удержал воду около 10 минут. После этого следует опорожнение кишечника.
Еще лучше усиливает перистальтику кишечника и способствует его очищению “гипертоническая” клизма. Вводится 200-300 мл 5-10 % раствора поваренной соли в прямую кишку. При отсутствии эффекта клизму можно повторить через 1-2 часа. Сифонная клизма применяется при невозможности очистить кишечник обычными клизмами в связи с каловыми завалами или механической кишечной непроходимостью. Используется метод сифона - многократного промывания толстой кишки по принципу сообщающихся сосудов с периодическим изменением положительного давления в просвете кишки на отрицательное. Применяют резиновую трубку длиной не менее 75 см, диаметром 1,5 см с надетой на наружный конец воронкой, вмещающей не менее 1 литра жидкости. Больного укладывают на левый бок или на спину. Конец зонда обильно смазывают вазелином и продвигают в кишку на 30-40 см, следя чтобы зонд не свернулся в ампуле прямой кишки. Воронку опускают ниже уровня тела, наливают в нее воду, дают возможность отойти воздуху, а затем поднимают вверх до высоты 1 метр. Когда кишечник будет заполнен водой, воронка опорожнится, ее опускают вниз, создавая обратный ток жидкости в воронку. При этом из кишечника выходят пузыри газа, кусочки кала и жидкие каловые массы. Жидкость сливают в таз, а в воронку наливается такая же порция чистой воды. Чередуя опускания и поднимания воронки, промывают кишечник до чистой воды. Необходимо следить, чтобы количество выведенной жидкости было не меньше количества введенной. Затем воронку снимают, а конец трубки опускают в ведро, оставляя трубку в кишке на 15-20 минут, для стока оставшейся жидкости и отхождения газов. Воронку и извлеченную трубку тщательно отмывают и стерилизуют кипячением.
В послеоперационном периоде у больных следует несколько раз в сутки осуществлять контроль за состоянием раны, обращая внимание на удобство, сохранность, чистоту и степень промокания повязки. После подавляющего большинства чистых операций рану зашивают наглухо и, наложив несколько слоев стерильной марли, фиксируют повязку наклейкой. Изредка между краями зашитой раны в повязку выводят дренаж из тонкой резины для оттока скапливающейся сукровицы, лимфы. Такая повязка может промокать и подлежит регулярной смене. Если повязка сбилась или промокла кровью, лимфой и т.п., нужно немедленно поставить в известность лечащего или дежурного врача, а после этого выполнить его назначения по смене повязки.
В некоторых случаях повязка не меняется, а только подбинтовывается, то есть поверх старой промокшей повязки накладывается новый слой марлевых салфеток или ваты, которые фиксируются новой более широкой наклейкой или бинтом.
У истощенных, онкологических, больных пожилого и старческого возраста иногда в послеоперационном периоде наблюдается расхождение краев раны брюшной стенки с выпадением внутренностей наружу. Такое осложнение называется эвентерацией, чаще оно возникает на 8-10-й день после лапаротомии, иногда в день снятия кожных швов. При кашле, резком напряжении брюшного пресса, а иногда без всяких видимых причин больной замечает, что повязка пропитывается светлым серозным или кровянистым отделяемым, которое может быть обильным. В рану из брюшной полости выпадают сальник и петли кишок, они подвергаются опасности охлаждения, загрязнения, что может привести к разлитому воспалению брюшины - перитониту или к ущемлению внутренностей и шоку.
Эвентерация требует немедленной операции, поэтому при обильном промокании повязки или видимом выпадении внутренностей необходимо немедленно вызвать хирурга, а выпавшие внутренности прикрыть стерильной салфеткой или полотенцем. Технология предстоящей операции заключается в санации органов и послойном зашивании раны брюшной стенки. В работе хирургического отделения очень часто используются различные виды дренирования полых органов, брюшной полости, ран и гнойных полостей.
Дренирование производится для удаления секрета, гноя и т.п. Различают пассивное дренирование, когда жидкость из полости, например из желчного пузыря, поступает самотеком. При активном дренировании или активной аспирации удаление содержимого из полостей производится с помощью различных приспособлений, создающих постоянное разрежение. Смена повязки вокруг дренажа производится врачом в перевязочной. В задачу медсестры входит наблюдение за дренажом и смена емкостей с отделяемым. Обычно банки меняют 1 раз в день, иногда чаще - по мере наполнения, количество жидкости измеряют. Обязательно 1 раз в сутки меняют все соединительные трубки. Емкости для дренажной системы не ставят на пол, так как там они будут мешать уборке палаты и, кроме того, могут быть опрокинуты. Банки подвязывают к кровати, на дно наливают немного дезинфицирующего средства. Трубка, опущенная на дно банки, фиксируется бинтом. Длина всей дренажной системы выбирается индивидуально, но так, чтобы не ограничивать подвижность больного. При смене емкостей количество отделяемого измеряют и записывают в историю болезни. Больные с наружными свищами органов пищеварения требуют особого ухода. Их, как правило, перевязывают один или несколько раз в сутки в перевязочной.
Дежурной медсестре нередко, особенно в вечернее и ночное время, приходится менять повязку, промокшую кишечным содержимым или желчью. При смене повязки необходимо тщательно соблюдать все правила асептики и особенно стараться не сместить дренажные трубки, которые часто фиксируют полоской бинта вокруг тела больного. При перевязках больных с желчными или панкреатическими свищами смена повязки должна производиться в присутствии врача, так как при этом можно вместе с повязкой удалить дренаж из раны. Нередко при желчных или панкреатических свищах имеется мацерация окружающей кожи от раздражения желчью и панкреатическим соком. Раздраженную кожу обмывают теплым раствором фурацилина, просушивают стерильным шариком, после чего наносят на нее толстый слой цинковой пасты или пасты Лассара. Обычно накладывают сухую асептическую повязку из нескольких слоев больших марлевых салфеток с разрезом до середины (штанишки) так, чтобы можно было через разрез пропустить дренаж. Вторую салфетку укладывают в противоположном направлении, следя за тем, чтобы разрезанная часть верхней салфетки легла на целую часть нижней.
Смена повязок у больных со свищами двенадцатиперстной и тонкой кишки производится также, как описано выше. Однако у этих пациентов чаще возникает сильная мацерация кожи. При обширном поражении кожи больные испытывают постоянную жгучую боль, причем малейшее прикосновение к разъеденной коже очень болезненно. Поэтому перед перевязкой больному целесообразно ввести обезболивающие средства. Удаляя пинцетом повязку, нужно действовать аккуратно, стараясь не причинять боль. Туалет кожи вокруг свища выполняют обмыванием теплым раствором фурацилина. Смазывать спиртом или иодом мацерированную кожу нельзя - это вызовет очень сильную боль. После обмывания кожу просушивают и наносят слой пасты с помощью стерильного шпателя. Затем свищ укрывают новой повязкой. Сформированные свищи толстой кишки обычно доставляют меньше забот. Оформленный кал легко убирается кусочками ваты, а кожа моется обычной водой с мылом. Загрязненный калоприемник меняют на чистый. Необходимо научить больного правильно пользоваться калоприемником и самостоятельно выполнять все гигиенические мероприятия. Не нужно забывать, что сам калоприемник подлежит ежедневному мытью и дезинфекции. При уходе за больными с гастростомой, то есть свищем желудка, нужно следить за чистотой кожи вокруг трубки и за ее хорошей фиксацией.
Борьба с болью является одной из наиболее важных задач в послеоперационном периоде. Эффективное обезболивание способствует ранней реабилитации больного, снижает частоту возникновения послеоперационных осложнений и хронических болевых синдромов. В настоящее время имеется широкий выбор лекарственных препаратов и методов немедикаментозного обезболивания, однако многочисленные исследования, проведенные в разных странах, выявили недостаточную анальгезию раннего послеоперационного периода почти у 50% больных [6,7,11]. Поэтому знание современных принципов обезболивания после операции имеет большое практическое значение.
Этапами адекватного обезболивания являются:
1. Предоперационная оценка интенсивности и длительности болевого синдрома (табл. 1, табл. 2).
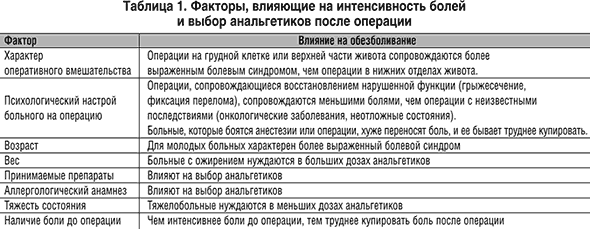
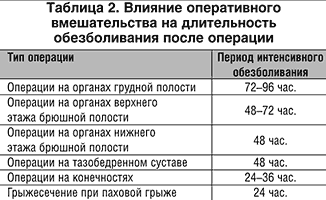
2. Построение плана лечения боли (анальгетик(и), пути введения, частота и т.д.) (табл. 3).
3. Лечение боли.

4. Послеоперационная оценка эффективности обезболивания (для корректировки плана лечения боли при недостаточном обезболивании). Для определения качества обезболивания после операции наибольшее распространение получила визуальная аналоговая шкала (рис. 1). Больной ставит на линии вертикальную отметку, соответствующую уровню боли. Обезболивание признается адекватным, если больной не отмечает болей в покое, а при движении, кашле возникает умеренная боль, не ограничивающая их.

Рис. 1. Визуальная аналоговая шкала
Опиоидные анальгетики реализуют свое действие через опиатные рецепторы, расположенные на спинальном и супраспинальном уровнях, и являются основной группой лекарственных средств для лечения боли в послеоперационном периоде.
В то же время после обширных внутриполостных хирургических вмешательств для достижения адекватного обезболивания у каждого третьего больного требуется введение опиоидов в дозах, превышающих стандартно рекомендуемые [3]. Увеличение дозы опиоидных анальгетиков сопровождается выраженными побочными реакциями (сонливостью, угнетением дыхания, тошнотой, рвотой, парезом желудочно–кишечного тракта, нарушениями мочеиспускания), поэтому в настоящее время признано, что монотерапия опиоидными анальгетиками не всегда достаточно эффективна, а иногда даже опасна.
Кроме того, при традиционном подкожном и внутримышечном введении трудно поддерживать оптимальную концентрацию опиоидов в плазме, что может сопровождаться либо угнетением дыхания, либо недостаточным обезболиванием.
Болюсное введение опиоидных анальгетиков интратекально или эпидурально обеспечивает хорошее обезболивание до 24 часов, однако даже небольшие дозы вводимых препаратов (в десятки раз меньше, чем при внутримышечном введении) могут сопровождаться побочными и токсическими эффектами.
Трамадол (Трамал) – это опиоидный агонист, стоящий особняком среди всех представителей опиоидов этого класса, прежде всего потому, что в отличие от них он не принадлежит к наркотическим средствам. Это подтверждено обширным клиническим опытом его использования во всем мире и специальными научными исследованиями его наркотического потенциала.
В отличие от других опиоидных агонистов трамадол имеет двойной механизм действия. Установлено, что анальгезия, вызванная трамадолом, полностью не устраняется опиоидным антагонистом налоксоном и наряду с опиоидным механизмом реализуется путем дополнительного торможения болевой импульсации с участием серотонин– и адренергической систем. Т.е. по механизму анальгетического действия трамадол не полностью идентичен другим опиоидным агонистам.
Анальгетический потенциал трамадола по данным разных авторов, составляет от 0,1 до 0,2 от потенциала морфина, он равен или несколько превосходит потенциал кодеина; по эффективности 50 мг трамадола эквивалентны 1000 мг метамизола, т.е. трамадол принадлежит к анальгетикам, предназначаемым для лечения боли сильной и умеренной интенсивности.
В многочисленных исследованиях не установлено значимого угнетения дыхания у послеоперационных пациентов под влиянием Трамала в диапазоне терапевтических доз от 0,5 до 2 мг на 1 кг массы тела даже при внутривенном болюсном введении, тогда как морфин в терапевтической дозе 0,14 мг/кг статистически достоверно и значительно снижает частоту дыхания и повышает напряжение СО2 в выдыхаемом воздухе.
Нестероидные противовоспалительные препараты (НПВП) обладают анальгетическими и противовоспалительными свойствами. Механизм действия связан с ингибированием циклооксигеназы, которая катализирует расщепление арахидоновой кислоты на различные простагландины, являющиеся основными медиаторами воспаления. Кроме того, НПВП оказывают влияние на проведение болевых импульсов в центральной нервной системе. НПВП считаются эффективными анальгетиками при легкой или умеренной боли. Побочные эффекты связаны с основным действием НПВП – подавлением синтеза простагландинов и развиваются, как правило, при длительном применении. К ним относят НПВП–гастродуоденопатию (диспептические расстройства, эрозии и язвы желудка и двенадцатиперстной кишки); нефротоксичность; нарушение свертывающей активности крови (торможение аггрегации тромбоцитов и образования протромбина в печени); гематотоксичность (снижение количества эритроцитов и лейкоцитов в крови). Выраженность побочных эффектов уменьшается при использовании селективных ингибиторов циклооксигеназы–2 [8].
Методы регионарной анестезии широко применяются при выполнении оперативных вмешательств для уменьшения побочных эффектов системного обезболивания и могут быть использованы в послеоперационном периоде.
Существует несколько способов применения местных анестетиков:
– инфильтрационная анестезия ран;
– блокада периферических нервов и сплетений;
– эпидуральная или интратекальная (спинномозговая, спинальная) анестезия.
Инфузия местных анестетиков позволяет обеспечить эффективную анальгезию, однако может сопровождаться артериальной гипотензией, моторным блоком, тошнотой и расстройствами мочеиспускания.
При выраженном болевом синдроме применяют катетеризацию эпидурального пространства для многократного введения анальгетика – длительная эпидуральная анестезия (реже применяется длительная спинальная анестезия).
Клонидин является агонистом a–норадренергических рецепторов и тормозит передачу болевых импульсов за счет воздействия на постсинаптические рецепторы.
Кетамин и сульфат магния снижают проведение болевых импульсов и препятствуют возбудимости нейронов на различных уровнях центральной нервной системы (ЦНС).
Несмотря на большое число обезболивающих препаратов, применение каждого из них сопряжено с риском развития побочных эффектов, поэтому в настоящее время одним из основных принципов послеоперационного обезболивания является принцип сбалансированного обезболивания, когда используется комбинация опиоидных анальгетиков, нестероидных противовоспалительных средств, местных анестетиков и препаратов других групп (кетамин, сульфат магния).
Одновременное применение препаратов разных групп (трамадол и ацетаминофен (Залдиар)) позволяет блокировать проведение ноцицептивных (болевых) импульсов на всех уровнях, уменьшает дозу каждого из анальгетиков, улучшает качество обезболивания и значительно снижает число побочных эффектов. Препарат может применяться после малотравматичных оперативных вмешательств (грыжечение, секторальная резекция молочной железы, резекция щитовидной железы и т.д.), при этом многие авторы до сих пор полагают, что монотерапия НПВП достаточна для эффективного обезболивания [3,12].
При более травматичных операциях (большинство полостных операций) наиболее оптимальным является сочетание НПВП с опиоидными анальгетиками (Залдиар). Синергизм анальгетического действия опиоидов и НПВП позволяет на 20–60%. снизить потребность в опиоидных анальгетиках и уменьшить их побочные эффекты (улучшение функции внешнего дыхания, быстрое восстановление моторики желудочно–кишечного тракта) [5,6,9].
Трамадол и ацетаминофен (парацетамол) – два анальгетика, доказавшие свою эффективность при широком спектре заболеваний, и послужили основой для создания комбинированного препарата Залдиар (трамадол 37,5 мг/ацетаминофен 325 мг). Использование такой комбинации препаратов оправдано, в первую очередь, с точки зрения фармакокинетических и фармакодинамических особенностей препаратов.
Механизм действия ацетаминофена (парацетамола) недостаточно понятен. Предполагают, что он имеет центральное действие, при этом анальгезия достигается за счет повышения порога боли, а антипиретическое действие – через торможение простагландин–синтетазы в гипоталамусе. Ацетаминофен назначают при слабых и умеренных болях, чаще при артрозе крупных суставов при небольшой выраженности воспаления.
Время достижения максимальной концентрации в сыворотке крови (Тmax) у ацетаминофена и у трамадола различные. Исходя из фармакокинетических особенностей, применение комбинации препаратов является обоснованным: ацетаминофен развивает ранний аналгетический эффект, в то время как трамадол реализует свое действие позже, и, обладая большим периодом полувыведения, обеспечивает пролонгацию аналгезии. Использование указанной комбинации лекарственных средств проявило большую клиническую эффективность, чем прием трамадола 75 мг в качестве монотерапии.
По результатам проведенного рандомизированного двойного слепого плацебо–контролируемого исследования у 1783 больных (одонтогенный болевой с–м, послеоперационные больные ортопедического, гинекологического профиля), комбинация трамадол/ацетаминофен оказалась более эффективна, чем применение обоих препаратов в отдельности [6]. По данным других авторов, применение 2 таблеток Залдиара (трамадол 75 мг + ацетаминофен 750 мг) у больных при одонтогенных оперативных вмешательствах оказывало более быстрый и длительный эффект, чем монотерапия трамадолом. Наиболее часто принцип сбалансированной анальгезии применяется после хирургических вмешательств, сопровождающихся большой травматичностью (расширенные онкологические операции с лимфаденэктомией; операции, выполняемые торакоабдоминальным доступом; резекция пищевода с пластикой желудочной трубкой или толстой кишкой; обширные резекции печени и т.д.). Для повышения качества послеоперационного обезболивания в последние годы применяется методика контролируемой пациентом анальгезии (КПА). Устройство для КПА представляет собой автоматический шприц с микропроцессорным управлением, приводимый в действие кнопкой, находящейся в руках больного. Применение КПА позволяет снизить дозу анальгетиков (и их побочных и токсических эффектов) и нивелировать индивидуальные особенности действия препаратов у различных больных. КПА на основе внутривенного введения морфина показана больным с низким риском развития сердечно–легочных осложнений и требуется введение опиоидных анальгетиков, как минимум, в течение 2 суток после операции. В данной методике нуждаются от 10 до 30% больных [6].
Условием проведения КПА являются восстановление сознания и адекватность больного, а также обязательное мониторирование жизненно важных функций, что вместе с высокой стоимостью устройств для КПА ограничивает применение метода. Традиционная концепция послеоперационного обезболивания предполагала использование анальгетиков только после появления сильных болей. Однако в настоящее время доказано, что обезболивания достичь гораздо труднее, если ощущение боли уже сформировалось. Во время оперативного вмешательства возникает травма тканей, которая сопровождается формированием большого количества ноцицептивных (болевых) импульсов. Затем из поврежденных тканей выделяются медиаторы воспаления и другие биологически активные вещества, которые, взаимодействуя с мембраной нервных окончаний ноцицептивных рецепторов, повышают их чувствительность к механическим и термическим факторам. Развивается сенситизация (повышение чувствительности) ноцицепторов в области повреждения, что проявляется снижением порога их активации (периферическая сенситизация) [1,2]. Поток ноцицептивных импульсов, возросший вследствие периферической сенситизации, приводит к увеличению возбудимости спинальных нейронов, участвующих в проведении болевых импульсов (центральная сенситизация).
При возникновении состояния сенситизации стимулы, которые в норме не вызвали бы боли, начинают восприниматься, как болевые, а болевые стимулы начинают восприниматься, как гиперболевые (гиперальгезия).
Возникшая вследствие повреждения тканей сенситизация ноцицептивных нейронов ЦНС может сохраняться несколько часов или дней после прекращения поступления ноцицептивных импульсов с периферии.
Принцип предупреждающего обезболивания (профилактика боли) заключается в применении анальгетиков (как правило, НПВП) до начала операции, что позволяет предотвратить возникновение периферической и центральной сенситизации (рис. 2) [4,10].
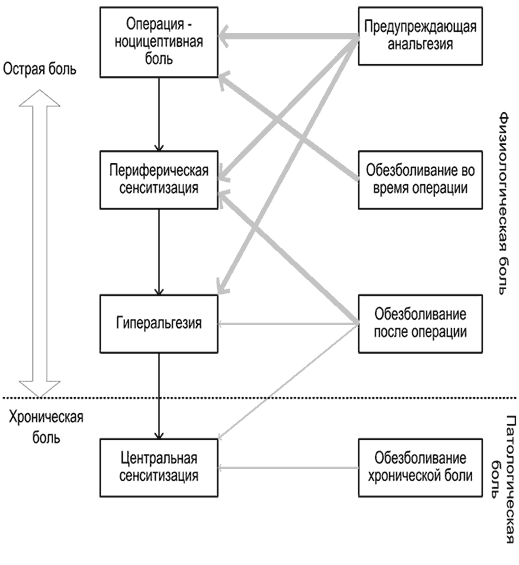
Рис. 2. Стратегия лечения боли (цит. по Kissin I., 2000 с изменениями) Толщина стрелок соответствует эффективности воздействия
Оптимального метода послеоперационного обезболивания в настоящее время не существует. Выбор лекарственных препаратов и методов обезболивания определяется опытом анестезиолога, материальными возможностями и другими факторами.
Приводим пример возможной схемы обезболивания при операции гастрэктомии с расширенной лимфаденэктомией в объеме D2.
Премедикация – накануне операции в 22:00 и за 20–60 минут до операции внутримышечно вводится мидазолам (0,07–0,1 мг/кг) и 100 мг кетопрофена. Катетеризация эпидурального пространства осуществляется на уровне ThVII–ThIX. Начальная доза местного анестетика составляет 6–10 мл ропивакаина (или бупивакаина 0,25%) с добавлением 50–100 мг фентанила, затем постоянная инфузия ропивакаина (8–12 мл/час) и фентанила (2–2,5 мкг/кг/час). Поддержание анестезии осуществляется любым доступным способом (нейролептоанестезия, тотальная внутривенная анестезия). В послеоперационном периоде для эпидуральной анестезии применяются меньшие концентрации местных анестетиков (0,2% ропивакаин или 0,2% бупивакаин). Минимально эффективная доза подбирается путем титрования (скорость инфузии при этом может варьировать от 4 до 12 мл в час). При недостаточной анальгезии не следует увеличивать скорость инфузии или концентрацию анестетика, а необходимо применить НПВП, другие ненаркотические анальгетики или опиоиды.
Важно отметить, что некупирующийся болевой синдром в послеоперационном периоде требует исключения осложнений после операции (несостоятельности швов, панкреонекроза и др.).






