Полимер (от греч. «поли» - много, «мерос» - часть) – это сложнаямного звеньевая цепь, образующаяся при соединении друг с другом простых молекул – мономеров.
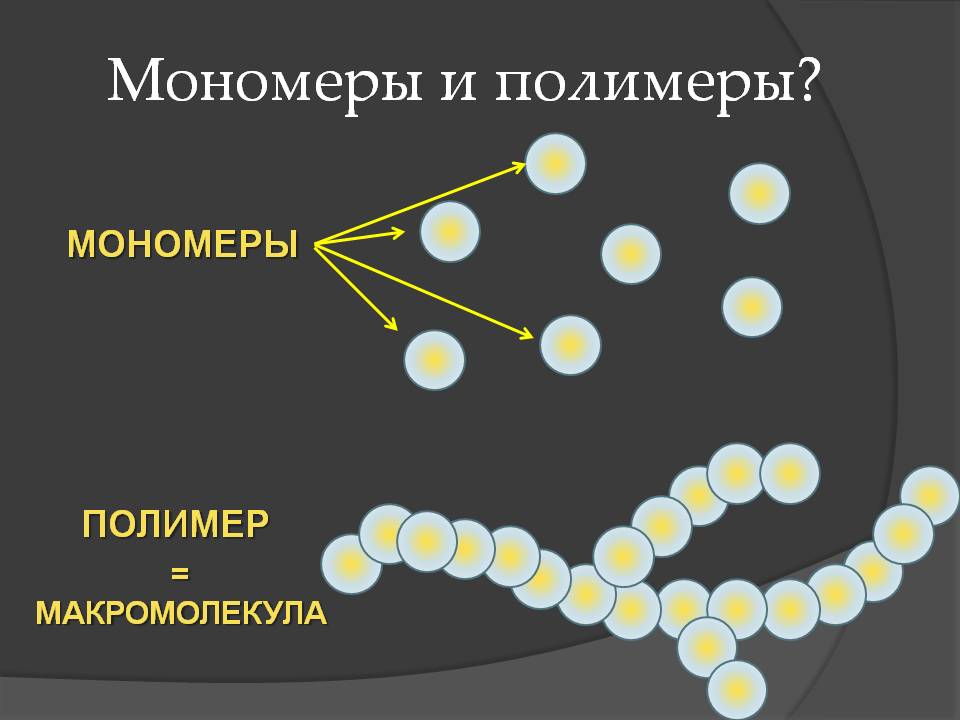
Биополимер – биологический полимер.
1) Углеводы (Сахара) – органические соединения, в состав которых входит C, H, O.
· Простые сахара (моносахариды): глюкоза, фруктоза - гидрофильны, имеют сладкий вкус и являются мономерами.
· Сложные сахара (полисахариды): целлюлоза, крахмал, гликоген, хитин – гидрофобны, безвкусны.
· Дисахариды – сахароза, мальтоза (образованы двумя мономерами).
Функции углеводов:
v Энергетическая (сахароза, глюкоза – основные источники энергии);
v Структурная (целлюлоза образует клеточную стенку растений);
v Резервная/запасающая (крахмал запасается в клетках растений, гликоген – в клетках грибов и животных);
v Защитная (хитиновый покров у беспозвоночных).
2) Жиры (Липиды) – состоят из остатков жирных кислот и глицерина.
Липиды, содержащие остаток фосфорной кислоты, называют фосфолипидами.
· Не растворимы в воде, но растворимы в некоторых органических соединениях;
· обладают плохой теплопроводностью;
· бывают твердыми (животного происхождения) и жидкими (масла).
Функции жиров:
v Структурная (фосфолипиды входят в состав клеточных мембран);
v Энергетическая (при расщеплении 1 г. жира выделяется 38,9 кДж энергии);
v Запасающая/резервная (при расщеплении 1 г. углеводов выделяется 17,6 кДж энергии, поэтому запасать питательные вещества в виде жиров энергетически выгодно);
v Защитная (воск на плодах растений, копчиковая железа у водоплавающих птиц);
v Терморегуляция (под кожей образуется жировая клетчатка)
v Регуляторная (липиды входят в состав некоторых гормонов и обеспечивают гуморальную регуляцию).
v Барьерная (жиры не пропускают воду с растворенными в ней веществами в клетку).
3) Белки (полипептиды) – биополимеры, мономерами которых являются аминокислоты.
В построении белков живых организмов участвует 20 аминокислот.
Строение аминокислоты: NH2 – CH – COOH
R

Структуры белка:
I. Первичная. Аминокислоты соединяются линейно с помощью пептидной связи (ковалентной).
II.Вторичная. Линейная цепь аминокислот закручивается в спираль и между витками образуется водородная связь.
III.Третичная. Спираль сворачивается в клубок - глобулу или вытягивается и образует фибриллу. (глобулярный белок: гемоглобин, иммуноглобулин; фибриллярный белок: коллаген, кератин). Связь образуется между радикалами (дисульфидный мостик). Белок выполняет свои функции только в состоянии глобулы.
IV. Четвертичная. Представлена несколькими глобулами.


Под действием высокой или низкой температуры, радиации и т.д. белок меняет свою структуру, т.е. происходит распад белка – денатурация. В результате чего белок теряет свою активность. Если в процессе распада не была нарушена первичная структура, то белок восстановится, т.е. произойдет ренатурация.
Функции белка:
v Структурная/строительная (входит в состав всех компонентов клетки);
v Транспортная (белок гемоглобин транспортирует кислород в крови);
v Ферментативная/каталитическая (фермент – катализатор белковой природы; катализатор – ускоритель химической реакции);
v Защитная (белки иммуноглобулины (антитела) вырабатываются организмом для уничтожения антигенов (чужеродных белков) – один из механизмов иммунитета);
v Регуляторная (белки входят в состав некоторых гормонов, обеспечивая гуморальную регуляцию);
v Сигнальная (белок –рецептор родопсин находится в сетчатке глаза и преобразует световую энергию в электрическую);
v Сократительная (белок миозин участвует в сокращении мышечных волокон);
v Энергетическая (при недостатке углеводов и жиров окисляются молекулы аминокислот).
4) Нуклеиновые кислоты – полимерные цепи, мономерами которых являются нуклеотиды.
Впервые нуклеиновые кислоты были обнаружены в ядрах клеток, в связи с чем получили свое название (лат. nucleus-«ядро»).
Виды нуклеиновых кислот:
1. ДНК – дезоксирибонуклеиновая кислота;
2. РНК – рибонуклеиновая кислота.
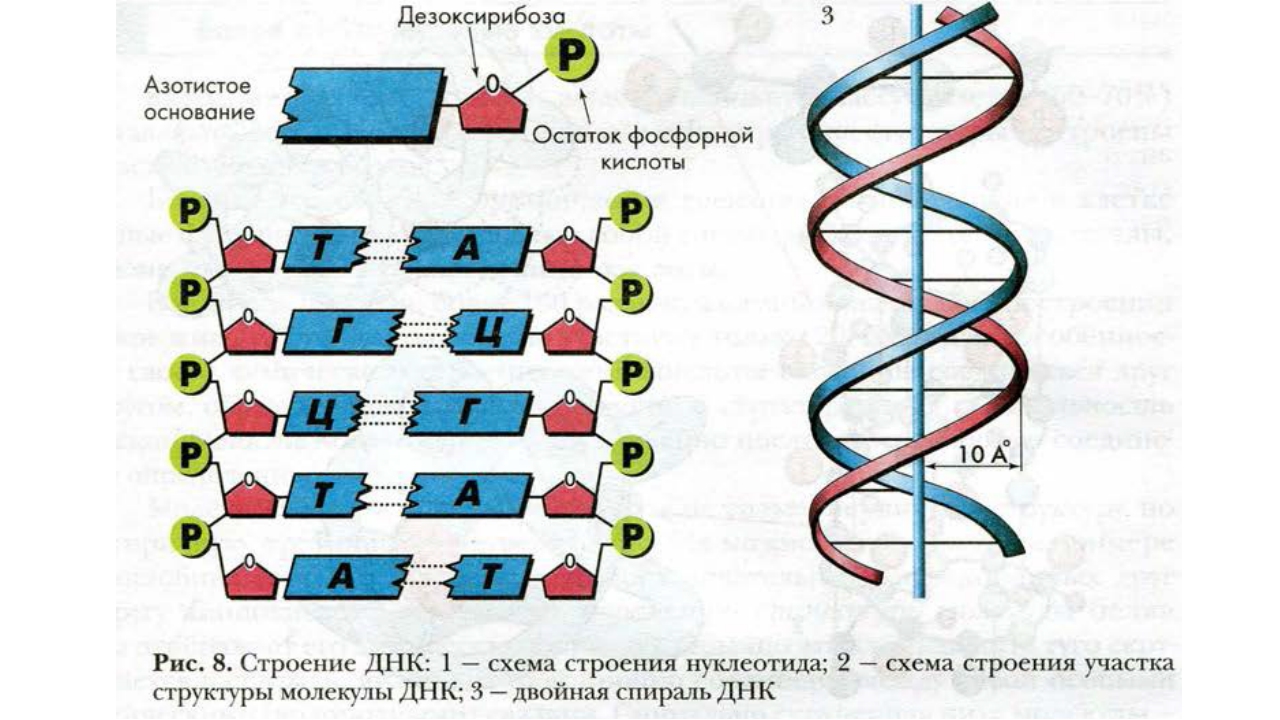
ДНК – двуцепочечная спиральная молекула.
Структуру ДНК открыли в 1953 году Крик и Уотсон.
Функция ДНК: хранение и передача наследственной информации.
| Дезоксирибоза |
| Азотистое основание (А, Т, Г, Ц) |
фосфорной кислоты
Две цепи молекулы ДНК соединяются водородными связями, которые возникает между азотистыми основаниями. Азотистые основания соединяются не случайно, а избирательно то есть по принципу комплиментарности. Так аденин всегда стыкуется с тимином и образует 2 водородные связи, гуанин с цитозином и образует 3 связи.
На принципе комплиментарности основана способность ДНК удваиваться – репликация (редупликация).
Соседние нуклеотиды одной цепи молекулы ДНК соединяются сахаро-фосфатными связями.
| В ДНК Т=А Г Ц |
| Т У |
| В РНК У=А Г Ц |
ДНК у эукариот находится в ядре, митохондриях и пластидах;
у прокариот – в цитоплазме.
РНК – одноцепочечнаянеспиральная молекула.
| Рибоза |
| Азотистое основание (А, У, Г, Ц) |
фосфорной кислоты
Нуклеотид РНК имеет строение схожее с нуклеотидом ДНК, отличия заключаются в том, что место тимина (Т) занимает урацил (У), а углевод – рибоза.
РНК находится в ядре, цитоплазме и некоторых органоидах клетки.
Виды РНК:
1. Информационная (иРНК) или матричная (мРНК) – считывает и переносит генетическую информацию с ДНК;
2. Транспортная (тРНК) – приносит аминокислоты к месту синтеза белка;
3. Рибосомальная (рРНК) – содержится в рибосомах.
Все виды РНК участвуют в синтезе белков.
ДНК1: А – Т – Г – А – Ц – Ц – Т – Г – Ц – А – А – Т
ДНК2: Т – А – Ц – Т – Г – Г – А – Ц – Г – Т – Т – А
иРНК: А – У – Г – А – Ц – Ц – У – Г – Ц – А – А – У
триплет (кодон)
Один триплет кодирует одну амнокислоту.
| 1 трип = 3 нукл 1 трип = 1 а/к |
АТФ (Аденозинтрифосфорная кислота) – это мононуклеотид, состоящий из азотистого основания (аденина), углевода (рибозы) и трех остатков фосфорной кислоты.
Схема строения нуклеотида АТФ

АТФ – универсальный накопитель и переносчик энергии (E). Между остатками фосфорной кислоты образуются макроэргические связи, распад которых приводит к выделению значительного количества энергии (40 кДж).
АТФ – P = AДФ (аденозиндифосфат); АДФ – P = АМФ (аденозинмонофосфат).






