-
|
· химически чистая вода не проводит ток;
·  растворы солей, кислот, щелочей (электролиты) проводят электрический ток
растворы солей, кислот, щелочей (электролиты) проводят электрический ток
- Зависимость сопротивления R(t)

1.
|
Электролитическая диссоциация – явление расщепления молекул вещества на ионы под действием растворителя.
Степень электролитической диссоциации - a
 |
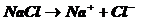
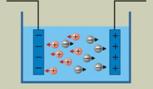
2. Взаимодействие ионов с электродами
 |  | ||||
 | |||||
Раствор CuCl 2
 Электролиз – выделение вещества на электродах при прохождении тока через электролит.
Электролиз – выделение вещества на электродах при прохождении тока через электролит.
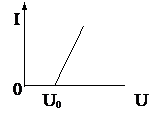
3. Вольтамперная характеристика
-
|

k – электрохимический эквивалент [k] = 1 кг/Кл
-
|
· электрометаллургия;
· гальванопластика;
· рафинирование;
· гальваностегия
· электрополирование.
Вопросы и задания по теме «ЭЛЕКТРИЧЕСКИЙ ТОК В ЖИДКОСТЯХ»
1.1 Пользуясь таблицей растворимости, определить какие из данных веществ являются электролитами: H2SO4, H2SiO3, NaCl, CuSO4, AgNO3, C6H12O6.
2.1 Каким образом можно экспериментально доказать справедливость закона Фарадея, как следствия построенной модели?
2.2 До каких пор может продолжаться электролиз раствора медного купороса, если в ванне электроды медные? Угольные?
2.3 Почему водный раствор сахара и спиртовые растворы красок не являются электролитами?
2.4 Степень электролитической диссоциации показывает какую часть составляют распавшиеся молекулы от общего числа молекул. От каких факторов зависит эта характеристика?
3.1 Две ванны с раствором CuSO4 и CuCl соединены последовательно. Одинаковое ли количество меди выделяется в ваннах при протекании тока?
3.2 Как изменится сила тока в электролитической ванне, если:
а) увеличить напряжение на зажимах лампы;
б) увеличить концентрацию электролита;
в) сблизить электроды;
г) частично приподнять электроды из раствора;
д) нагреть электролит?
Ответы проверить экспериментально.
Экспериментальная задача
Электролиз проводится с раствором медного купороса. Какие вещества выделяются на электродах? Запишите окислительно-восстановительные реакции, происходящие на катоде и электроде.
Домашнее задание
1. Используя материал учебника, записать формулу 2 закона Фарадея.
Как можно экспериментально определить величину заряда?
Как рассчитать элементарный заряд, не проводя никаких измерений?
Чем отличаются заряды электрона и ионов натрия, меди, хлора?
2. Используя дополнительную литературу, подготовьте доклады на темы:
«Практическое применение электролиза»,
«Электролиз в нашем регионе»






