В печени человека присутствуют специфические пиридоксальфосфатзависимые ферменты сериндегидратаза, треониндегидратаза, катализирующие реакции неокислительного дезаминирования аминокислот серина и треонина.
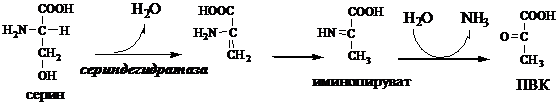

Внутримолекулярное дезаминирование
Внутримолекулярноедезаминирование характерно для гистидина. Реакцию катализирует гистидаза (гистидин-аммиаклиаза). Эта реакция происходит только в печени и коже.

Лекция 4.Обезвреживание аммиака: восстановительное аминирование 2-оксоглутарата и синтез глутамина.
Аммиак токсичен для центральной нервной системы, поэтому в организме существуют процессы, в которых происходит связывание (дезактивация, обезвреживание) аммиака. За это отвечают системы обезвреживания аммиака, в результате функционирования которых в крови поддерживается его низкая концентрация (около 0,05 ммоль/л). Условно выделяют местные (тканевые), в результате которых происходит временное связывание аммиака; и общие (конечное обезвреживание) пути обезвреживания NH3, благодаря которым он выводится из организма.
Основным путем связывания аммиака в мозге является образование глутамина:
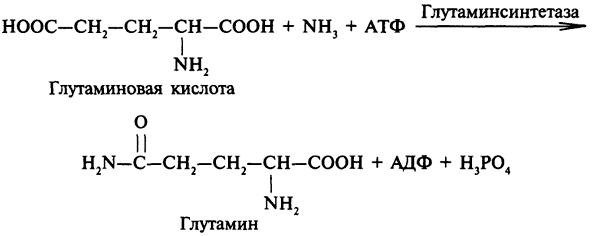
Глутамин может использоваться не только для синтеза белка, но и для других метаболических процессов, следовательно его можно рассматривать как хранилище аммиака. Подобным образом происходит образование аспарагина, катализируемое соответствующейсинтетазой.
Орнитиновый цикл синтеза мочевины.
Основным путем связывания аммиака является орнитиновый цикл, называемый также циклом мочевины.
Первой реакцией орнитинового цикла является процесс образования карбамоилфосфата из аммиака и оксида углерода (IV) при участии АТФ. Катализирует этот процесс карбамоилфосфатсинтетаза. Интересно отметить, что в данном процессе принимает участие две молекулы АТФ, одна из которых является донором остатка фосфорной кислоты, а другая выполняет энергетическую функцию:
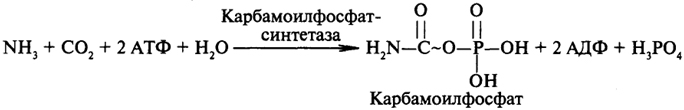
Следующая стадия процесса - перенос карбамоила на аминогруппу
бокового радикала аминокислоты орнитина - происходит довольно быстро. Равновесие этой реакции сдвинуто в сторону синтеза цитруллина. Последующая цепь реакций приводит к конечному продукту обмена азота - мочевине:
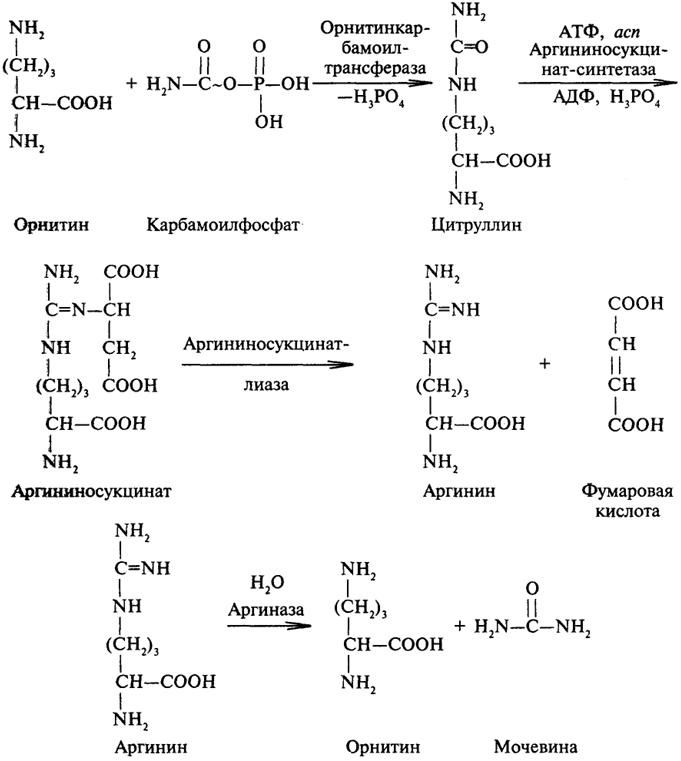
Образование мочевины происходит исключительно в клетках печени - единственном органе, где локализован фермент аргиназа. Мочевина выделяется из клеток печени в кровь и выводится из организма с мочой.
Транспорт аммиака.
Транспортными формами аммиака из тканей в печень являются глутамин, аланин, в меньшей степени аспарагин и глутамат, некоторое количество аммиака находится в крови в свободном виде. Глутамин и аланин являются наиболее представленными, их доля среди всех аминокислот крови составляет до 50%.
Целевыми органами для транспорта аммиака являются печень, почки и кишечник.
печень:
а) аспарагин и глутаминдезаминируются соответственно аспарагиназой и глутаминазой, образующийся аммиак используется для синтеза мочевины,
б) аланин вступает в реакции трансаминирования сα-кетоглутаратом,
в) глутаминовая кислота подвергается окислительномудезаминированию,
кишечник:
а)часть глутаминадезаминируетсяглутаминазойи NH3выделяется в кровь
б) глутамат вступает в трансаминирование с пируватом, амино-азот переходит на аланин и с ним поступает в печень,
почки:
а)образование и удаление аммонийных солейглутамата, глутамина и аспарагина
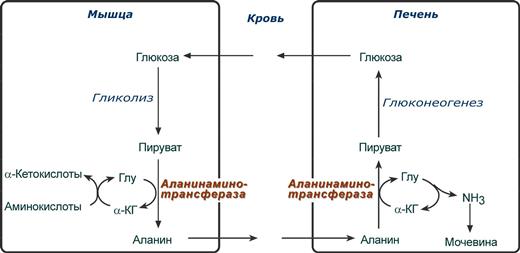
Глюкозо-аланиновый цикл
В мышцах акцептором лишнего аминного азота является пируват. При катаболизме белков в мышцах происходят реакции трансаминирования аминокислот, образуется глутамат, который далее передает аминоазот на пируват и образуется аланин. Из мышц с кровью аланин переносится в печень, где в обратной реакции передает свою аминогруппу на глутамат. Образующийся пируват используется как субстрат в реакциях синтеза глюкозы (глюконеогенез), а глутаминовая кислота дезаминируется и аммиак используется в синтезе мочевины.
Гипераммонемии.
Аммиак является токсичным соединением. Предельно допустимый уровень аммиака в крови 60 мкмоль/л(при норме 11-20мкмоль/л)При повышении концентрации аммиака (гипераммониемия) до предельных величин может наступить кома и смерть. При хроническойгипераммониемии развивается умственная отсталость.
Выделяют наследственные иприобретенные (вторичные) формы гипераммониемий.
Наследственные формы гипераммониемии вызваны генетическим дефектом любого из пяти ферментов синтеза мочевины.Соответственно ферменту заболевание делится на пять типов.Наиболее частой является гипераммониемия типа ΙΙ, связанная с недостатком орнитин-карбамоилтрансферазы.
Первичными признаками гипераммониемии являются сонливость, отказ от пищи, рвота, беспокойство, судороги, нарушение координации движений.






