Простые ферменты состоят только из аминокислот – например, пепсин, трипсин, лизоцим.
Сложные ферменты (холоферменты) имеют в своем составе белковую часть, состоящую из аминокислот – апофермент, и небелковую часть – кофактор. Кофактор может называться коферментом или простетической группой.
Примеры: сукцинатдегидрогеназа (содержит ФАД) (в цикле трикарбоновых кислот), аминотрансферазы (содержат пиридоксальфосфат), пероксидаза (содержит гем).
Кофактор:
· входит в состав активного центра,
· участвует в связывании субстрата или в его превращении.
Ферменты могут быть мономерами (состоят из одной субъединицы) и полимерами (из нескольких субъединиц).
Структурно-функциональная организация ферментов
1. Активный центр – комбинация аминокислотных остатков (обычно 12-16), обеспечивающая непосредственное связывание с молекулой субстрата и осуществляющая катализ.
В активном центре выделяют два участка:
· якорный (контактный, связывающий) – отвечает за связывание и ориентацию субстрата в активном центре,
· каталитический – непосредственно отвечает за осуществление реакции.
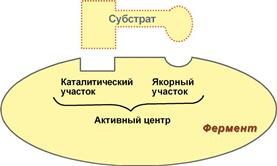
Схема строения ферментов
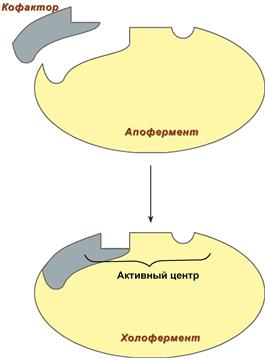
Схема формирования сложного фермента
2. Аллостерический центр (allos – чужой) – центр регуляции активности фермента, который пространственно отделен от активного центра и имеется не у всех ферментов. Связывание с аллостерическим центром какой-либо молекулы (называемой активатором или ингибитором, а также эффектором, модулятором, регулятором) вызывает изменение конфигурации белка-фермента и, как следствие, скорости ферментативной реакции.
Аллостерические ферменты являются полимерными белками, активный и регуляторный центры находятся в разных субъединицах.
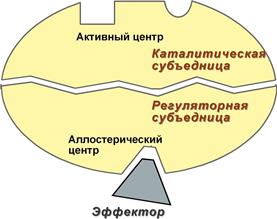
Схема строения аллостерического фермента
Изоферменты
Изоферменты – это молекулярные формы одного и того же фермента, возникшие в результате небольших генетических различий в первичной структуре фермента. Различные изоферменты определяют скорость и направление реакции благодаря разному сродству к субстрату.
Например, димерный фермент креатинкиназа (КК): M (англ. muscle – мышца) и B (англ. brain – мозг).
Креатинкиназа-1 (КК-1) состоит из субъединиц типа B и локализуется в головном мозге,
креатинкиназа-2 (КК-2) – по одной М- и В-субъединице, активна в миокарде,
креатинкиназа-3 (КК-3) содержит две М-субъединицы, специфична для скелетной мышцы.
 Изоферменты креатинкиназы
Изоферменты креатинкиназы
|  Изоферменты лактатдегидрогеназы
Изоферменты лактатдегидрогеназы
|
Пять изоферментов лактатдегидрогеназы: Н (англ. heart – сердце) и М (англ. muscle – мышца).
Лактатдегидрогеназы типов 1 (Н4) и 2 (H3M1) присутствуют в тканях с аэробным обменом (миокард, мозг, корковый слой почек), обладают высоким сродством к молочной кислоте (лактату) и превращают его в пируват.
ЛДГ-4 (H1M3) и ЛДГ-5 (М4) находятся в тканях, склонных к анаэробному обмену (печень, скелетные мышцы, кожа, мозговой слой почек), обладают низким сродством к лактату и катализируют превращение пирувата в лактат.
ЛДГ-3 (H2M2) – в тканях с промежуточным типом обмена (селезенка, поджелудочная железа, надпочечники, лимфатические узлы).






