Пусть молекула вещества А реагирует с молекулой вещества В с образованием продукта реакции АВ в газовой смеси.
А+В=АВ
Для получения АВ из А и В необходимо, чтобы молекулы А и В прореагировали, т.е. столкнулись между собой. Без соударения вещества А В не получится.
Скорость химической реакции прямо пропорциональна произведению концентрации реагирующих веществ, возведенных в степень их стехиометрических коэффициентов – это закон действующих масс.
Математический закон выражается так:
аА+вВ=сС
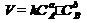
 – коэффициент пропорциональности, константа скорости реакции. Коэффициент
– коэффициент пропорциональности, константа скорости реакции. Коэффициент  численно равен скорости реакции при концентрации каждого из реагирующих веществ равной 1моль/л, или когда произведение концентраций равно единице.
численно равен скорости реакции при концентрации каждого из реагирующих веществ равной 1моль/л, или когда произведение концентраций равно единице.
а и в – стехиометрические коэффициенты.
В случае гетерогенных реакций в уравнение закона действующих масс входят концентрации только жидких и газообразных веществ. Концентрация твердого вещества величина постоянная, поэтому не входит в константу скорости К.
Например, для реакции горения угля:
С(тв.)+О2=СО2(газ)

3. Влияние температуры на скорость реакции.
Зависимость скорости реакции от температуры выражается правилом Вант - Гоффа: при увеличении температуры на каждые 10°С скорости реакции возрастает в 2-4 раза.

Где  и
и  - скорости при температуре Т1 и Т2. γ - температурный коэффициент.
- скорости при температуре Т1 и Т2. γ - температурный коэффициент.
Примеры решения задач.
Пример 1: Как изменится скорость реакции протекающей в закрытом сосуде, если увеличить давление в 4 раза?
2NO(г.)+О2(г.)=2NO2
Решение:
увеличить давление в 4 раза означает увеличить и концентрацию газов во столько же раз.
1. Определяем скорость реакции до повышения давления.
V1 =K*C2NO*CO2
2. Определяем скорость реакции после повышения давления.
V2=K*(4CNO)2*(4CO2)=64K*C2NO*CO2
3. Определяем, во сколько раз возросла скорость реакции
V1/V2=64*K*C2NO*CO2 / K*C2NO*CO2
Ответ: скорость реакции возросла в 64 раза.
Пример 2: Во сколько раз возрастёт скорость реакции при повышении температуры с 20 С˚ до 50 С˚? Температурный коэффициент равен 3.
Решение:
По правилу Вант – Гоффа:

По условию требуется определить  . Подставим данные в формулу:
. Подставим данные в формулу:

Ответ: скорость реакции возросла в 27 раз.
ОБЪЕКТ ИССЛЕДОВАНИЯ.
Зависимость скорости химической реакции от концентрации реагирующих веществ должна быть показана на основании измерения времени от момента сливания растворов до начала реакции, определяемой по помутнению раствора, обусловленному выделением свободной серы.
КОНТРОЛЬНЫЕ ВОПРОСЫ.
1.Что называется скоростью химической реакции?
2. Какова зависимость скорости реакции от концентрации реагирующих веществ?
3. Как называется величина К? Каков её физический смысл?
4. Зависит ли коэффициент К от изменения температуры?
5. Как влияет температура на скорость химической реакции?
6. Как влияет давление на скорость химической реакции между газообразными веществами?






