Электронное строение металлов определяет такие их общие физические свойства, как блеск, ковкость, пластичность, высокие тепло- и электропроводность. Практически все металлы, кроме ртути, при комнатной температуре – твердые вещества. Большинство из них кристаллизуется в одной из трех форм кристаллических решеток:
а) кубическая гранецентрированная (Al, Cu, Ag);
б) кубическая объемноцентрированная (Na, K, Ba);
в) гексагональная (Mg, Zn, Cd).

Рис. 2. Кристаллические решетки металлов: а – кубическая гранецентрированная; б – кубическая объемноцентрированная; в - гексагональная
Металлы обладают полиморфизмом – способностью в определенных условиях кристаллизоваться в разных формах.
При температуре затвердевания расплавленного кристалла кристаллизация начинается одновременно во многих точках – центрах кристаллизации. Обычно кристаллы металлов имеют неправильную форму за счет сросшихся мелких кристаллов, то есть образуют кристаллиты. В особых случаях при температуре затвердевания расплавленного металла можно получить монокристалл (кристаллизация идет из одной точки).
Сплавы
В жидком состоянии большинство металлов растворяются друг в друге, образуя однородные расплавы. При охлаждении расплавов происходит кристаллизация, в процессе которой получаются сплавы. Металлы и сплавы широко используются как конструкционные и электротехнические материалы. Сплавы улучшают свойства металлов, придавая им новые свойства (жаропрочность, коррозионную устойчивость, механическую прочность и др.).
Изучение природы сплавов, их особенностей и свойств, а также свойств чистых металлом – область науки, называемой металловодением. В основе металловедения лежит физико-химический анализ – установление зависимости между изучаемым свойством и составом системы. Результаты исследования выражаются графически в виде диаграммы состав – свойство. Изучаемыми свойствами могут быть температура плавления или кристаллизации (термический анализ), электропроводность, плотность и др.
При проведении термического анализа диаграмма состав – свойство строится в координатах температура плавления (затвердевания) – процентный состав компонентов и называется диаграммой плавкости. Диаграммы плавкости строят с помощью кривых охлаждения.
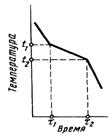
Кривая охлаждения чистого вещества приведена на рис. 3а. Горизонтальный участок соответствует температуре плавления или затвердевания. Как только исчезает жидкая фаза, охлаждение продолжается с обычной скоростью. Кривая охлаждения смеси веществ (рис. 3б) не имеет горизонтального участка и изменяет наклон в двух точках (начало и конец кристаллизации).

|
|
| а | б |
Рис. 3. Кривые охлаждения: а- чистого вещества; б – смеси веществ
По характеру взаимодействия компонентов различают три основных вида твердых сплавов: 1) твердый раствор одного компонента в другом; 2) механическая смесь, состоящая из кристаллов одного и другого компонентов; 3) химическое соединение одного компонента с другим. Диаграммы плавкости различных видов сплавов приведены на рис. 4.

|

|
|
| а | б | в |
Рис. 4. Диаграммы плавкости сплавов: а) твердый раствор одного компонента в другом; б) механическая смесь, состоящая из кристаллов одного и другого компонентов; в) химическое соединение одного компонента с другим.
Верхние кривые на диаграммах плавкости (ликвидус) показывает температуры, при которой из жидкой фазы начинают выделяться кристаллы. Выше этой кривой лежит область расплава. Нижняя кривая (солидус) показывает температуры конца затвердевания. Под ней на диаграмме лежит область твердой фазы. Между кривыми ликвидуса и солидуса находится область, отвечающая сосуществованию жидкой и твердой фаз.
Диаграмма плавкости, представленная на рис. 4а, соответствует неограниченной растворимости одного металла в другом как в жидкой, так и в твердой фазе. Образованию таких сплавов способствует близость химических свойств металлов, их атомных радиусов и типа кристаллической структуры (например, Cu – Au).
Диаграмма плавкости сплава, являющегося механической смесью компонентов (рис. 4б), имеет пять областей. Область I, отвечает однородной жидкой фазе (расплаву компонентов А + В). Области, отвечающие двухфазным состояниям системы: II – твердая фаза компонента А + жидкая фаза расплава А + В; III – твердая фаза компонента В + жидкая фаза расплава А + В; IV – твердая фаза компонента А, вкрапленная в сплав эвтектического состава; V – твердая фаза компонента В, вкрапленная в сплав эвтектического состава.
Однородный сплав А + В можно рассматривать как ненасыщенный раствор (А в В или В в А). При охлаждении начинается постепенное выделение из раствора одного из компонентов, растворимость которого достигает насыщения. При этом жидкая фаза обогащается другим компонентом в соответствии с кривой ликвидуса (движение по стрелкам) до тех пор, пока состав расплава и температура кристаллизации не достигнут минимума. Расплав такого состава (эвтектический состав) насыщен одновременно по двум компонентам и поэтому затвердевает полностью. Температура плавления эвтектической смеси обычно ниже температуры плавления ее отдельных компонентов. К числу сплавов, образующих эвтектику, относятся сплавы Bi – Cd, Pb – Sb, Sn – Pb. Например, температура плавления чистой сурьмы равна 630°С, а температура плавления свинца равна 327°С, в то время, как эвтектическая смесь, содержащая 13% сурьмы и 87% свинца, плавится при температуре 246°С и используется как легкоплавкий припой. Сплавы типа эвтектических образуют металлы, близкие по природе, но имеющие разные формы кристаллических решеток.
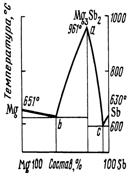
Металлы, имеющие чаще всего несходную химическую природу и заметно отличающиеся по электроотрицательности, образуют сплавы, относящиеся к химическим соединениям (интерметаллидам). Диаграммы состояния сплавов такого типа можно представить как наложение двух диаграмм сплавов эвтектического типа. Максимум на кривой ликвидуса соответствует составу химического соединения. Состав интерметаллида определяется валентными состояниями металлов (K4Pb), взаимными размерами атомов (MgCu2) или числом электронов в зоне проводимости (Cu5Zn8).
Химические свойства металлов
Валентные электроны металлов слабо связаны с ядром, поэтому металлы являются типичными восстановителями (легко отдают электроны, превращаясь в положительно заряженные ионы). По активности металлы располагаются в ряд, называемый электрохимическимрядом напряжений или рядом активностей металлов. Металлы, стоящие в ряду активностей до водорода, имеют отрицательные значения стандартных электродных потенциалов (j0), а металлы, стоящие после водорода - положительные значения j0. Чем левее стоит металл, тем больше его активность.
Металлы реагируют с кислородом воздуха с образованием оксидов, а щелочные и щелочноземельные металлы - пероксидов и супероксидов: 4Li + O2  2Li2O (оксид лития)
2Li2O (оксид лития)
2Na + O2  Na2O2 (пероксид натрия)
Na2O2 (пероксид натрия)
К + О2  КО2 (супероксид калия)
КО2 (супероксид калия)
Металлы реагируют с неметаллами: 2Al +3S  Al2S3.
Al2S3.
Активные металлы способны вытеснять водород из воды:
2Na + 2H2O  2NaOH + H2
2NaOH + H2 
Более активные металлы вытесняют менее активные из оксидов и солей: Cr2O3 + 2Al  Al2O3 + 2Cr
Al2O3 + 2Cr
CuSO4 + Fe  FeSO4 + Cu
FeSO4 + Cu
Реакции металлов с кислотами:
1. Кислоты-неокислители (все кислоты, кроме H2SO4 конц. и HNO3 любой концентрации) реагируют только с металлами, стоящими в ряду напряжений до водорода. В результате реакции образуется соль и выделяется водород: 2Al+6HCl  2AlCl3+3H2
2AlCl3+3H2 
2. Кислоты-окислители (H2SO4 конц., HNO3 конц., HNO3 разб.) реагируют со всеми металлами, кроме Au и Pt. В результате образуются соль, вода и продукт восстановления кислоты, который зависит от концентрации кислоты и активности металла:
Например, Cu + 2H2SO4 конц.  CuSO4 + 2H2O + SO2
CuSO4 + 2H2O + SO2 
Cu + 4HNO3 конц.  Cu(NO3)2 + 2H2O + 2NO2
Cu(NO3)2 + 2H2O + 2NO2 
3Cu + 8HNO3 разб.  3Cu(NO3)2 + 4H2O + 2NO
3Cu(NO3)2 + 4H2O + 2NO 
Металлы, стоящие в ряду напряжений до алюминия, восстанавливают очень разбавленную азотную кислоту до NH4NO3: Сa+10HNO3оч.разб.  4Ca(NO3)2 +3H2O+NH4NO3
4Ca(NO3)2 +3H2O+NH4NO3
Коэффициенты в вышеуказанных реакциях расставляются по правилам окислительно-восстановительных реакций.
Концентрированные серная и азотная кислоты пассивируют такие металлы, как железо, алюминий, хром и некоторые другие, покрывая их прочной оксидной пленкой, которая препятствует дальнейшему окислению.
Электрохимические процессы
Процессы взаимного превращения химической и электрической форм энергии называют электрохимическими процессами. Электрохимические процессы можно разделить на две основные группы: 1) процессы превращения химической энергии в электрическую (в гальванических элементах и химических источников тока); 2) процессы превращения электрической энергии в химическую (электролиз).
Электрохимическая система состоит из двух электродов и ионного проводника между ними. Электроды замыкаются металлическим проводником (проводником 1-го рода). Ионным проводником (проводником 2-го рода) служат растворы или расплавы электролитов, а также твердые электролиты.
Электродные потенциалы
Если металл погрузить в раствор собственной соли, то возможны два процесса:
1) достройка кристаллической решетки металла за счет осаждения ионов из раствора (поверхность металла заряжается положительно);
2) переход ионов металла в раствор за счет взаимодействия с молекулами воды (поверхность металла заряжается отрицательно).
Заряженная поверхность притягивает ионы противоположного знака из раствора. В результате между металлам и раствором возникает разность потенциалов, а на границе – двойной электрический слой.
M  Mn+ + ne-
Mn+ + ne-
Равновесие имеет динамический характер, процессы идут с одинаковой скоростью в прямом и обратном направлениях. Потенциал, устанавливающийся в условиях равновесия электродной реакции, называется равновесным электродным потенциалом. Абсолютные значения электродных потенциалов экспериментально определить невозможно, однако можно определить разность потенциалов. Поэтому для характеристики электродных процессов пользуются относительными значениями электродных потенциалов. За нулевой потенциал принимают потенциал стандартного водородного электрода.
Стандартный водородный электрод состоит из платиновой пластинки, погруженной в раствор серной кислоты с концентрацией ионов водорода, равной 1 моль/л. через этот раствор при давлении 101325 Па и температуре 298 К пропускают газообразный водород, который адсорбируется платиной и взаимодействует с раствором:
2H+ + 2e-  H2; j° (2H+/H2) = 0 В
H2; j° (2H+/H2) = 0 В
для определения потенциала металлического электрода собирают гальванический элемент, который состоит из стандартного водородного и металлического электродов:
H2, Pt ½ H2SO4 ½½ Mn+ ½M
Если концентрация ионов металла в растворе электролита равна 1 моль/л, то потенциал такого электрода называется стандартным электродным потенциалом, j ° (М n + / M). Они количественно характеризуют восстановительную способность атомов металлов и окислительную способность ионов металлов. Чем более отрицательное значение имеет стандартный электродный потенциал металла, тем более сильным восстановителем является металл. Наоборот, чем более положительное значение потенциала, тем большими окислительными способностями обладает ион металла.
Если концентрация иона металла в электролите не равна 1 моль/л, то потенциал такого электрода рассчитывается по уравнению Нернста:
j(Мn+/M) =j°(Мn+/M) + 
если соединить два металлических электрода, то получим систему, называемую гальваническим элементом. При его работе электроны будут перетекать от более отрицательного к более положительному электроду, возникает электрический ток. При этом более отрицательный электрод (анод) будет растворятся, а ионы электролита более положительного электрода (катода) – осаждаться из раствора на поверхность металла.
Zn½1M ZnSO4 ½½ 1M CuSO4 ½Cu
j° (Zn2+/Zn) = -0,76 В (Zn – анод)
j° (Сu2+/Cu) = +0,34 В (Cu – катод)
Электродные процессы: Zn – 2e- ® Zn2+
Cu2++ 2e- ® Cu
 |
Zn + Cu2+ ® Zn2+ + Cu
Электродвижущая сила гальванического элемента, ЭДС (Е) – это работа, которую может совершить гальванический элемент. Она определяется как разность потенциалов:
Е = j(катода) – j(анода)
КОРРОЗИЯ МЕТАЛЛОВ
Процесс разрушения веществ под действием окружающей среды называется коррозией. При этом металл окисляется, образуя продукты коррозии, состав которых зависит от условий протекания процесса.
Коррозия – самопроизвольный процесс, ей подвергаются практически все металлы, кроме золота и платины. Это – экзотермический процесс, энергия выделяется в виде тепла.
Ежегодно 10% производимого в мире металла безвозвратно теряется в результате коррозии.
По механизму протекания коррозия делится на химическую и электрохимическую.
Химическая коррозия – это разрушение металлов в агрессивных токонепроводящих средах. Она проявляется в виде прямого гетерогенного (межфазного) взаимодействия металла с окислителем окружающей среды. Химическая коррозия бывает:
а) газовая – коррозия в газах и парах без конденсации влаги на поверхности металла,
4 Fe + 3 O2 ® 2 Fe2O3
б) коррозия в неэлектролитах – агрессивных органических жидкостях. Например, коррозия в сернистой нефти:
Fe + S ® FeS
Электрохимическая коррозия характерна для сред с ионной проводимостью. При контакте двух металлов во влажном воздухе возникают микрогальванические пары, приводящие к анодному растворению металла и катодному восстановлению окислителя. Электрохимическая коррозия бывает электролитной, атмосферной, почвенной. Чаще всего электрохимической коррозии подвергаются металлические контакты, сплавы металлов, а также металлы низкой степени чистоты, содержащие металлические или неметаллические примеси.
В процессе электрохимической коррозии более активный металл, имеющий более отрицательное значение стандартного электродного потенциала, отдает электроны и переходит в раствор (служит анодом). Электроны от него перемещаются к менее активному металлу или неметаллической примеси (катоду) и участвуют в восстановительных процессах ионов и молекул, находящихся в окружающей микрогальваническую пару среде.
В кислых растворах идет процесс водородной деполяризации: 2Н+ + 2е  Н2
Н2 
Электрохимический потенциал этой системы определяется величиной рН раствора и парциальным давлением водорода:
j1 = – 0,059 рН – 0,0295 lg(р Н2)
В нейтральных и щелочных средах идет процесс с участием растворенного кислорода воздуха - кислородная деполяризация: О2 + 2Н2О + 4е  4ОН
4ОН 
В этом случае электрохимический потенциал определяется величиной рН раствора и парциальным давлением кислорода:
j2 = 1,23 + 0,01471 lg(р О2) – 0,059 рН
 Пример Коррозия контакта Cu / Zn, среда - КОН.
Пример Коррозия контакта Cu / Zn, среда - КОН.
Zn: Zn - 2e  Zn2+
Zn2+  2
2
Cu: О2 + 2Н2О + 4е  4ОН
4ОН 
 1
1
 Zn + O2 + 2H2O
Zn + O2 + 2H2O  2Zn(OH)2
2Zn(OH)2
Следует отметить, что коррозия по вышеуказанному механизму возможна только при условии, что потенциал окислителя больше потенциала металла (jок > jМ).
Если j1 < jM < j2, то коррозия возможна в щелочной среде и не возможна в кислой. Если jM < j1, то коррозия возможна в любой среде.
Защита от коррозии
Методы защиты от коррозии условно делятся на следующие группы: а) легирование металлов; б) защитные покрытия (металлические и неметаллические); в) электро-химическая защита; г) изменение свойств коррозионной среды; д) рациональное конструирование изделий.
Легирование металлов – это введение в состав сплава компонентов, вызывающих пассивацию металлов. В качестве таких компонентов применяют хром, никель, вольфрам и др.
Защитные покрытия – это слои, искусственно создаваемые на поверхности металлических изделий для предохранения их от коррозии. Защитные покрытия бывают как органические (лаки, краски), так и неорганические (покрытие металлов слоем оксида – оксидирование или воронение – или фосфата – фосфатирования).
Наиболее распространены металлические покрытия, материалами для которых могут быть как чистые металлы (Zn, Al, Cu, Ni, Cr, Ag, Au и др.), так и их сплавы (бронза, латунь и др.). по характеру поведения металлических покрытий при коррозии их можно разделить на катодные и анодные.
К катодным покрытиям относятся покрытия, потенциалы которых в данной среде имеют более положительные значения, чем потенциал основного металла (покрытие менее активным металлом). Примерами катодных покрытий могут служить золочение, серебрение металлов, никелирование и лужение (покрытие оловом) стали. Катодные покрытия сами по себе корродируют медленнее, чем металл изделия, однако при повреждении покрытия возникает микрогальванический элемент, в котором основной материал служит анодом и растворяется, а металл покрытия – катодом, на котором выделяется водород или поглощается кислород. Таким образом, катодные покрытия могут защищать металл только при отсутствии повреждений покрытия.
Анодное покрытие – это покрытие металла слоем более активного металла (металлом с более отрицательным потенциалом), например, оцинкованное железо. Более активный металл сам по себе подвергается коррозии, поэтому анодное покрытие менее долговечно. Однако при нарушении целостности покрытия основной металл будет катодом микрогальванического элемента, поэтому коррозия основного металла не происходит до тех пор, пока не растворится покрытие.
Потенциалы металлов зависят от состава растворов, поэтому при изменении условий может изменять характер покрытия. Например, покрытие стали оловом в растворах сильных минеральных кислот – катодное, а в растворах органических кислот – анодное.
Электрохимическая защита металлов от коррозии основана на торможении анодных или катодных реакций коррозионного процесса. Она включает в себя катодную и протекторную защиту. Катодная поляризация осуществляется за счет извне приложенного тока (подключение изделия к отрицательно заряженному электроду). Отрицательный заряд, подаваемый на изделие, препятствует выходу положительно заряженных ионов металла в окружающую среду при коррозионном растворении. Недостатком данного метода защиты является то, что она может применяться только к изделиям, не контактирующими с людьми (шлюзовые ворота, морские трубопроводы, оборудование химических производств).
Защита от коррозии подземных трубопроводов и кабелей осуществляется присоединением к защищаемой конструкции более активного металла (протекторная защита), который служит анодом, то есть разрушается в процессе коррозии, предохраняя при этом изделие.
Разработана также защита металла от коррозии наложением анодной поляризации. Этот метод применим лишь к металлам и сплавам, способным легко пассивироваться при смещении потенциала в положительную сторону (например, предотвращение коррозии нержавеющих сталей в серной кислоте).
Изменение свойств коррозионной среды. Для снижения агрессивности среды уменьшают концентрацию компонентов, опасных в коррозионном отношении (например, деаэрация, то есть удаление кислорода, снижение концентрации ионов водорода и др.). Для защиты от коррозии широко применяют ингибиторы.
Ингибиторы – это вещества, которые уменьшают скорость коррозии металла. По составу различают ингибиторы органические и неорганические. По условиям, в которых они применяются, их можно разделить на ингибиторы для растворов и летучие ингибиторы, которые защищают металлы в условиях атмосферной коррозии.
Механизм действия ингибиторов заключается в их адсорбции на поверхности изделия и торможении катодных или анодных процессов. К анодным ингибиторам можно отнести ингибиторы окисляющего действия (NaNO2, Na2Cr2O7 и др.). К катодным ингибиторам относятся относятся органические вещества, содержащие азот, серу и кислород, например, диэтиламин, уротропин, формальдегид и др. В качестве летучих ингибиторов обычно используются амины с небольшой молярной массой, в которые вводятся группы NO2 или COO-.
ПРОГРАММА






