Начавшим изучение химии в 8 классе
Учебник: Ходаков Ю.В. и др. Неорганическая химия: учеб. для 7–8 кл. сред. шк. / Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глориозов. – 18-е изд. – Москва: Просвещение, 1987. – 240 с.
Также можно воспользоваться аналогичными учебниками 1985 и 1986 гг.
Самостоятельно разобрать материал §§ 1 – 19 (стр. 1 – 38),
§§ 52 – 54 (стр. 124 – 127).
Знать:
· определение химии
· определения понятий «физическое тело», «вещество», понимать разницу между этими понятиями;
· определения понятий «свойство», «физические свойства», «химические свойства», основные физические свойства веществ;
· определения понятий «чистое вещество», «смесь», «однородная смесь», «неоднородная смесь», понимать разницу между этими понятиями;
· основные способы разделения смесей;
· определения понятий «физические явления» и «химические явления», понимать разницу между этими понятиями;
· определения понятий «молекула», «атом», понимать разницу между этими понятиями;
· основные положения атомно-молекулярного учения;
· определения понятий «простое вещество», «сложное вещество», понимать разницу между этими понятиями;
· определения понятий «химический элемент», «относительная атомная масса химического элемента»;
· начертание и произношение знаков 30 химических элементов (см. таблицу далее);
· определения понятий «химическая формула», «индекс», «коэффициент»;
· структуру Периодической системы химических элементов Д.И. Менделеева;
· закон постоянства состава веществ;
· определение понятия «относительная молекулярная масса»;
· определения понятия «валентность»;
· закон сохранения массы веществ;
· определение понятия «химическое уравнение»;
· типы химических реакций;
· определения понятий «количество вещества», «моль», «молярная масса».
Уметь:
· характеризовать физические свойства веществ;
· определять, имеет вещество молекулярное или немолекулярное строение, исходя из его температуры плавления;
· находить относительную атомную массу химического элемента;
· характеризовать положение химического элемента в Периодической системе химических элементов Д.И. Менделеева;
· находить относительную молекулярную массу химического соединения;
· находить массовую долю элемента в химическом соединении;
· выводить формулу химического соединения по массовым долям входящих в его состав элементов;
· находить валентность элементов по формуле химического соединения;
· составлять формулу химического соединения по валентности входящих в его состав элементов;
· составлять уравнения химических реакций;
· находить количество вещества по известной массе;
· находить массу по известному количеству вещества;
· по химическому уравнению находить массу или количество вещества одного из реагентов или продуктов реакции по известной массе или количеству вещества другого реагента или продукта реакции.
Некоторые справочные материалы
(в дополнение к материалу учебника)
| Название химического элемента | Химический знак | Произношение химического знака |
| Азот | N | Эн |
| Алюминий | Al | Алюминий |
| Барий | Ba | Барий |
| Бор | B | Бор |
| Бром | Br | Бром |
| Водород | H | Аш |
| Железо | Fe | Феррум |
| Золото | Au | Аурум |
| Иод | I | Иод |
| Калий | K | Калий |
| Кальций | Ca | Кальций |
| Кислород | O | О |
| Кремний | Si | Силициум |
| Магний | Mg | Магний |
| Марганец | Mn | Марганец |
| Медь | Cu | Купрум |
| Натрий | Na | Натрий |
| Ртуть | Hg | Гидраргирум |
| Свинец | Pb | Плюмбум |
| Сера | S | Эс |
| Серебро | Ag | Аргентум |
| Углерод | C | Це |
| Фосфор | P | Пэ |
| Фтор | F | Фтор |
| Хлор | Cl | Хлор |
| Цинк | Zn | Цинк |
| Литий | Li | Литий |
| Бериллий | Be | Бериллий |
| Мышьяк | As | Арсеникум |
| Олово | Sn | Станнум |
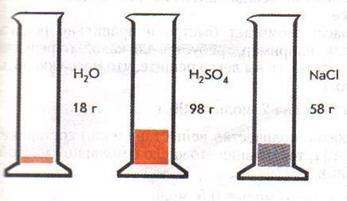
Атомная единица массы (а. е. м.) – 1/12 массы атома углерода
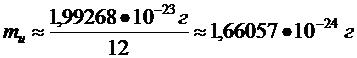 Величина а. е. м. в граммах:
Величина а. е. м. в граммах:
Массы атомов в граммах:
m(H)≈1,67375∙10-24 г
m(O)≈2,656812∙10-23 г
Массы атомов в а. е. м.:
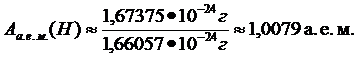 | ||
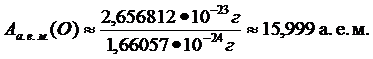 | ||
Полученные величины можно рассматривать в качестве безразмерных относительных атомных масс.
Относительная атомная масса элемента Ar показывает, во сколько раз масса его атома больше 1/12 массы атома углерода.
Индекс r – от англ. relative – относительный.
Относительную атомную массу округляют до целого числа,
исключение – Ar(Cl)=35,5.
Относительная молекулярная масса вещества Mr показывает, во сколько раз масса его молекулы больше 1/12 массы атома углерода.
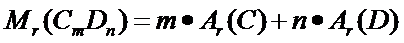 Пусть дано вещество CmDn, тогда
Пусть дано вещество CmDn, тогда
Массовая доля элемента в химическом соединении рассчитывается по формуле:
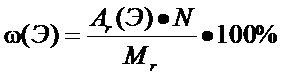 |
,
где N – число атомов элемента в соединении.


Алгоритм определения валентности элемента по формуле соединения
1. Пишут химическую формулу вещества и отмечают валентность известного элемента.
2. Находят и записывают общее число единиц валентности известного элемента (наименьшее общее кратное).
3. Вычисляют и проставляют над химическими знаками валентность другого элемента. Для этого общее число единиц валентности делят на индекс элемента.
Алгоритм составления химических формул по валентности
1. Пишут рядом химические знаки элементов, которые входят в состав соединения.
2. Над знаками элементов проставляют их валентность.
3. Определяют наименьшее общее кратное чисел, выражающих валентность обоих элементов.
4. Делением НОК на валентность соответствующего элемента находят индексы (индекс «1» не пишут).

Алгоритм составления уравнений химических реакций
1. В левой части уравнений пишут формулы веществ, вступающих в реакцию, затем ставят стрелку. Помнить: молекулы многих газообразных простых веществ состоят из двух атомов (H2, O2, N2, Cl2 и т.д.).
2. В правой части (после стрелки) пишут формулы веществ, образующихся в результате реакции. Таким образом получают схему химической реакции.
3. Уравнение реакции составляют на основе закона сохранения массы веществ, т.е. слева и справа должно быть одинаковое число атомов. Это достигается расстановкой коэффициентов перед формулами веществ.
Вначале уравнивают число атомов, которых в реагирующих веществах содержится больше всего, затем уравнивают число атомов остальных химических элементов.
В получившемся уравнении химической реакции вместо знака «→» можно использовать знак «=».
Если для начала реакции требуется нагревание, над стрелкой ставят знак «t°».
Если в результате реакции выделяется газ, рядом с его формулой ставят знак «↑», осадок – знак «↓».

Реакции соединения:
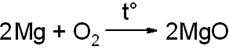
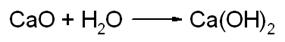
Реакции разложения:
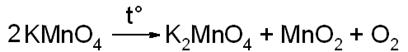
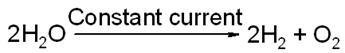
Реакции замещения:


Реакции обмена:
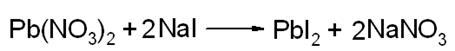
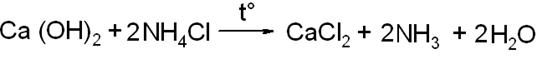
Количество вещества (n или ν) – это порция вещества, содержащая определенное число частиц (атомов, молекул).
n =[моль]
Моль – это количество вещества, содержащее столько же частиц (атомов, молекул), сколько содержится атомов углерода в 12 г углерода.
Моль был введен в систему СИ в качестве основной единицы количества вещества решением 14-й Генеральной конференции по мерам и весам (1971)
Слово «моль» склоняется, если стоит после числительного, но не склоняется, если стоит после числа.
Пример: «получили два моля воды»; «в 2 моль воды».
Было установлено, что 12 г углерода содержат 6,02∙1023 атомов. Следовательно, любое вещество количеством 1 моль содержит 6,02∙1023 частиц.
 Число 6,02∙1023 названо числом Авогадро
Число 6,02∙1023 названо числом Авогадро
,
где N – число частиц, n – количество вещества.
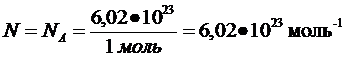 |
При n=1 моль .
Число NA=6,02∙1023 моль-1 называют постоянной Авогадро.
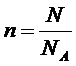 |
Молярная масса вещества (M) – масса одного моля вещества.
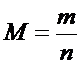 |
M=[ г/моль ]