1. Изобарный процесс (p = const). При изобарном процессе работа газа при увеличении объема от V 1 до V 2 равна:
 ,
,
а первое начало термодинамики для изобарного процесса примет вид:
 .
.
2. Изохорный процесс (V = const). При изохорном процессе газ не совершает работы против внешних сил, то есть А= 0, а первое начало термодинамики для изохорного процесса примет вид:
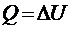 .
.
т. е. все количество теплоты, сообщаемое газу, расходуется на увеличение его внутренней энергии.
3. Изотермический процесс (T = const). Работа при изотермическом расширении газа:
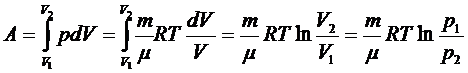 .
.
Так как при постоянной температуре внутренняя энергия идеального газа не изменяется, то первое начало термодинамики для изотермического процесса:
 ,
,
то есть все количество теплоты Q, сообщаемое газу, расходуется на совершение им работы A против внешних сил.
Тема 17. Теплоемкость газа при изопроцессах. Уравнение Майера.
Теплоемкостью тела называется величина, равная количеству теплоты, которое нужно сообщить телу, чтобы повысить его температуру на 1 К.
Удельная теплоемкость вещества – величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К:
 .
.
Молярная теплоемкость вещества – величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К:
 , откуда
, откуда  .
.
Различают теплоемкости газа при изохорном и изобарном процессах.
1. Молярная теплоемкость газа при изохорном процессе  .
.
Для изохорного процесса первое начало термодинамики можно записать в следующем виде:
 .
.
Так как  , то для изохорного процесса:
, то для изохорного процесса:
 ,
,
откуда  ,
,
где i –число степеней свободы молекулы.
2. Молярная теплоемкость газа при изобарном процессе  .
.
Для изобарного процесса первое начало термодинамики можно записать в следующем виде:
 .
.
Так как для изобарного процесса  ,
,
то  ,
,
откуда  .
.
Уравнение Майера.
Сравнение между собой Ср и С V приводит к уравнению Майера:
 .
.
Это уравнение показывает, что Ср больше, чем С V на величину универсальной газовой постоянной R. Это объясняется тем, что при изобарном нагревании газа, в отличие от изохорного нагревания, требуется дополнительное количество теплоты на совершение работы расширения газа.
Таким образом, молярная теплоемкость газа определяется лишь числом степеней свободы и не зависит от температуры. Это утверждение справедливо в довольно широком интервале температур лишь для одноатомных газов.Уже у двухатомных газов число степеней свободы, проявляющееся в теплоемкости, зависит от температуры.






