ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Раствор- это однородная система, состоящая из растворителя,растворенных веществ и продуктов их взаимодействия. Растворителем чаще всего является то вещество, которое в чистом виде имеет тоже агрегатное состояние, что и раствор, либо присутствует в избытке.
Растворителем является то вещество, которое в чистом виде имеет то же агрегатное состояние, что и раствор, находится визбытке.
По агрегатному состоянию различают растворы: жидкие, твердые, газообразные. По соотношению растворителя и растворенного вещества все растворы делятся на:
¾ Ненасыщенный раствор — раствор, в котором концентрация растворенного вещества меньше, чем в насыщенном растворе, и в котором при данных условиях можно растворить ещё некоторое его количество.
¾ Насыщенный раствор — раствор, в котором растворённое вещество при данных условиях достигло максимальной концентрации и больше не растворяется. Осадок данного вещества находится в равновесном состоянии с веществом в растворе.
¾ Пересыщенный раствор — раствор, содержащий при данных условиях больше растворённого вещества, чем в насыщенном растворе, избыток вещества легко выпадает в осадок. Обычно пересыщенный раствор получают охлаждением раствора, насыщенного при более высокой температуре (пересыщение).
Состав раствора обычно передается содержанием в нем растворимого вещества в виде массовой доли, процентной концентраций и молярности.
· Массовая доля ( безразмерная величина) – это отношение массы растворенного
вещества к массе всего раствора:
W м.д. = mраст. вещества
m раствора.
· Процентная концентрация (%) – это величина показывающая сколько грамм растворенного вещества cсодержится в 100 гр. раствора :
W % = mраст. вещества 100%
m раствора
· Молярная концентрация, или молярность (моль/литр)- это величина показывающая сколько молей растворимого вещества содержатся в 1 литре раствора:
См = mраст. вещес
М r (раст. вещества ) V раствора .
ПРАКТИЧЕСКАЯ ЧАСТЬ
| Ход работы, задание | Решение, расчеты | |
| Опыт №1 ПРИГОТОВЛЕНИЕ РАСТВОРА ПОВАРЕННОЙ СОЛИ | ||
| Задание: Определить процентную и молярную концентрацию раствора массой 20 гр., содержащего 3гр. соли NaCL, плотность которого 1,2 гр/л | Дано: | Решение: ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
|
| Найти: | ||
| Опыт №2 ПРИГОТОВЛЕНИЕ САХАРНОГО РАСТВОРА РАЗБАВЛЕНИЕМ | ||
| Задание: Определить массу воды и растворённого в ней сахара, если масса раствора 150гр., а процентная концентрация сахара в растворе равна 40%. Как изменится концентрация раствора если к нему прилить 30гр. воды | Дано: ............................................................................................................................................................ Найти .................................................... | Решение: ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… |
| Опыт №3 ПРИГОТОВЛЕНИЕ САХАРНОГО РАСТВОРА С БОЛЬШЕЙ КОНЦЕНТРАЦИЕЙ | ||
| Определить массу раствора сахара в воде, если масса сахара в нём 15гр., а процентная концентрация 45%. Как изменится концентрация раствора,если к нему добавить 5гр.сахара | Дано: ............................................................................................................................................................ Найти .................................................... | Решение: ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… |
| Опыт №4 ПРИГОТОВЛЕНИЕ РАСТВОРА УКСУСНОЙ КИСЛОТЫ ИЗ 2-Х РАСТВОРОВ | ||
| Смешали 40 гр. 9%-ного раствора уксуса и 20гр. 70%-ного раствора уксусной эсенцинции. Определить концентрацию полученного раствора уксусной кислоты. | Дано: ............................................................................................................................................................ .................................................... .................................................... Найти .................................................... | Решение: ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… |
| Опыт №5 ПРИГОТОВЛЕНИЕ РАСТВОРА ЗАДАННОЙ КОНЦЕНТРАЦИИ | ||
| Сколько грамм сахара необходимо добавить к 300г. 60%-ного сахарного раствора, чтобы он стал 90%-ным | Дано: ............................................................................................................................................................ Найти .................................................... | ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… |
Общий вывод: ............................................................................................................................................................................................
……………………............................................................................................................................................................................……………………...........................................................................................................................................................................................................
…………...........................................................................................................................................................................................................
…………...........................................................................................................................................................................................................
ЛАБОРАТОРНАЯ РАБОТА №3
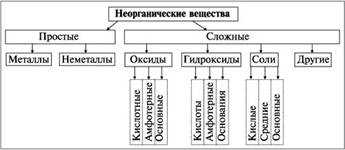
Тема: "Классы неорганических веществ"
Цель: Познакомиться с основными классами неорганических веществ, исследовать наиболее распространенные свойства данных соединений
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
ПРАКТИЧЕСКАЯ ЧАСТЬ
| Ход работы | Рисунки, реакции, наблюдения. | Выводы |
| Опыт № 1 ОЗНАКОМЛЕНИЕ СО СВОЙСТВАМИ КИСЛОТ Кислоты – сложные вещества, содержащие в своем составе водород и кислотныей остаток. | ||
| 1.1 Меняют цвет индикатора В 3-пробирки влить по 1мл. НСL и добавим лакмус, метилоранж, фенолфталеина. | Наблюдали: ............................................................................ ........................................................................................................................................................ | |
| 1.2 Взаимодействуют с металлами a) В 2-пробирки влить по 1-2мл. соляной кислоты и добавим кусочки меди и цинка. b) В 2 пробирки влить 1-2мл разбавленной азотной кислоты и добавить туда кусочки меди и цинка. В 3 пробирки влить 1-2мл концентрированной азотной кислоты и добавить туда кусочки меди, цинка и алюминия c) В 2 пробирки влить 1-2мл разбавленной серной кислоты и добавить туда кусочки меди и цинка. В 2 пробирки влить 1-2мл концентрированной серной кислоты и добавить туда кусочки меди, цинка. | А) Допишем реакции: HCL +Zn→....................................................... HCL +Cu→....................................................... ............................................................................ ............................................................................ Б) Допишем реакции: HNO3(разб) +Zn→NH3 +................................... HNO3(разб) +Cu→ NО +.................................. HNO3(конц) +Zn→NО2 +.................................. HNO3(конц) +Cu→ NО2 +................................ HNO3(конц) +Al→.............................................. ............................................................................ ............................................................................ ............................................................................ .......................................................................... С) Допишем реакции: H2 SO4(разб) +Zn→H2+..................................... H2 SO4(разб) +Cu→........................................... H2 SO4(конц) +Zn→SО2 +............................... H2 SO4(конц) +Cu→ SО2 +............................... ............................................................................ ............................................................................ ............................................................................ | |
| 1.3. Взаимодействуют с основными оксидами В 3-пробирки влить по 1мл. НСL и добавим оксиды Fe2O3 и CаО. Пробирку с Fe2O3 нагреем | Допишем реакции: HCL +Fe2O3→................................................... HCL +CаО→.................................................... Наблюдали: ............................................................................ ............................................................................ | |
| 1.4. Взаимодействуют с солями В пробирку влить 1мл серной кислоты и добавить хлорид бария. Нанести 1мл соляной кислоты на кусок мрамора. | Допишем реакции: HCL +СаСО3 →............................................... H2 SO4+ВаСL2 →............................................. Наблюдали: ............................................................................ ............................................................................ ...................................................................................................................................................... | |
| Опыт № 2 ОЗНАКОМЛЕНИЕ СО СВОЙСТВАМИ ОСНОВАНИЙ Основания -это соединения, состоящие из катионов металла (или катиона аммония) и гидроксильной группы ОН1- | ||
| 2.1 Меняют цвет индикатора В 3-пробирки влить по 1мл. NaOH и добавим лакмус, метилоранж, фенолфталеина | Наблюдали: .................................................................................................................................................................................................................. | |
| 2.2 Взаимодействуют с кислотами, вступая в реакцию нейтрализации В пробирку влить по 1мл. NaOH и добавим пару капель фенолфталеина, после чего добавить HCL | Допишем реакцию: NaOH +HCL→.................................................. Наблюдали: ............................................................................ ............................................................................ ........................................................................... | |
| 2.3Взаимодействуют с солями В пробирку поместим 1мл раствора CuSO4, добавим по 1-2 капли NaOH и индикатора. Осадок меди будем длительно нагревать до его разложения | Допишем реакцию: СuSO4+ NaOH ® ………………………… Сu(ОН)2 нагреем ®………………............ Наблюдали: ............................................................................ ............................................................................ | |
| Опыт №3 ОЗНАКОМЛЕНИЕ СО СВОЙСТВАМИ СОЛЕЙ Соли – это продукты полного или частичного замещения атомов «Н» в молекуле кислоты на металл(либоNH4+), либо групп «ОН» в молекуле основания на кислотный остаток | ||
| 3.1 Взаимодействуют друг с другом В пробирку поместим 1мл. раствора сульфида натрия Na2S, добавим 1мл. нитрата серебра AgNO3. | Допишем реакцию: Na2S+ AgNO3® ………………………… Наблюдали: ............................................................................ ............................................................................ | |
| 3.1 Взаимодействуют c металлами В 3пробирки поместим по 1мл. растворов AgNO3, СuSO4 Pb(NO3)2добавим металлы соответственно Сu, Fe, Zn | Допишем реакцию: Сu+ AgNO3® …………………………..… … Fe + СuSO4 ® ……………………………… Zn+ Pb(NO3)2® …………………………….. Наблюдали: ............................................................................ ........................................................................... ………………………………………………... | |
Общий вывод: .............................................................................................................................................................................................
……………………............................................................................................................................................................................……………………............................................................................................................................................................................……………………....................................................................................................................................................................................................
ЛАБОРАТОРНАЯ РАБОТ №4
Тема: "Гидролиз солей, испытание кислот и щелочей индикаторами"
Цель: Познакомиться с понятием «гидролиз солей».Научиться определять среду раствора солей, кислот, щелочей с помощью индикаторов и составлять реакции гидролиза.
ТЕОРЕТИЧЕСКИЙ ОБЗОР
Гидролиз – это процесс взаимодействия ионов соли с водой, приводящий к образованию слабого электролита.
Все соли можно разделить на 4 группы:
1. Соль образована сильным основанием и сильной кислотой К2 SО4, Na NO3,)– гидролиз не идет, среда нейтральная рН = 7.
2. Соль образована слабым основанием и слабой кислотой (MgСО3, Al 2S3, Zn(NO2)2, ..) - гидролиз протекает практически в нейтральной среде рН ближе к 7, гидролиз идет по катиону и аниону:
3. Соль образована сильным основанием и слабой кислотой (например: Na2СО3, К2S, Ва(NO2)2, СН3СОО Li) -гидролиз протекает в щелочной среде рН >7, гидролиз идет по аниону.
4. Соль образована слабым основанием и сильной кислотой (MgSО4, AlCL3, Zn(NO3)2, ..) - гидролиз протекает в кислой среде рН< 7, гидролиз идет по катиону.
Глубина гидролиза зависит от температуры (чаще всего ее приходится повышать) и концентрации раствора (при разбавлении раствора гидролиз усиливается)
Если продукты гидролиза летучи,или нерастворимы, то он необратим.
Сведения по веществам
· Сильные кислоты – кислоты, являющиеся сильными электролитами (H2SO4, HCl, HNO3, HBr, HI, HClO4 и другие).
· Слабые кислоты – кислоты, являющиеся слабыми электролитами (H2CO3, H2SO3, H2S, H2SiO3, H3PO4, НСN и другие)
· Сильные основания – сильные электролиты - щелочи (NaOH, KOH, и другие).
· Слабые основания – нерастворимые основания, слабые электролиты (Cu(OH)2, Ca(OH)2, NH4OH, Al(OH)3 и другие.
ХОД РАБОТЫ
| Ход работы | Рисунки, реакции, наблюдения | Выводы |
| Опыт №1 Определение характера среды кислот и щелочей | ||
| Возьмём по 3 стеклянных пробирки и заполним их соляной кислотой и щёлочью натрия Добавим в них индикаторы: лакмус, фенолфталеин и метилоранж . |
НCL (рН<7) NaOН(рН>7)
      Наблюдали:
………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………
Наблюдали:
………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………
| ............................... ............................... ................................ ................................ ................................. |
| Опыт №2 Определение характера среды растворов солей, кислот, щелочей. | ||
| А) Гидролиз соли,образованной сильными основание и кислотой В пробирку нальем 1 мл раствора Na2SO4,- внесем- 2-капли индикатора-лакмуса | Наблюдали: ........................................................................................................................................................................................................................................................................................................... Составить уравнения гидролиза: Na2SO4+ НОН→................................................... ............................................................................................................................................................... | |
| б) Гидролиз соли,образованной слабой кислотой и сильным основанием В пробирку нальем 1 мл раствора соли Na2СО3 и внесем 2 капли лакмуса. | Наблюдали:
 ...........................................................................................................................................................................................................................................................
Составить уравнения гидролиза:
Na2CO3+ НОН →....................................
............................................................................
.............................................................................
Nа2SiO3+ НОН →......................................
............................................................................
............................................................................. ...........................................................................................................................................................................................................................................................
Составить уравнения гидролиза:
Na2CO3+ НОН →....................................
............................................................................
.............................................................................
Nа2SiO3+ НОН →......................................
............................................................................
.............................................................................
| |
| в) Гидролиз соли, образованной слабым основанием и сильной кислотой. В пробирку нальем 1 мл раствора соли ZnSO 4 и внесем 1-2 капли лакмуса В пробирку нальем 1 мл раствора соли CuSO 4 и внесем 1-2 капли лакмуса | Наблюдали:
 ...........................................................................................................................................................................................................................................................................................................
Составить уравнения гидролиза:
ZnSO4+ НОН ®................................................
..............................................................................................................................................................
СuSO4+ НОН ®....................................................
................................................................................
.............................................................................................................................................................. ...........................................................................................................................................................................................................................................................................................................
Составить уравнения гидролиза:
ZnSO4+ НОН ®................................................
..............................................................................................................................................................
СuSO4+ НОН ®....................................................
................................................................................
..............................................................................................................................................................
| |
| Опыт №3 Влияние температуры на гидролиз | ||
| В пробирку нальем 1 мл раствора соли Na2SO3 и 1мл фенолфталеина. Поместим в раствор индикаторную бумагу, нагреем содержимое пробирки в пламени горелки. | Наблюдали: …………………………………………………………………………………………………………………………………………………………………………….. Na2SO3+ НОН ®................................................ ................................................................................. ................................................................................................................................................................................................................................................................................................................................................................................................................. | |
Общий вывод:…………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………….................
ЛАБОРАТОРНАЯ РАБОТА №5
Тема: " Реакции соединения, разложения, замещения, обмена, эндо-и экзо-термические реакции. РИО, идущие необратимо"
Цель: Научиться практически выполнять реакции соединения, разложения, замещения, ионного обмена. составлять РИО, идущие необратимо.
ТЕОРЕТИЧЕСКИЙ ОБЗОР
· Экзотермическая реакция — химическая реакция, сопровождающаяся выделением тепла.
· Эндотермическая реакция — химическая реакция, сопровождающаяся поглощением тепла.
· Реакция замещения — это реакции, в результате которых происходит замещение одних атомов, содержащихся в молекуле, на другие. В данную реакцию вступает одно сложное вещество и одно простое, в результате образуется новое простое и новое сложное вещества:СuSO4+ Zn®ZnSO4+ Cu
· Реакция разложения — это реакции, в результате которых из исходного вещества образуется два и более новых веществ: СаСО3 нагревание ® СаО+СО2
· Реакции обмена — это реакции, в результате которых происходит обмен атомами, входящими в состав молекулы: НCL+AgNO3® AgCL¯+ HNO3
· Реакция присоединения — это реакции в результате которых из исходных веществ получается одно новое вещество: Н2+ CL2®2HCL.
Ионные реакции -реакции протекающие в растворах между ионами.
Реакции ионного обмена не сопровождается изменением заряда ионов (степени окисления атомов). Возможно два варианта исхода РИО: а) реакция идет обратимо; б) реакция идет необратимо.
Реакции ионного обмена идут в соответствии со схемой: AB + C Д à АД + ВС
РИО протекает необратимо в трех случаях, когда образуется: трудно растворимое соединение(осадок), газообразные вещества (H2S, CO2, NH3...), малодиссоциирующих веществ (Н2О, НСN,CH3COOH, НNO2, H3PO4)
Нестойкие соединения. NH4OH→ NH3 + H2O; H2CO3 → CO2 + H2O; H2SO3 → H2O + SO2
ХОД РАБОТЫ
| Ход работы | Рисунки, реакции, наблюдения. | Выводы | |||||
| Опыт № 2 РЕАКЦИИ ПРИСОЕДИНЕНИЯ, РАЗЛОЖЕНИЯ И ЗАМЕЩЕНИЯ | |||||||
| а)Реакция замещения В пробирку поместим 1мл. Cu SO4 и железную скрепку (внесем в пробирку 1-2 капли Н2SO4 раз.) красной кровяной соли. | Составим уравнения реакций: а) Cu SO4 + Fe ®…..…………………………
……………………………………… …………………………………….... |
…………………………………………………………………………………………………………………………………………………………………………………………………………………. | |||||
| б)Реакция разложения В фарфоровую чашку поместить небольшой горкой дихромат аммония (NH4)2Cr2O7 и ввести в центр горки горящую спичку. | Наблюдали: | ||||||
| (NH4)2Cr2O7 ®N2 + Cr2O3 + 4H2O
………………………………… ………………………………… ………………………………… ………………………………
| |||||||
| в) Реакция присоединения Железную скрепку внесем в пламя горелки (образуется оксид Fe2О3) | |||||||
| в) O2 + Fe ®…..…………………………… Наблюдали: ………………………………………………........ | |||||||
|
Опыт №3 РЕАКЦИИ ИОННОГО ОБМЕНА ИДУЩИЕ НЕОБРАТИМО | |||||||
| а)Образование осадка. В пробирку к 1 мл раствора сульфата меди прильем по каплям раствор щелочи | Составим РИО: СuSO4+ NaOH®……………………………… .................................................................................... ............................................................................... Наблюдали: |
…………………………………………………………………………………………………………………………………………………………………………………………………………………. | |||||
|
| .................................................................................................................................................. | ||||||
| б)Образование газа В пробирку с 1 мл раствора карбоната натрия (Na2CO3) осторожно прильем 1 мл соляной кислоты | HCL + Na2CO3®……………………………… .................................................................................... ...................................................................................... Наблюдали: | ||||||
|
| .............................................................................................................................................................................................................. | ||||||
| в)Образование воды В пробирку к 1 мл раствора едкого натра прильем каплю фенол-фталеина и добавим 1 мл.. | NaOH + HCL ®.................................................. ...............………….……………………………… ……………………………………........................... Наблюдали:.................................................................................... ...................................................................................... | ||||||
| г)Образование осадка и его растворение В пробирке смешаем по 1 мл раствора cжелеза (III) и едкого натра. К полученному осадку гидроксида железа(III) прильем раствор HCL | FeCl3 + NaOH® ……………………………… …………………………………………………… ……………………………………………… Fe(OH)3 + HCL ® ………………… .................................................................................................................................................................... Наблюдали: | ||||||
|
| |||||||
| Опыт №3 РАСПОЗНОВАНИЕ ЭКЗОТЕРМИЧЕСКИХ И ЭНДОТЕРМИЧЕСКИХ РЕАКЦИИ | |||||||
| а)В стеклянный стакан внести 2-3 гранулы NaOH и добавим воду. Измерим температуру раствора термометром. | Наблюдали:.................................................................................. .................................................................................. .................................................................................. ……………………………………………………..
|
................................................................................................................................................................................................. | |||||
| б) В пробирку к 1 мл раствора NaOH добавим 2-4 капли раствора NH4CL, нагреем до появления запаха | NH4CL+NaOH→.....................................................…………………………………………… ……………………………………............... Наблюдали:..................................................................................
| ||||||
Общий вывод: …………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
ЛАБОРАТОРНАЯ РАБОТА №6
Тема: "Факторы, влияющие на скорость реакции."
Цель: Познакомиться с понятиями: гомогенная и гетерогенная реакция, скорость реакции, химическое равновесие. Научиться составлять уравнения прямой и обратной реакции, выражать константу равновесия, определять зависимость скорости от природы реагирующих веществ, их концентрации, температуры, поверхности соприкосновения и использования катализаторов.
ТЕОРЕТИЧЕСКИЙ ОБЗОР
Скорость химической реакции ( ט )- определяется изменением концентрации одного из реагирующих веществ в единицу времени: ט = ∆С / ∆ t
· Гомогенные системы - реакции, компоненты которых находятся в одинаковом физическом состоянии -в газообразном или растворенном:
аАгаз + вВгаз→сСгаз + dD газ
По закону действующих масс:
-Скорость прямой реакции равна: ט пр. = Кпр. ∙ СА а ∙ СВ в = Кпр
-Скорость обратной реакции равна: ט обр.= Кобр.. ∙ СС с ∙ СD d= Кобр..
ü К - константа скорости, величина постоянная;
ü С (Р)- молярные концентрации(давление) реагентов
· Гетерогенные системы - реакции, компоненты которых находятся в разных физических состояниях -в газообразном, в растворенном, в твердом.
Скорость реакции изменяется только в зависимости от концентрации газов и растворенных веществ:
аАтверд.. + вВгаз→сСжидк.
-Скорость прямой реакции равна: ט пр. = Кпр. ∙ СВ в
-Скорость обратной реакции равна: ט обр.= Кобр.. ∙ СС с
Ф а к т о р ы, в л и я ю щ и е н а с к о р о с т ь р е а к ц и и.
- Природа реагирующих веществ
- Концентрация реагирующих веществ.
Чем выше концентрация веществ, тем больше скорость, протекающей реакции.
- Температура - зависимость скорости реакции от температуры выражается правилом Вант
Гоффа: при повышении температуры на 10 градусов скорость химической реакции увеличивается в 2-4 раза, где V 2 и V 1 - скорости реакций при температурах t 2 и t 1; γ - температурный коэффициент скорости реакции.
- Поверхность реагирующих веществ.
- Ингибитор, катализатор.
Изменение скорости реакции под действием катализаторов называют - катализом.
Химическое равновесие - это такое состояние обратимого химического процесса, при котором скорости прямой и обратной реакций равны между собой: ט пр. = ט обр Концентрации реагирующих веществ, которые устанавливаются при химическом равновесии, называются равновесными.
ПРАКТИЧЕСКАЯ ЧАСТЬ
| Ход работы | Рисунки, реакции, наблюдения. | Выводы | |
| Опыт № ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ | |||
| а) Добавим к цинку серную кислоту в 2х различных концентрациях. По количеству выделенного Н2 определим, как влияет концентрация кислоты на скорость реакции б) Как изменится скорость реакции, если увеличить концентрацию Н2 в 2раза | а)Zn+ Н2SO4® …………………………………… У равнения скорости прямой и обратной реакции: ........................................................................................................................................................................ Наблюдали: ……............................................................................. …………………………………………………………… б) N2(г)+ 3H2 (г) →2NH3(г) Расчет: ……............................................................................. …………………………………………………………… ……............................................................................. | ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… | |
|
Опыт №2 ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ | |||
| а) Добавим к цинку серную кислоту при 2х различных температурах. По количеству выделенного Н2 определим, как влияет температура кислоты на скорость реакции б) Определить скорость реакции при 600С, если при 200С скорость равна 0,5моль/л.с., а температурный коэффициент- 2 | а)Наблюдали:
……..................................................................................................................................................................................................................................................
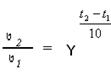 б)Расчет:
…….....................................................................................................................................................................................................................................................................................................................................
б)Расчет:
…….....................................................................................................................................................................................................................................................................................................................................
| ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… | |
| Опыт №3 ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ПОВЕРХНОСТИ РЕАГИРУЮЩИХ ВЕЩЕСТВ | |||
| Добавим к гранулам цинка различного размера серную кислоту. По количеству выделенного Н2 определим, как влияет поверхность веществ на скорость реакции. | Наблюдали: …….............................................................................................................................................................................................................................................. .................................................................................................................................................................... | …………………………………………………………………………………………………………………………………… | |
| Опыт №4 ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ПРИРОДЫ РЕАГИРУЮЩИХ ВЕЩЕСТВ | |||
| Добавим к гранулам цинка уксусную и серную кислоты. По количеству выделенного Н2 определим влияние природа веществ на скорость реакции. | Составим реакции: СН3СООН + Zn→……………………………… H2SO4+ Zn→……………………………… Наблюдали: ……............................................................................................................................................................... | ……………………………………………………………………………………………………………………………………………………………… | |
| Опыт №5 ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КАТАЛИЗАТОРА И ИНГИБИТОРА | |||
| А) Сравним разложение перекиси водорода в присутствии МnO2 и без него. Б) Сравним количество образованного Н2 при взаимодействии цинка с H2SO4 в присутствии формалина и без него. | Составим реакции: 2Н2О2 MnO 2 → 2Н2О + О2 H2SO4+ Zn→……………………………… Наблюдали: ……......................................................................................................................................................................................................................................................... | …………………………………………………………………………………………………………………………………… | |
| Опыт №6 ХИМИЧЕСКОЕ РАВНОВЕСИЕ | |||
| В 3 пробирки нальём раствор хлорида железа и прильём в них родонит калия KCNS, растворы разбавим водой. Поочерёдно добавим в растворы исходные реагенты и хлорид железа. | Составим реакцию: FeCl3(ж)+3KCNS(ж) =Fe(CNS)3(ж)+3KCl(ж)
Кравнов.=
Наблюдали: ……...............................................................................……..................................................................................................................................................................... | …………………………………………………………………………………………………………………………………………………………………………………………………………………… | |
Общий вывод:
……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
ЛАБОРАТОРНАЯ РАБОТА №7
Тема: "Получение чугуна и стали. "
Цель: Ознакомится с процессами производства чугуна и стали с помощью флеш -анимации; изучить химические процессы производства, сырьё, продукты, виды чугуна, виды сталей; научиться выполнять расчеты, связанные с получением металлов.
ТЕОРЕТИЧЕСКИЙ ОБЗОР
Чугун- сплав железа с углеродом (1,7-5%) и металлургическими примесями (Mn, Si, P и др.)
Для выплавки чугуна в доменных печах используют: руду: магнитный железняк (Fe3O4); красный железняк (Fe2O3), бурый железняк (гидраты оксидов железа 2Fe2O3 * 3H2O и Fe2O3 * H2O) и др.
· Топливо: кокс, но возможна частичная замена газом, мазутом.
· Флюсы: известняк CaCO3, доломитизированный известняк(CaCO3 + MgCO3)
ТЕХНОЛОГИЧЕСКИЙ ПРОЦЕСС
I. Подготовка руд ы - дробление и сортировка, обогащение руды (промывка, магнитная сепарация), агломерация. Для агломерации шихту, состоящую из железной руды (40…50 %), известняка (15…20 %), кокса (4…6 %), влаги (6…9 %), спекают при температуре 1300…1500 0С., образуются окатыши.
II. 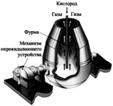 Доменный процесс. А гломерат направляют в доменную печь, где при температуре1000…1100 0C.восстановленное из руды твердое железо, взаимодействуя с оксидом углерода, коксом и сажистым углеродом, интенсивно растворяет углерод. Капли железоуглеродистого сплава, протекая по кускам кокса, дополнительно насыщаются углеродом (до 4%), марганцем, кремнием, фосфором которые при температуре 1200 0Cвосстанавливаются из руды, и серой, содержащейся в коксе. В нижней части доменной печи образуется шлак в результате сплавления окислов пустой породы руды, флюсов и золы топлива. Сливают чугун каждые 3…4 часа, шлак -1,5-2 часа. Шлаки содержат Al2O3, CaO, MgO, SiO2, MnO, FeO, CaS. Чугун отправляют на производство стали или формуют (литьем) в виде чушек-слитков массой 45 кг.
Доменный процесс. А гломерат направляют в доменную печь, где при температуре1000…1100 0C.восстановленное из руды твердое железо, взаимодействуя с оксидом углерода, коксом и сажистым углеродом, интенсивно растворяет углерод. Капли железоуглеродистого сплава, протекая по кускам кокса, дополнительно насыщаются углеродом (до 4%), марганцем, кремнием, фосфором которые при температуре 1200 0Cвосстанавливаются из руды, и серой, содержащейся в коксе. В нижней части доменной печи образуется шлак в результате сплавления окислов пустой породы руды, флюсов и золы топлива. Сливают чугун каждые 3…4 часа, шлак -1,5-2 часа. Шлаки содержат Al2O3, CaO, MgO, SiO2, MnO, FeO, CaS. Чугун отправляют на производство стали или формуют (литьем) в виде чушек-слитков массой 45 кг.
III. Сталь – сплав железа с углеродом (до 1,7%) и металлургическими примесями Mn, Сr, Si,Ni. Основными исходными материалами являются передельный чугун и стальной лом (скрап). Способы получения стали:
· Конверторный способ основан на продувке сжатым воздухом расплавленного чугуна.
· 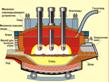 Мартеновский способ вызван к жизни необходимостью перерабатывать стальной лом
Мартеновский способ вызван к жизни необходимостью перерабатывать стальной лом
· Плавка стали в электропечах дает возможность получать высококачественные стали.
По химическому составу стали делят на углеродистые и легированные.
¾ Углеродистые стали, кроме углерода, содержат до 0,35% кремния, 0,8% марганца, 0,06% серы, 0,07% фосфора. Различают мало-, средне- и высокоуглеродистые стали.
¾ Легированные стали имеют в своем составе легирующие элементы (хром, никель, вольфрам, ванадий, молибден, кобальт и др.) для сообщения стали требуемых свойств.
Нержавеющей сталью называется сталь, обладающая стойкостью против атмосферной коррозии. Это обеспечивается введением легирующих элементов хрома и меди.
По назначению делятся на:
¾ Конструкционные;
¾ инструментальные;
¾ стали с особыми свойствами.
По способу выплавки различают сталь обыкновенного качества, качественную и высококачественную.
Закалка — распространенный процесс термической обработки стальных деталей. Она осуществляется путем нагрева деталей,выдержки при этой температуре и быстрого охлаждения. Основная цель закалки стали — получение высокой твердости, износостойкости и физико-механических свойств.
Отпуск заключается в нагреве закаленной заготовки до определенной температуры и последующем охлаждении ее на воздухе, в воде, масле или других охлаждающих средах. Отпуск уменьшает хрупкость, повышает вязкость, улучшает обрабатываемость резанием.
ПРАКТИЧЕСКАЯ ЧАСТЬ
| Ход работы | Рисунки, реакции, наблюдения. | Выводы | |
| Опыт № 1 ИССЛЕДОВАНИЕ ПРОЦЕССА ПОЛУЧЕНИЯ ЧУГУНА ИСТАЛИ | |||
Просмотрим видео анимацию. "Производство чугуна и стали ".
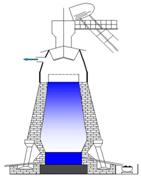 Доменная печь
Доменная печь
| Определим формулы соединений, дадим описание сырья и продуктов реакций: 1. Кокс.................................................................................................................. 2. Известняк......................................................................................................... 3. Магнитный железняк..................................................................................... 4. Красный железняк......................................................................................... 5. Бурый железняк............................................................................................... 6. Чугун................................................................................................................ 7. Шлак................................................................................................................. 8. Сталь.................................................................................................................
| ||
| Опыт № 2 ИССЛЕДОВАНИЕ ОБРАЗЦОВ СТАЛИ | |||
| Рассмотрим образцы 1. малоуглеродистую 2. среднеуглеродистую 3. высокоуглеродистую 4. нержавеющую | Описание образцов стали: 1. ………………..………………………………………………………… 2. ……………..…………………………………………………………… 3. ………………………………..………………………………………… 4. ………………………………………………………………………… | ||
| Опыт № 3 ОПРЕДЕЛЕНИЕ МАССОВОЙ ДОИ МЕТАЛЛА В РУДЕ | |||
| Задача №2 Определить массовую долю алюминия в природном соединении К2О* Al2O3*6SiO2 | Дано: …………………………………………………………………………………………… Найти .................................................... | Решение: …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… | |
| Опыт № 4 ОПРЕДЕЛЕНИЕ МАССЫ МЕТАЛЛА В РУДЕ | |||
| Задача Руда массой 500кг, содержит 25% рутила TiO2, определить массу титана, полученного из этой руды: | Дано: ............................................................................................................................................Найти ..................................... | Решение: ……………………………………………………………………………………………………………………………………………………………………………… | |
| Опыт № 5 ОПРЕДЕЛЕНИЕ МАССЫ РУДЫ | |||
| Задача Определить массу руды, содержащую 20% Fe3O4, если из неё получено 40г железа. | Дано: ............................................................................................................................................ Найти .................................................... | Решение: ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….
| |
Общий вывод:...........................................................................................................................................................
...............................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................
ЛАБОРАТОРНАЯ РАБОТА №8
Тема: " Получение, собирание и распознавание газов. Решение экспериментальных задач."
Теоретический обзор
· Углекислый газ или оксид углерода (IV) СО2 – бесцветный, не имеющий запах газ.
Он примерно в полтора раза тяжелее воздуха. Растворим в воде. В лаборатории углекислый газ получают действием соляной кислоты на карбонат кальция:
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑.
Распознание:
- Помутнение известковой воды (продувание углекислого газа через известковую воду)
СО2 + Са(ОН)2 = СаСО3 + Н2О; - Горящую лучину опустить в сосуд с углекислым газом. Лучина гаснет.
· Водород (Н2) – самыйлегкий, бесцветный, не имеет запаха.
Вытеснением водорода металлами из растворов кислот: Zn + 2HCl = ZnCl2 + H2 ↑.
· Кислород (О2) без запаха и цвета, тяжелее воздуха, мало растворим в воде.
1.Разложением перманганата калия: 2KMnO4 = K2MnO4 + MnO2 + О2 ↑;
2.Разложением пероксида водорода:2H2O2 = 2Н2О + О2 ↑.
Вспыхивание тлеющей лучинки, внесенной в сосуд с кислородом.
· Аммиак (NН3) имеет резкий характерный запах, без цвета, хорошо растворим в воде, легче воздуха.
1.В промышленности:
3H2 + N2 = 2NH3;
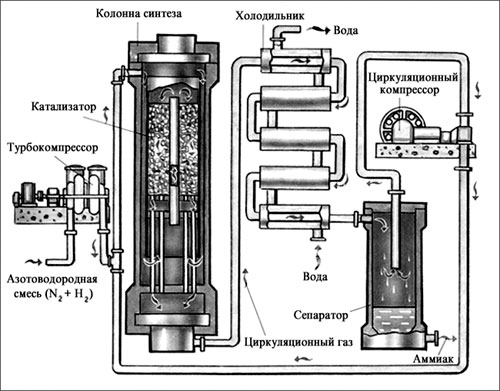
2.В лаборатории:
NH4Cl + NaOH = NaCl + H2O + NH3↑.
ПРАКТИЧЕСКАЯ ЧАСТЬ
| Ход работы | Рисунки, реакции, наблюдения. | Выводы |
| Опыт №1 ПОЛУЧЕНИЕ АММИАКА И ЕГО ОБНАРУЖЕНИЕ. | ||
Соберем прибор.
 В фарфоровой чашке измельчим 1г. NH4CL и 0,5г Ca(OH)2.Смесь поместим в сухую пробирку и нагреем. Осторожно понюхаем полученный газ. Поднесем к отверстию трубки лакмусовую бумажку. Соберем газ в пробирку и опустим в нее стеклянную палочку смоченную в соляной кислоте. В фарфоровой чашке измельчим 1г. NH4CL и 0,5г Ca(OH)2.Смесь поместим в сухую пробирку и нагреем. Осторожно понюхаем полученный газ. Поднесем к отверстию трубки лакмусовую бумажку. Соберем газ в пробирку и опустим в нее стеклянную палочку смоченную в соляной кислоте.
| Запишем РИО: NH4CL + Ca(OH)2→ …..……………… ..................................................................... Допишем реакцию: NH3+ HCL→ …..………………………... Наблюдали: …………………………………………………………………………………………………………………………………………………………………………………………………………. | ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… |
| Опыт №2 ПОЛУЧЕНИЕ КИСЛОРОДА И ЕГО ОБНАРУЖЕНИЕ. | ||
| В пробирку внесем 1-2 мл. KMnO4 добавим 1мл.соляной кислоты. В полученный газ опустим зажженную лучину. |  Наблюдали:
………………………………………………………………………………………………………….
2KMnO4 = K2MnO4 + MnO2 + О2 ↑; Наблюдали:
………………………………………………………………………………………………………….
2KMnO4 = K2MnO4 + MnO2 + О2 ↑;
| ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… |
| Опыт № 3. ПОЛУЧЕНИЕ ОКСИДА АЗОТА (II) И ЕГО ОБНАРУЖЕНИЕ. | ||
| На дно пробирки поместим 1гр. NaNО3 (или КNО3) и добавим 4-5 капель серной кислоты. Доведем содержимое пробирки до кипения. Осторожно поместите в пробирку медную проволоку. | Допишем реакции и подберем коэффициенты:
NaNО3+ Н2SO4®………………………
HNО3(кон.)+Си®Си(NО3)2+NO2+H2 O
 Наблюдали:
………………………………………………………………………………………………….......... Наблюдали:
…………………………………………………………………………………………………..........
| ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… |
| Опыт №4 ПОЛУЧЕНИЕ УГЛЕКИСЛОГО ГАЗА И ЕГО ОБНАРУЖЕНИЕ. | ||
| В пробирку внесем 1-2 кусочка мрамора и добавим 1мл.соляной кислоты. В полученный газ опустим зажженную лучину. |  Наблюдали:
…………… …………………………………………………………………………………………….……
Допишем реакцию (РИО):
СаСО3 +HCL®……………………
………………………………………………………………………………………… Наблюдали:
…………… …………………………………………………………………………………………….……
Допишем реакцию (РИО):
СаСО3 +HCL®……………………
…………………………………………………………………………………………
| ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… ………………………… |
Общий вывод:...........................................................................................................................................................
...............................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................
ЛАБОРАТОРНАЯ РАБОТА №9
Тема: "Изготовление моделей молекул углеводородов. Обнаружение углерода в органических соединениях»
Цель: Изучить строение молекул метана, этилена, ацетилена, циклопрпана, бензола и их гомологов. Научиться: изготавливать шаростержневые модели этих молекул и определять характер связей; обнаруживать углерод в органических соединениях с помощью реакции горения.
ТЕОРЕТИЧЕСКИЙ ОБЗОР
| 1. При перекрывании всех 4х орбиталей 2S1, 2Px1, 2Py1, 2Pz1 атом углерода переходит в S р3 – гибридное состоянии. На образовавшихся новых 4х орбиталях, находится по 1 неспаренному электрону, а сами они направлены к несимметричными вершинам тетраэдра, образуя валентный угол j = 109028¢ | Углерод в Sр3 гибридном состоянии образует - простую, одинарную связь
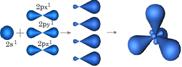 S р3 – гибридное состоянии.
S р3 – гибридное состоянии.
|
| 2. При перекрывании орбиталей 2S1, 2Px1, 2Py1 атом углерода переходит в S р2 – гибридное состоянии. Перекрываясь,три орбитали изменяют форму и становятся несимметричными, образуя между собой валентный угол j = 1200. Орбиталь 2Pz1 остается без изменений, так как в гибридизации не участвует. | Углерод в Sр2 гибридном состоянии образует «=» двойную связь.
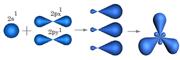 S р2 – гибридное состоянии.
S р2 – гибридное состоянии.
|
| 3. При перекрывании орбиталей 2S1, 2Px1 атомуглерода переходит в S р – гибридное состоянии. Перекрываясь, две орбитали изменяют форму и становятся несимметричными, образуя между собой валентный угол j = 1800.Орбитали 2Py1 и 2Pz1 остаются без изменений, в гибридизации не участвуют. | Углерод в Sр -гибридном состоянии образует «≡» тройную связь
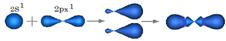 S р – гибридное состоянии.
S р – гибридное состоянии.
|
σ- связь (сигма-связь) — ковалентная связь, образующаяся перекрыванием электронных облаков «по осевой линии». π-связь (пи-связь) -это связь, образованная по обе стороны от линии соединяющей центры атомов
ПРАКТИЧЕСКАЯ ЧАСТЬ
| Ход работы | Рисунки, реакции, наблюдения. | Выводы | ||||||||||||
| Опыт №1 ОБНАРУЖЕНИЕ УГЛЕРОДА И ВОДОРОДА В ГЕКСАНЕ И КЕРАСИНЕ | ||||||||||||||
| Нальём немного керасина и гексана, подожжём. Обратим внимание на цвет пламени и характер горения керасина и гексана | Наблюдали: ………………………………………………………………………………………………Урав
Дата добавления: 2018-10-14; Мы поможем в написании ваших работ!; просмотров: 743 | Нарушение авторских прав Поиск на сайте: Лучшие изречения: |
|||||||||||||
Ген: 0.016 с.





 Наблюдали:
Наблюдали:

 .......................................................................
.......................................................................