ГОСТ Р ИСО 15189-2009
ЛАБОРАТОРИИ МЕДИЦИНСКИЕ
ЧАСТНЫЕ ТРЕБОВАНИЯ К КАЧЕСТВУ И КОМПЕТЕНТНОСТИ
(утв. Приказом Ростехрегулирования от 09.12.2009 N 629-ст)
1. Лаборатория должна участвовать в межлабораторных сличениях, организованных системами внешней оценки качества. Руководство лаборатории должно отслеживать результаты внешней оценки качества и участвовать в проведении корректирующих действий в случаях, когда контрольные критерии не достигнуты. Программы межлабораторных сличений должны в основномсоответствовать установленным требованиям (ИСО/МЭК.Руководство 43-1).
Программы внешней оценки качества должны, насколько это возможно, устанавливать клинически важные задачи, которые имитируют пробы пациентов и позволяют оценить весь аналитический процесс, включая пре- и постаналитические процедуры.
7. ПРИКАЗ Минздрава РФ от 26.05.2003 N 220 "ОБ УТВЕРЖДЕНИИ ОТРАСЛЕВОГО СТАНДАРТА "ПРАВИЛА ПРОВЕДЕНИЯ ВНУТРИЛАБОРАТОРНОГО КОНТРОЛЯ КАЧЕСТВА КОЛИЧЕСТВЕННЫХ МЕТОДОВ КЛИНИЧЕСКИХ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ С ИСПОЛЬЗОВАНИЕМ КОНТРОЛЬНЫХ МАТЕРИАЛОВ"
Отраслевой стандарт "Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов" устанавливает единый порядок внутрилабораторного контроля качества количественных исследований, выполняемых в клинико-диагностических лабораториях, медицинских организациях, в составе которых действуют лаборатории.
ВЕДЕНИЕ ОСТ
Ведение ОСТ осуществляется Московской медицинской академией им. И.М. Сеченова Минздрава России.
3. В КДЛ производится:
1. Регистрация и обработка всего поступающего биологического материала и проб больных, в том числе с использованием персонального компьютера (ЛИС);
2. Занесение результатов в специальные журналы;
3. Выдача бланков по отделениям осуществляется в тот же день;
4. Ведение документации по санэпидрежиму;
5. Ведение документации по материально-техническому оснащению лаборатории.
Ежедневно производятся все виды исследований, за исключением многоэтапных и трудоемких методик и исследований: ИФА, ПЦР, цитологические методы исследования и т. д.
Особое значение придается выполнению требований противоэпидемического режима, инструкции составлены на основании приказов МЗ СССР №408, №720, №752, №916, №1230, отраслевых стандартов ОСТ 42-21-2-85 22 «Стерилизация и дезинфекция изделий медицинского назначения. Методы, средства и режимы».
Приказ Минздрава №720 от 31.07.78. «Об улучшении медицинской помощи больным с гнойными хирургическими заболеваниями и усилении мероприятий по борьбе с внутрибольничной инфекцией».
Приказ Минздрава №408 от 12.07.1989 «О мерах по снижению заболеваемости вирусными гепатитами в стране».
Приказ Минздрава №916 от 04.08.1983. «Об утверждении инструкции по санитарно - противоэпидемическому режиму и охране труда персонала инфекционных больниц (отделений)».
Приказ Минздрава №1175 от 21.11.1979 «Об унификации клинических лабораторных методов исследования» (вместе с «методическими указаниями по применению унифицированных клинических лабораторных методов исследования»)
Перечень унифицированных методов клинических лабораторных исследований (приложение N 1) в дополнение к приказу N 290 от 11.04.1972.
В КДЛ необходимо иметь:
· Должностные инструкции на каждого сотрудника;
· На каждом рабочем столе инструкции, необходимые для проведения исследований и процедур (методик);
· Инструкции по работе на аппаратуре;
· Калибровочные таблицы для расчета единиц измерений (СИ), составленные в соответствии с приказами (№380, №545 «О дальнейшем совершенствовании контроля качества клинических лабораторных исследований и участии КДЛ в ФСФОК, ВОК», №60 «О состоянии и перспективах развития лабораторной клинико-диагностической службы в стране»).
На основании приказа МЗ СССР №1175 от 23.07.90 г. «Расчетные нормы времени на клинические лабораторные исследования» организована структура рабочей недели, рассчитана нагрузка сотрудников, соответственно функциональным обязанностям врачей и лаборантов процентном соотношении.
4.Контроль качества клинических лабораторных исследований существует в двух взаимосвязанных формах: внутрилабораторного контроля качества и внешней оценки качества. Внешняя оценка качества лабораторных исследований в медицинских организациях Российской Федерации регламентируется соответствующими нормативными документами. Внутрилабораторный контроль качества клинических лабораторных исследований осуществляется сотрудниками каждой клинико-диагностической лаборатории с целью поддержания стабильности аналитической системы и регламентируется нормативными документами медицинской организации
Внутрилабораторный контроль качества – объективная проверка результатов лаборатории, осуществляемая ежедневно непосредственно в лаборатории, ˗преимущественно с целью оценки воспроизводимости. Внутрилабораторный контроль качества решает две основные задачи: контроль переменных внешних факторов (разные партии реагентов, калибровочных материалов и пр.) и контроль стабильности выполнения методики в лаборатории.
Цель внутрилабораторного контроля качества – выявление и устранение отклонений от стабильного выполнения теста в лаборатории, т. е. выявление и устранение недопустимых аналитических ошибок. Порядок проведения внутрилабораторного контроля качества состоит из трех последовательных стадий:
Стадия 1: Оценка сходимости результатов измерения.
Стадия 2: первый, второй и третий этапы. Оценка воспроизводимости и правильности результатов измерений (установочные серии), построение контрольных карт.
Стадия 3: Проведение оперативного контроля качества результатов лабораторных исследований в каждой аналитической серии.
Контроль качества должен быть:
- систематическим, повседневным, проводится по единым правилам, анализ проб должен включаться в обычный ход работы лаборатории;
- объективным;
- проводиться в реальных условиях лаборатории;
- охватывать все области измерений.
Принцип проведения внутреннего контроля качества достаточно прост: периодически в каждой серии нужно осуществлять измерение одного и того же контрольного материала, а результаты этих измерений заносить на контрольную карту.
Для оценки качества исследований рассчитываются статистические показатели:
- Среднее арифметическое значение (Хср):
Хср = 
Хi– значения конкретных измерений, n – число измерений.
- Отклонение от правильного значения, разница между истинной величиной (μ) и средней арифметической, отражает величину систематической ошибки (b) и соответственно точность определений (В, %):
Абсолютная величина (b) = Хср– μ
Или
В (отклонение, %) = 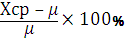
- Стандартное отклонение (σ, SD):
σ = √
Стандартное отклонение отражает величину случайной ошибки, т. е. воспроизводимость конкретного измерения в абсолютной величине.
- Коэффициент вариации (V или CV):
CV = 
Коэффициент вариации отражает воспроизводимость в относительном значении (процентах). Чем меньше CV, тем выше воспроизводимость результатов.
Внутрилабораторный контроль качества с использоанием аттестованной контрольной крови (контроль правильности ивоспроизводимости). Контрольный материал должен быть аттестован для вашего прибора и в паспорте указаны референсные границы контролируемых параметров.
Существует несколько принципов оценки контрольных карт, однако общепринятыми являются правила Вестгарда:
· Один из результатов в серии вышел за предел Хср±2σ - сигнал для применения других критериев.
· Один из результатов в серии вышел за предел Хср±3σ- случайная ошибка.
· Разница между двумя измерениями в серии превышает 4σ- случайная ошибка.
· Два последовательных измерения в серии вышли за предел Хср+ 2 σ или Хср - 2 σ – систематическая ошибка.
· Четыре последовательных измерения в серии вышли за предел Хср+ 1 σ или Хср - 1 σ – систематическая ошибка
· Десять последовательных измерений лежат по одну сторону от средней линии Хср – систематическая ошибка.
Предупредительные действия:
- периодический просмотр /обслуживание оборудования, документация этих действий;
- создание соответствующих условий для хранения реактивов, контрольной крови и проб пациентов;
- точная маркировка всех реагентов и проб;
- нанесение на контрольную карту всех пометок, связанных с заменой реагентов, калибраторов и пр.
Внутрилабораторный контроль качества без использования контрольной крови (контроль воспроизводимости).
Контроль качества поежедневным средним (используются результаты исследования образцов пациентов).
Преимуществом этого метода является то, что не требуется специального контрольного материала, позволяет выявлять ошибки на преаналитическом этапе.
Данный метод имеет ряд ограничений:
- обследуемый изо дня контингент должен быть достаточно однородным;
- в расчет должны приниматься только те значения, которые принимаются в определенные пределы;
- пределы усреднения могут быть установлены произвольно (диапазон усреднения не должен быть слишком узким, но и не должен быть слишком широким);
- минимальное количество усредняемых ежедневно результатов должно быть не менее 15;
- большая часть пациентов должна иметь результаты в области усреднения.
Карты по ежедневным средним анализируются по тем же правилам, что и карты по контрольным материалам.
Контрольная карта Шухарта строится автоматически при работе по программе контроль качества с аттестованным контрольным материалом. Для каждого вида контрольного материала (нормальная, патологически низкая или патологически высокая) строится своя контрольная карта.
Для построения карт (аналогично картам Шухарта) необходимо выполнить следующие действия:
- 20 дней рассчитывать среднее по результатам пациентов;
- по этим значениям рассчитать среднюю, стандартное отклонение и коэффициент вариации;
-если коэффициент вариации (CV) будет существенно больше, чем CV контрольным материалам, то надо увеличить количество усредняемых результатов.
Контроль качества по дубликатам.
Метод применим для любых биологических материалов, пробы которых можно измерить дважды.
Для проведения контроля пробу перед началом измерения разделяют на два образца, каждый из которых обрабатывается и анализируется самостоятельно. Из полученных данных рассчитывается величина относительного размаха (Ri), которая откладывается на контрольной карте.
Для построения контрольной карты необходимо:
- отбирать 20 проб и провести по 2 параллельных исследования в каждой пробе;
-для каждой пробы рассчитать величину относительного размаха(Ri) между первым значением показателя (Х1) и вторым (Х2) по формуле:
Ri =  ₓ 100%
ₓ 100%
- из полученных 20 значений (R1,2,..20) рассчитать среднее арифметическое значениеR.
- рассчитать контрольные пределы по формуле:
Для 95% границы (R±2σ) – Rx2,46
Для 99% границы (R±3σ) – Rx3,23
- на основании полученных данных строится контрольная карта, где откладывается величина среднего относительного размаха, нулевая точка (граница между двумя измерениями равна «0») и два контрольных предела.
При хорошей воспроизводимости точки будут располагаться равномерно с двух сторон от величины среднего относительного размаха.
Приказ №45 от 07.02.2000 г. «О системе мер по повышению качества клинических лабораторных исследований в учреждениях здравоохранения РФ»
Приказ №220 от 26.05.2003 г. – отраслевой стандарт ОСТ «Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов».
Внутрилабораторный контроль качества обязателен в отношении всех видов количественных исследований, выполняемых в клинико-диагностической лаборатории, для которых разработаны контрольные материалы.
Порядок и технология проведения внутрилабораторного контроля качества измерений лабораторных показателей должны выполняться по правилам настоящего ОСТа.
Допускается использование клинико-диагностической лабораторией компьютерных программ для выполнения внутрилабораторного контроля качества, аттестованных и разрешенных к использованию в клинико-диагностических лабораториях Министерством здравоохранения Российской Федерации.
Отчетные формы проведения внутрилабораторного контроля качества оформляются в виде контрольных карт, таблиц, журналов или на электронных носителях и архивируются на срок не менее 3 лет.
Результаты внутрилабораторного контроля качества должны быть отражены в формах отчетности, которые приведены в Приложениях к данному отраслевому стандарту:
- регистрационная форма "Оценка сходимости результатов измерения" (Приложение 2 к настоящему отраслевому стандарту);
- регистрационная форма "Результаты установочных серий измерений показателя в контрольных материалах" (Приложение 3 к настоящему отраслевому стандарту);
- журнал "Регистрация отбракованных результатов внутрилабораторного контроля качества" (Приложение 4 к настоящему отраслевому стандарту).
Наличие системы внутрилабораторного контроля качества является одним из критериев аккредитации лаборатории и учитывается при лицензировании медицинской деятельности.
Проверка наличия системы внутрилабораторного контроля качества в клинико-диагностических лабораториях осуществляется территориальными органами управления здравоохранением.
Настоящие правила устанавливают средства, способы и порядок проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований, предусматривающие использование контрольных материалов и направленные на выявление недопустимых случайных и систематических погрешностей на аналитическом этапе лабораторного исследования.
Аналитический этап лабораторного исследования включает в себя: хранение и подготовку пробы к измерению, калибровку аналитической системы, измерение лабораторного показателя в аналитической серии, в пробах пациентов и контрольных материалах, оценку приемлемости полученных результатов. Аналитической системой является полная совокупность измерительных приборов и другого оборудования, объединенных для выполнения специальных измерений, которая включает в себя также химические и биологические вещества и другие материалы. Аналитической серией является совокупность измерений лабораторного показателя, выполненных в одних и тех же условиях без перенастройки и калибровки аналитической системы, при которых характеристики аналитической системы остаются стабильными.
Цель проведения внутрилабораторного контроля качества - достижение стабильности аналитической системы.
Контрольные материалы, используемые в клинико-диагностических лабораториях для проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований, должны быть рекомендованы к применению Министерством здравоохранения Российской Федерации.
При внутрилабораторном контроле используются контрольные материалы с аттестованными и неаттестованными значениями контролируемых показателей. Аттестованным значением является значение измеряемой характеристики контрольного материала (концентрации вещества, ферментативной активности и т.п.), установленное при его аттестации и приводимое в паспорте и других документах на контрольный материал. Для одного и того же показателя в документах на контрольный материал может быть указано несколько значений отдельно по каждому методу измерения.
Контрольные материалы с аттестованными значениями показателей используются для контроля правильности и воспроизводимости результатов лабораторного анализа, с неаттестованными значениями - только для контроля воспроизводимости.
Контрольный материал нельзя использовать одновременно в качестве калибровочного материала.
Статистической основой оценки погрешностей при внутрилабораторном контроле качества количественных методов лабораторных исследований является допущение о том, что частотные распределения результатов многократного измерения одного и того же контрольного материала одним и тем же аналитическим методом имеют вид нормального распределения.






