1. Высаливание – разделение на основе различной растворимости альбуминов и глобулинов. Осаждение белков обычно производят сульфатом аммония (NH4)2SO4. В насыщенном растворе этого реактива осаждаются альбумины, а в полунасыщенном – глобулины.
2. Электрофорез – разделение белков при движении в электрическом поле за счет разности их заряда.
Основные белки сыворотки крови делятся на несколько фракций. Быстрее всех движутся к аноду альбумины – это гомогенная фракция. Глобулины делятся на 4 фракции: a1, a2, b, g [рис. альбуминов и 4-х глобулинов и как они движутся к аноду].
В крови определяется общий белок. Нормальное общее содержание белка, но изменено соотношение его фракций – диспротенемия. При инфекционных заболеваниях увеличивается содержание g-глобулиновой фракции. При заболеваниях почек снижается содержание альбуминовой фракции, но увеличивается содержание a2 и b глобулинов. Также наблюдается парапротеинемия – появление патологических белков, например при некоторых онкологических заболеваниях.
III. Проламины и глютелины. Это основные растительные белки. Они не растворяются ни в водных растворах, ни в свободном этаноле, но растворяются в 65% растворе этанола. По АК-составу присутствует глутамин (до 25%), пролин (до 15%). В кукурузе содержится зеин, в ячмене – гордеин, в пшенице – глиадин.
IV. Протеиноиды (склеропротеины). Они не растворяются ни в воде, ни в солевых растворах. Это фибриллярные белки опорных тканей. Входят в состав сухожилий, костной, хрящевой тканей и др. К ним относятся: кератины – белки волос, ногтей; коллагены – белки соединительной ткани; эластины – белки, входящие в состав связок. Особенностью АК-состава является повышенное содержание аланина, глицина, пролина. Имеется оксипролин. Эти белки составляют 25-33% от всех белков в организме.
Характеристика сложных белков
Они имеют белковую и небелковую (простетическую) части. Белковую часть составляет полипептид, построенный из АК-остатков. В состав небелковой части может входить: гем, металл, остаток фосфорной кислоты, углеводы, липиды и т.д.
Хромопротеины
Для них простетическая часть окрашена (chromos – краска). К хромопротеинам относятся гемоглобин, миоглобин, каталаза, пероксидаза, ряд флавинсодержащих ферментов (сукцинатдегидрогеназа, альдегидоксидаза, ксантиноксидаза), цитохромы (гемсодержащие белки) и т.д. Велика биологическая роль этих белков – участвуют в физиологических процессах: дыхание клетки, транспорте кислорода и углекислого газа, окислительно-восстановительных процессах.
Гемоглобин. Его белковая часть представлена глобином, небелковая – гемом. Это олигомерный белок, т.е. имеет четвертичную структуру, состоящую из 4 субъединиц.
a цепи построены из 141 АК-остатка.
b цепи из 146 АК-остатков [рис. 4-х субъединиц, в каждой нарисована точка - гем].
Каждая из субъединиц связана с гемом:
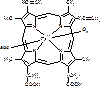 [гем]
[гем]
Основная функция гемоглобина – транспортная (кислород, углекислый газ). Также он представляет собой основную буферную систему крови (75% от всей буферной емкости крови).
Различают:
- HbO2 – оксигемоглобин (связан с молекулой O2);
- HbCO – карбоксигемоглобин;
- HbCO2 – карбгемоглобин;
- HbOH – метгемоглобин (образуется при соединении с нитросоединениями, не способен связывать кислород).
Типы гемоглобина. Всего известно более 100 типов, но их все делят на 2 группы:
1) Физиологические гемоглобины;
2) Патологические (аномальные).
К физиологическим гемоглобинам относятся:
- Hb P – примитивный гемоглобин, имеет место быть у 1-2 недельного эмбриона;
- Hb F – фетальный или гемоглобин плода, к моменту рождения составляет около 70% всего гемоглобина в крови;
- Hb A, Hb A2, Hb A3 – это гемоглобины взрослого организма. На Hb A приходится около 90-96%.
Физиологические типы гемоглобинов отличаются глобулиновой частью (АК-составом). Например Hb A содержит 2a и 2b субъединицы, а Hb F – 2a и 2g субъединицы.
К аномальным (возникающих при наследственных заболеваниях) гемоглобинам относятся:
- HbS – гемоглобин, сопутствующий серповидно-клеточной анемии. Отличается от нормального тем, что с N-конца в 6 положении b–цепи глутамин заменен на валин.
Миоглобин по сравнению с гемоглобином имеет третичную структуру, одну полипептидную цепь, один гем и может связывать одну молекулу кислорода. Гемоглобин и миоглобин функционируют вместе. Гемоглобин доставляет кислород из легких к тканям, а миоглобин перераспределяет его внутри клетки (доставляет к митохондриям).
Оба белка – гемопротеины, т.е. гемсодержащие белки.
Липид-белковые комплексы
Липид-белковые комплексы – сложные белки, простетическую часть которых составляют различные липидные компоненты. К таким компонентам относятся:
1. предельные и непредельные ВЖК. К предельным относятся стеариновая С17Н35СООН и пальмитиновая С15Н31СООН; к непредельным – олеиновая С17Н33СООН, линолевая С17Н31СООН, линоленовая С17Н29СООН и др.;
2. простые и смешанные триацилглицериды. К простым относится трипальмитин, а к смешанным – олеодистеарин:
СН2 - О - СО - С15Н31 СН2 - О - СО - С17Н33
| |
СН - О - СО - С15Н31 СН - О - СО - С17Н35
| |
СН2 - О - СО - С15Н31 СН2 - О - СО - С17Н35
3. фосфолипиды – сложные эфиры глицерина, ВЖК, остатка фосфорной кислоты и гидроксилсодержащего компонента (холин, серин, этаноламин, инозит и др.).
СН2 - О - СО - О - РО2Н - О - С2Н4 - NH2
|
СН - О - СО - С17Н35
|
СН2 - О - СО - С17Н35 [фосфатидилэтаноламин]
4. холестерин (холестерол), его эфиры. В основе холестерина лежит циклопентанпергидрофенантрен.

Связывание белковой и простетической части может осуществляется за счет:
- ионных связей, что характерно для связи фосфолипидов с белковой частью;
- гидрофобных взаимодействий между гидрофобным участком белковой молекулы и более гидрофобным участком простетической части.
Липопротеины. Делятся на:
- свободные липопротеины (ЛП) – хорошо растворимые в воде вещества, транспортные формы (доминируют белки);
- структурные протеолипиды – хорошо растворимые в органических растворителях.
К свободным ЛП относят транспортные ЛП крови. В составе этих частиц могут быть ВЖК, триацилглицерины, фосфолипиды, холестерин, холестериды и др. Наружная часть - p-полярные соединения (гидрофильные): белки, фосфолипиды, холестерин. В центре частицы локализованы холестериды, эфиры ВЖК, триацилглицириды, фосфолипиды [рис. этого]. Все их можно разделить по плотности и по электрофоретической подвижности:
1. хиломикроны (ХМ) – самые крупные и наименее плотные (r <1»0,95 кг/л) частицы. Состоят из 2% белка и 98% липидных компонентов (триглицериды). Образуются в кишечнике. Их количество резко возрастает после приема богатой липидами пищи;
2. ЛП очень низкой плотности (ЛПОНП) – по электрофоретической подвижности эта фракция предшествует b-ЛП (пре-b-ЛП). Их плотность =0,94 – 1,006 кг/л. Содержат повышенное количество белка. Образуются в печени, осуществляют транспорт триглицеридов из нее;
3. ЛП низкой плотности (ЛПНП) – по электрофоретической подвижности b-ЛП. Плотность от 1,006 до 1,06 кг/л;
4. ЛП высокой плотности (ЛПВП) – по электрофоретической подвижности a-ЛП. Плотность от 1,06 до 1,2 кг/л. Содержат примерно 60% белка.
По составу липидов, ЛП низкой и высокой плотности богаты холестерином и фосфолипидами.
Биологическая роль свободных ЛП сводится к транспортным функциям. За счет их гидрофильной оболочки происходит перенос различных веществ в клетки. Также они играют важную роль в диагностике патогенеза.
ЛПНП и ЛПОНП относятся к атерогенным ЛП, т.к. они богаты холестерином и являются крупными частицами, поэтому они застревают в сосудах и вызывают разрастание соединительной ткани.
ЛПВП – это антиатерогены, т.к. транспорт холестерина ими происходит из клеток в ткани.
Структурные липопротеины. Они плохо растворяются в воде, но хорошо в других растворителях. Участвуют в построении биомембран. Содержат 65-85% белка, находящийся в центре частицы и окружен липидами - поэтому их называют протеолипиды. В составе структурных ЛП важную роль играют фосфолипиды. Биологическая роль структурных ЛП заключается в транспорте веществ через клеточные мембраны, передаче нервного импульса и выполнении ими ферментативной функции.
Нуклеопротеины
Нуклеопротеины – это сложные белки, содержащие в качестве небольшой части нуклеиновые кислоты (до 65%).
НП состоят из 2-х частей: белковой (содержит гистоны и протамины, которые являясь основными белками, придают основные свойства) и простетической, представленной НК, сообщающими кислотные свойства. Взаимодействие между этими частями по ион-ионному механизму.
Все НП по составу НК можно разделить на 2 группы: рибонуклеопротеины (РНП) и дезоксирибонуклеопротеины (ДНП).
Состав НК:
НК – высокомолекулярные органические вещества, полинуклеотиды. Мономерами являются мононуклеотиды. Каждый мононуклеотид состоит из: углевода, азотистого основания и фосфорной кислоты. Так, РНК содержит b-D-рибофуранозу (рибозу), одно из 4-х возможных азотистых оснований (А, Г, Ц или У) и остаток фосфорной кислоты. ДНК содержит b-D-дезоксирибофуранозу (дезоксирибозу), одно из 4-х возможных азотистых оснований (А, Г, Ц или Т) и остаток фосфорной кислоты.

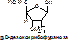
Строение азотистых оснований:
К группе пуриновых относятся аденин (6-аминопурин) и гуанин (2-амино-6-оксипурин). К группе пиримидиновых – урацил (2,4-диоксипиримидин), тимин (5-метилурацил) и цитозин (2-окси-4-аминопиримидин).



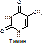

Схема образования нуклеотидов: [рис. схемы: аденин присоединяет рибозу и фосфорную к-ту, при этом выделяются 2 молекулы воды и образуется АМФ]. В клетке имеются нуклеотидфосфаты, дезоксинуклеотидфосфаты, трифосфаты (АТФ).
Структура нуклеиновых кислот:
Имеют несколько уровней структурной организации.
1. первичная структура. РНК и ДНК построены однотипно – представлены полинуклеотидной цепью, состоящей из отдельных мононуклеотодов, соединённых между собой 3’→5’-фосфодиэфирными связями. Эта связь образуется между фосфорным остатком одного мононуклеотида и 3’-ОН-группой пентозного остатка другого мононуклеотида. [рис. образования такой связи] Разные НК отличаются числом, порядком чередования и составом НК.
2. вторичная структура. По рентгеноструктурному анализу ДНК в 1953г Уотсон и Крик предложили модель строения ДНК, которая объясняла самовоспроизведение организмов, наследственную изменчивость. Вторичная структура представляет собой двойную спираль, состоящую из 2 полинуклеотидных цепей, закрученных вокруг одной общей оси. Эти цепи антипараллельны, т.е. одна идет в направлении 5’→3’, а другая 3’→5’. Пуриновому основанию одной цепи соответствует пиримидиновое основание другой цепи – эти основания комплиментарны друг другу, т.е. дополняют одно другое до целого. Между А и Т две водородные связи (А=Т), а между Г и Ц – 3 (ГºЦ).
Молекула спирализована на всем протяжении, гидрофобные участки внутри спирали, их плоскости перпендикулярны основаниям и параллельны друг другу. В вертикальном направлении возникают гидрофобные взаимодействия. Вторичная структура стабилизируется водородными связями и гидрофобными взаимодействиями.
Вторичная структура РНК более простая, представляет собой одну полинуклеотидную цепь, в которой спирализованы лишь некоторые участки. Вторичная структура РНК представлена в виде клеверного листа. Для тРНК известна третичная структура в форме буквы Г. [рис. РНК в виде клеверного листа]
Биологическая роль НК:
ДНК – основная часть её локализуется в ядре в виде ДНП в составе хроматина или хромосом делящихся клеток. Главная роль – хранение генетической информации, участие в процессе транскрипции в качестве матрицы для построения молекулы РНК.
Все РНК по функции делятся на:
- рРНК (рибосомальные), составляют до 80% в составе рибосом. Играют роль каркаса для объединения рибосом белков;
- мРНК (иРНК) – образуется в ядре (ядрышке). Переносит информацию из ядра в цитоплазму, является матрицей в процессе трансляции белка. последний кодон иРНК соответствует последней АК в белке;
- тРНК по своей форме напоминает форму клеверного листа и представляет собой полинуклеотидную цепь, которая составляет 3 петли и отдельные участки могут быть спирализованы. тРНК активирует аминокислоты и транспортирует их к месту биосинтеза белков, также участвует в трансляции. Имеет антикодоновый триплет – место, с помощью которого тРНК связывается с комплиментарным кодоном мРНК.






