Міністерство освіти і науки молоді та спорту
Національний університет “Львівська Політехніка”
Лабораторна робота №18
на тему:
“ Вивчення процесу абсорбції вуглекислого газу розчином лугу ”
з дисципліни:
“Процеси та апарати хімічної технології ”
Виконав:ст.гр. АТПс-11
Вітічак Є.О.
Перевірила: Кіндзера Д.П.
Львів 2013
І. Мета роботи
Визначення коефіцієнту масопередачі К для абсорбції СО2 розчином лугу з повітряної суміші
Теоретичний вступ
Абсорбцією називається процес поглинання газів або парів з газової та парогазової суміші рідкими поглиначами (абсорбентом).
При фізичній абсорбції газ, який поглинається, не взаємодіє хімічно з абсорбентом. Якщо компонентно поглинається утворює з абсорбентом хімічні сполуки, то процес називається хемосорбцією. Фізична абсорбція в більшості випадків є зворотною. Зворотний процес - виділення поглинутого газу з поглинача- називається десорбцією.
В промисловості процеси абсорбції застосовуються для вилучення цінних компонентів з газових сумішей та для очищення цих сумішей від шкідливих домішок.
При абсорбції вміст газу в розчині залежить від властивостей газу або рідини: тиску, температури і складу газової суміші(парціального тиску абсорбтиву).
В багатьох випадках поглинання газу рідиною супроводжується хімічною взаємодією фаз. При протіканні реакції в рідкій фазі частина газоподібного компоненту переходить в зв’язаний стан. При цьому концентрація вільного компоненту в рідині зменшується, що призводить до прискорення процесу абсорбції оскільки збільшується рушійна сила процесу. Швидкість хемосорбції залежить як від швидкості реакції, так і від швидкості масопередачі між фазами. В залежності від того, який процес визначає загальну швидкість процесу переносу маси, розрізняють кінетичну і дифузійну області протікання хемосорбційних процесів.
В кінетичній області швидкість власне хімічної взаємодії менша швидкості масопередачі і тому лімітує швидкість цього процесу.
В дифузійній області лімітує процес хемосорбції швидкість дифузії компонентів в зоні реакції, яка залежить від гідродинаміки та фізичних властивостей фаз. При співрозмірності швидкості реакції і масопередачі процес абсорбції протікає в змішаній (дифузійно-кінетичній) області.
В результаті масообміну між газоподібною і рідкою фазами концентрація компоненту, що поглинається, в газовій фазі змінюється від Уп до Ук, а в рідкій фазі від Хп до Хк. Кількість компоненту, що перейшов з газової фази, складає:
М = G(Уп - Ук).
Рушійною силою процесу абсорбції (мал. І) в будь-якому перерізі абсорбційної колони є різниця між робочою та рівноважнию концентраціями (Уроб- Урівн). Рушійна сила змінюється по висоті абсорбера, тому вводиться поняття середньої рушійної сили по газовій фазі

де 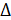 Уб = Уп -Урп;
Уб = Уп -Урп; 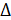 УМ= Ук -Урк.
УМ= Ук -Урк.
Оскільки СО2 добре реагує з розчином NаОН, то концентрація СО2 під поверхнею рідини близька до нуля і можна прийняти:
Урп = 0; Урк = 0
Тоді 

Швидкість процесів абсорбції характеризується рівнянням, якщо рушійну силу 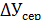 виразити в концентраціях газової фази
виразити в концентраціях газової фази
М=Ку  F
F 
І наступним рівнянням, якщо рушійна сила  виражена в концентраціях рідкої фази
виражена в концентраціях рідкої фази
М=Кх  .
.
В цих рівняннях коефіцієнти масопередачі Ку і Кх визначаються таким чином:
Ку =  і Кх=
і Кх= 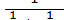
Де  - коефіцієнт масопередачі від потоку газу до поверхні контакту фаз;
- коефіцієнт масопередачі від потоку газу до поверхні контакту фаз;
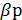 - коефіцієнт масовіддачі від поверхні контакту фаз до потоку рідин;
- коефіцієнт масовіддачі від поверхні контакту фаз до потоку рідин;
 − тангенс кутанахилу рівноважної лінії.
− тангенс кутанахилу рівноважної лінії.
 - мольнамаса суміші;
- мольнамаса суміші;
 - мольна маса СО2;
- мольна маса СО2;
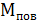 - мольна маса повітря.
- мольна маса повітря.
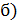 критерій Рейнольдса:
критерій Рейнольдса:
Re = 
d – діаметр газопроводу в місці під’єднаня трубки Піто-Прандля, м
 - в’язкість газової суміші, визначається з рівняння:
- в’язкість газової суміші, визначається з рівняння:
 =
=  +
+  ;
;
В залежності від величини Re знаходиться співвідношення W/Wmax.
в) середня швидкість руху газової суміші
W=  , м/с
, м/с
г) площа поперечного перерізу газопроводу в місці встановлення трубки Піто-Прандля (d  =52
=52  мм).
мм).
д) густина повітря в умовах досліду
 =
=  , кг/м3
, кг/м3
де 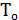 =273
=273  ;
;  = 760 мм рт. ст.
= 760 мм рт. ст.
е) об’ємна витрата СО2
 =
=  , м3/с
, м3/с
є) об’ємна витрата повітря
 , м3/с
, м3/с
ж) об’ємна витрата газової суміші
 , м3/с
, м3/с
з) масова витрата повітря
G=  , кг/с
, кг/с
і) кількість поглинутого СО2
М=  Уп- Ук), кг
Уп- Ук), кг
де Уп, Ук – концентрації СО2 в газовій суміші відповідно на вході (внизу) і на виході (вверху) колони, кг/кг інертного газу.
Перерахунок об’ємної долі СО2 у відносну масову концентрацію
У=  ; кг СО2/кг повітря
; кг СО2/кг повітря
к) середня рушійна сила процесу хемосорбції 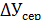 (знаходиться на початку)
(знаходиться на початку)
л) площа поверхні насадки
F=0.785  D2
D2  H
H 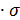 , м2
, м2
де D – діаметр абсорбера, 0.14 м;
H – висота шару насадки, 1.38 м;
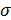 - питома поверхня насадки, 63 м2/м3.
- питома поверхня насадки, 63 м2/м3.
Опис установки
Абсорбер 2, діаметром D  =160
=160 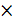 10 мм і висотою 3000 мм наповнений насадкою 2 (кільця Решига 50
10 мм і висотою 3000 мм наповнений насадкою 2 (кільця Решига 50 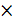 50
50 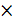 7 мм). Висота насадкового шару 1380 мм. Розчин
7 мм). Висота насадкового шару 1380 мм. Розчин
NаОН (7 %) за допомогою поспи 8 попадає зі збірника в верхню частину абсорбера. Кількість рідини фіксується ротаметром 3. Стікаючи по насадці, рідина зливається назад в збірник. Газ, що абсорбується (СО2), з балону 7 дроселюється редукційним вентилем 5. Витрата газу визначається по ротаметру 4. Газ змішується з повітрям, що подається в систему вентилятором 9. Кількість газової суміші, що подається в абсорбер, визначається трубкою Піто-Прантля ІІ, яка приєднана до мікроманометра 10. Витрата рідкої та газової фаз регулюється запірно-регулюючою арматурою 6. Вентилі 12 використовуються для відбирання проб газу з нижньої та верхньої частини абсорбера.

Методика проведення роботи
Включають помпу 8 і за допомогою вентилів 6 встановлюють по ротаметру 3 задану витрату рідини. Після цього включають вентилятор 9 та вентилем 6 встановлюють необхідну витрату повітря. Редукційним вентилем 5 в лінію подачі повітря дроселюють з балону 7 вуглекислий газ. Через 3-5 хв відбирають проби газової суміші в верхній та нижній частинах абсорбера. Відбирання проб проводиться відкриванням вентилів 12. Концентрація СО2 в газовій суміші визначається за допомогою газоаналізатора.
Обробка дослідних даних
Обробка дослідних даних зводиться до визначення коефіцієнту масо передачі К:
К= 
Для цього необхідно визначити:
а) максимальну швидкість руху газової суміші, м/с
 , м/с
, м/с
де g =9.81 м2/с – прискорення вільного падіння;
H – покази манометра;
K – поправочний коефіцієнт мікроманометра;
 - питома густина рідини мікроманометрі, кг/м3;
- питома густина рідини мікроманометрі, кг/м3;
 - густина газової суміші при температурі досліду, кг/м3;
- густина газової суміші при температурі досліду, кг/м3;
б) густина газової суміші
 , кг/ м3;
, кг/ м3;
де  =760 мм рт. ст.;
=760 мм рт. ст.;
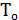 =273
=273  .
.
Приклад. Скруббер для поглинання парів ацетону з повітря скраплюється водою в кількості 3000 кг/год. Середня температура в скрубері 20 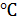 . Через скруббер пропускається під атмосферним тиском суміш повітря з парами ацетону, яка містить 6% (об.) ацетону. Чистого повітря в цій суміші – 1400 м3/год (за нормальних умов). В скруббері вловлюється 98 % ацетону.
. Через скруббер пропускається під атмосферним тиском суміш повітря з парами ацетону, яка містить 6% (об.) ацетону. Чистого повітря в цій суміші – 1400 м3/год (за нормальних умов). В скруббері вловлюється 98 % ацетону.
Урівнювання лінії рівноваги:
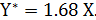
Тут Х і  виражені в кіломолях ацетону на 1 кмоль іншого компоненту (води чи повітря).
виражені в кіломолях ацетону на 1 кмоль іншого компоненту (води чи повітря).
Знайти діаметр і висоту скруббера, заповненого керамічними кільцями, розміром 25 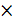 25
25 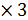 мм. Швидкість газу приймати на 25 % менше швидкості захлинання.
мм. Швидкість газу приймати на 25 % менше швидкості захлинання.
Коефіцієнт масопередачі Ку = 0.4 кмоль ацетону/(м2 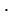 год
год  Коефіцієнт змоченості насадки приймати рівним одиниці.
Коефіцієнт змоченості насадки приймати рівним одиниці.
Розв’язання. Кількість поглиненого ацетону:
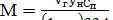 =
=  кмоль/год,
кмоль/год,
де  =0.98 – ступінь поглинання.
=0.98 – ступінь поглинання.
Початкова концентрація ацетону в воді, яка подається на верх скруббера, Хв=0. Кінцева концентрація ацетону в воді, яка витікає внизу з скруббера:
 =
= 
Початкова концентрація ацетону в повітрі внизу при вході в скруббер:


Кінцева концентрація ацетону в повітрі, яке виходить з скруббера:
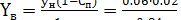 =0.00128
=0.00128 
По цих точках на діаграмі Y-X нанесена робоча лінія; нище проведена рівноважна лінія по зрівнюванню 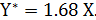
Знаходимо рухому силу абсорбції внизу скруббера:

Значення  знаходимо по урівнюванню рівноважної лінії для Хв, відповідного низу скруббера:
знаходимо по урівнюванню рівноважної лінії для Хв, відповідного низу скруббера:
 1.68
1.68 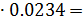 0.0393
0.0393 
Рухома сила абсорбції на верху скруббера:

Середня рухома сила:


Потрібну поверхню масопередачі знаходимо по урівнюванню:

Об’єм шару керамічних кілець, необхідний для створення знайденої поверхні, при  :
:
V= 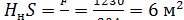
де 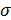 =204 м2/м3 – питома поверхня насадки.
=204 м2/м3 – питома поверхня насадки.
Уточнимо перетин скруббера.
По урінюванню вираховуємо фіктивну швидкість газу в точці інверсії, нехтуючи невеликим вмістом ацетону в рідині і газі.
Значення входящих в урівнювання величин:
L= 3000 кг/год;  ;
;
G=1400 
 ;
;
L/G=3000/1810=1.66; 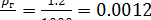 ;
;
 м3/м3.
м3/м3.
Підставляємо ці значення в формулу:
lg(
або lg 0.0616  ,
,
звідки 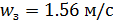 .
.
За умовою беремо робочу фіктивну швидкість газу 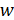 на 25 % менше:
на 25 % менше:
 .
.
Площа поперечного перерізу скруббера:

Звідси діаметр скруббера:

Необхідна висота насадки: