Белки, их структура и биологические функции. Ферменты.
Все химические вещества делят на две группы: органические и неорганические.
Неорганические вещества: вода, минеральные соли и кислоты.
Органические вещества – это соединения углерода, которые возникли в живых организмах или являются продуктами их жизнедеятельности.
Органические вещества составляют в среднем 20-30% массы клетки живых организмов.
Органические вещества: белки, липиды, углеводы и нуклеиновые кислоты.
Молекулы этих веществ имеют очень большую молекулярную массу, состав их молекул входят тысячи, десятки тысяч или даже миллионы атомов, поэтому их называют макромолекулами (биополимерами).
Биополимеры состоят из одинаковых или схожих звеньев – мономеров, которые последовательно связаны между собой ковалентной связью.
Если обозначить тип мономера определенной буквой, например А, то полимер можно изобразить в виде очень длинного сочетания мономерных звеньев: А—А—А—А—...—А. Если соединить два типа мономеров А и Б, можно получить очень большой набор разнообразных полимеров, например Б Б А Б Б А Б Б А Б Б... Т.об. мономеры служат строительным материалом для полимеров.
| Мономеры белков — аминокислоты, |
| нуклеиновых кислот — нуклеотиды, |
| сложных углеводов — моносахариды. |
Большинство липидов образуются из глицерина и жирных кислот, но их будет рассмотрен отдельно. Помимо образования макромолекул малые биологические молекулы выполняют и различные специальные функции.
Ряд органических веществ относится к биологически активным веществам: гормоны, пигменты, витамины и т.д. Они влияют на процессы обмена веществ и преобразование энергии, осуществляют гормональную регуляцию процессов жизнедеятельности организма.
Среди органических веществ белки занимают первое место, как по количеству, так и по значению. У животных на них приходится около 50% сухой массы клетки.
Белки – это высокомолекулярные азотосодержащие биополимеры, мономерами которых являются остатки аминокислот.
Название «белки» происходит от способности многих из них при нагревании становится белыми.
Белки обладают большой молекулярной массой: яичный альбумин — 36 000, гемоглобин — 152 000, миозин — 500 000. Для сравнения: молекулярная масса спирта — 46, уксусной кислоты — 60, бензола — 78.
Если белки состоят только из аминокислот, их называют простыми (протеины).
Если белки содержат помимо аминокислот еще и небелковый компонент, их называют сложными (протеиды). Небелковый компонент может быть углеводом (гликопротеиды), липидами (липопротеиды), нуклеиновыми кислотами (нуклеопротеиды).
Аминокислотный состав белков
Чем выше уровень организации живых существ, тем разнообразнее состав белков. В организме человека встречается около 5 млн типов белков. Но несмотря на такое разнообразие, обычно белки построены всего из 20 различных аминокислот, а огромное разнообразие белков обеспечивается различными комбинациями этих аминокислот.
М ономерами белков являются α-аминокислоты.
Все аминокислоты содержат:
1) карбоксильную группу (– СООН) – обеспечивает кислотные свойства,
2) аминогруппу (– NH2) – обеспечивает основные свойства,
3) радикал или R -группу (остальная часть молекулы). У разных аминокислот радикалы отличаются.
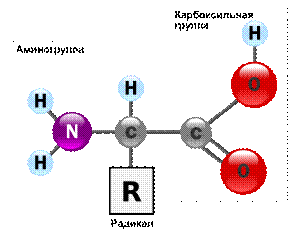
Строение радикала у разных видов аминокислот — различное. В зависимости от количества аминогрупп и карбоксильных групп, входящих в состав аминокислот, различают: нейтральные аминокислоты, имеющие одну карбоксильную группу и одну аминогруппу; основные аминокислоты, имеющие более одной аминогруппы; кислые аминокислоты, имеющие более одной карбоксильной группы.
Аминокислоты являются амфотерными соединениями, так как в растворе они могут выступать как в роли кислот, так и оснований. В водных растворах аминокислоты существуют в разных ионных формах.
В зависимости от того, могут ли аминокислоты синтезироваться в организме человека и других животных, различают:
• заменимые аминокислоты — могут синтезироваться;
• незаменимые аминокислоты— не могут синтезироваться.
Незаменимые аминокислоты должны поступать в организм вместе с пищей. Незаменимые аминокислоты, которые не синтезируются человеческим организмом.
Для разных видов животных и людей разного возраста набор незаменимых аминокислот неодинаковый, например аргинин и гистидин заменимы для взрослых и незаменимы для детей.
Белки, которые содержат все незаменимые аминокислоты, называют полноценными. Неполноценные белки – белки, в состав которых не входят некоторые незаменимые кислоты.
Недостаток незаменимых аминокислот вызывает такие проблемы, как:
· нарушение обмена веществ (организм начинает потреблять аминокислоты из белков соединительной ткани, мышц, крови и печени, ведь поддерживать нормальную работу сердца и мозга – наиболее важных органов, в итоге - истощение),
· в детском возрасте – задержка роста и развития,
· потерю массы тела,
· снижение иммунитета и депрессии.
· При занятиях спортом недостаток незаменимых аминокислот резко увеличивает риск травм и снижает спортивные результаты.
Незаменимые кислоты содержатся в следующих продуктах:
· Валин – в зерновых, грибах, мясе, молочных продуктах, сое, арахисе.
· Изолейцин – в орехах кешью и миндале, курином мясе и яйцах, рыбе, печени, мясе, ржи, чечевице, сое и в большинстве семян.
· Лейцин – в мясе и рыбе, орехах, чечевице, буром рисе и также в большинстве семян.
· Лизин – в рыбе, мясе, молоке и молочных продуктах, пшенице и орехах.
· Метионин – в молоке, рыбе, яйцах, мясе, бобовых.
· Треонин – в яйцах и молочных продуктах.
· Триптофан – в мясе, бананах, финиках, кунжуте, арахисе, овсе.
· Фенилаланин – в говядине, курице, рыбе, яйцах, сое, молоке и твороге.
Норма потребления белка в сутки составляет 1,5 г на 1 кг веса. При больших физических нагрузках норма возрастает. До недавнего времени считалось, что норма потребления белка - 150 г ежедневно, сегодня официально признанная норма - 30-45 г.
• Что происходит с мясом, если поместить его в теплую влажную среду?
Оно начинает гнить. В организме человека точно также накапливаются продукты гниения, которые необходимо нейтрализовать. С помощью специальных реакций.
Потребление избыточного количества белка вызывает интоксикацию организма - отравление продуктами распада белков. Существует легенда, что в древнем Китае применялся вид казни, когда преступника кормили исключительно вареным мясом. Через пару месяцев почки прекращали справляться с выведением продуктов белкового распада, вследствие чего наступало отравление организма.
Вегетарианцы – не едят мяса.
Веганы – строгие вегетарианцы, они не приемлют насилия над животными. Не едят мясо, рыбу, молоко, масло, сыр, яйца, не используют кожу, шерсть и мех.
Растения синтезируют все виды аминокислот. Чтобы получить полный набор незаменимых аминокислот из растительных продуктов, желательно сочетать злаки, бобовые, орехи, овощи и фрукты.
Строение белков
Остатки аминокислот в составе белков соединяются между собой пептидной связью: между карбоксильной группой одной аминокислоты и аминогруппой другой.

При взаимодействии двух аминокислот образуется дипептид.
Полипептиды – структуры, которые состоят из 20-50 остатков аминокислот. На одном конце пептида находится свободная аминогруппа (его называют N-концом), а на другом — свободная карбоксильная группа (его называют С-концом).
Белки это полипептиды с высокой молекулярной массой, содержат свыше 50 аминокислотных остатков.

Уровни структурной организации белков
Известно четыре уровня структурной организации белков: первичная структура, вторичная, третичная и четвертичная.
Первичная
Это последовательность аминокислот в полипептидной цепи. Определяется качественным и количественным составом аминокислот.
Замена всего лишь одной аминокислоты на другую в полипептидной цепочке приводит к изменению свойств и функций белка. Например, замена в β-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к тому, что молекула гемоглобина в целом не может выполнять свою основную функцию — транспорт кислорода; в таких случаях у человека развивается заболевание — серповидноклеточная анемия.
Вторичная
Это пространственное расположение полипептидной цепи.
Чаще всего полипептидная цепь полностью или частично закручивается в спираль. Радикалы аминокислот находятся с внешней стороны спирали, внутри спирали находятся амино- и карбоксильная группа. Стабилизация витка происходит благодаря водородным связям, возникающим между карбоксильной и аминогруппой. Водородные связи гораздо слабее пептидных.
Третичная
Обусловлена способностью полипептидной спирали закручиваться в клубок (глобулу), благодаря дисульфидным связям. Поддержание третичной структуры обеспечивают дисульфидные связи, гидрофобные взаимодействия и ионные связи.
При этом белок скручивается так, что гидрофобные боковые цепи погружены вглубь молекулы и защищают ее от взаимодействия с водой, а снаружи расположены боковые гидрофилбные цепи.
Третичную структуру имеют большинство белков. Для каждого вида белка характерна своя форма клубка с изгибами и петлями.
4) Четвертичная
Образуется когда объединятся несколько глобул. Субъединицы удерживаются в молекуле благодаря ионным, гидрофобным и электростатическим взаимодействиям. Например молекула гемоглобина состоит из четырех остатков молекул белка миоглобина.
Свойства белков
Свойства белков обусловлены их аминокислотным составом и пространственной структурой.
По способности растворяться в воде белки подразделяются на глобулярные (растворимые) и фибриллярные (нерастворимые).
• Что происходит при варке яиц с белком?
Денатурация – это процесс нарушения природной структуры белка, который сопровождается разворачиванием белковой молекулы без нарушения первичной структуры.
Денатурацию могут вызвать нагревание, ультрафиолетовое излучение, тяжелые металлы и их соли, изменения рН, радиация, обезвоживание.
Причиной денатурации является разрыв связей, стабилизирующих определенную структуру белка. Первоначально рвутся наиболее слабые связи, а при ужесточении условий и более сильные. Поэтому сначала утрачивается четвертичная, затем третичная и вторичная структуры. Изменение пространственной конфигурации приводит к изменению свойств белка и, как следствие, делает невозможным выполнение белком свойственных ему биологических функций.
Чаще всего денатурация необратима, но бывает иногда возможна ренатурация - процесс восстановления структуры белка после денатурации (в таком случае это была обратимая денатурация).
Если восстановление пространственной конфигурации белка невозможно, то денатурация называется необратимой.
Деструкция – необратимый процесс разрушения первичной структуры.
Функции белков
| Функция | Примеры и пояснения |
| Строительная | Белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), волос (кератин), сухожилий (коллаген) и т.д. |
| Транспортная | Белок крови гемоглобин присоединяет кислород и транспортирует его от легких ко всем тканям и органам, а от них в легкие переносит углекислый газ; в состав клеточных мембран входят особые белки, которые обеспечивают активный и строго избирательный перенос некоторых веществ и ионов из клетки во внешнюю среду и обратно. |
| Регуляторная | Гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например, гормон инсулин регулирует уровень глюкозы в крови, способствует синтезу гликогена, увеличивает образование жиров из углеводов. |
| Защитная | В ответ на проникновение в организм чужеродных белков или микроорганизмов (антигенов) образуются особые белки — антитела, способные связывать и обезвреживать их. Фибрин, образующийся из фибриногена, способствует остановке кровотечений. |
| Двигательная | Сократительные белки актин и миозин обеспечивают сокращение мышц у многоклеточных животных. |
| Сигнальная | В поверхностную мембрану клетки встроены молекулы белков (рецепторы), способных изменять свою третичную структуру в ответ на действие факторов внешней среды, таким образом осуществляя прием сигналов из внешней среды и передачу команд в клетку. |
| Запасающая | В организме животных белки, как правило, не запасаются, исключение: альбумин яиц, казеин молока. Но благодаря белкам в организме могут откладываться про запас некоторые вещества, например, при распаде гемоглобина железо не выводится из организма, а сохраняется, образуя комплекс с белком ферритином. |
| Энергетическая | При распаде 1г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов — воды, углекислого газа и аммиака. Однако в качестве источника энергии белки используются только тогда, когда другие источники (углеводы и жиры) израсходованы. |
| Каталитическая | Одна из важнейших функций белков. Обеспечивается белками — ферментами, которые ускоряют биохимические реакции, происходящие в клетках. |
| Функция антифриза | В плазме крови некоторых живых организмов содержатся белки которые предупреждают ее замерзание в условиях низких температур. |






