В переважній більшості випадків остеопороз у дитячому віці вторинний. Він розвивається як ускладнення ендокринної, хронічної соматичної, автоімунної та алергічної, онкогематологічної патологій, а також є наслідком ятрогенних впливів – медикаментозної терапії, що спричинила втрату кісткової маси.
В дитячому віці частіше спостерігається перший ступінь формування остеопорозу – остеопенія, тобто зниження кісткової маси. Остеопенічний синдром у дітей може бути проявом критичних вікових змін фізичного розвитку. Він реєструється у 2,5 – 30,0 % дітей у дошкільному та молодшому шкільному віці та у 40,0 – 45,0 % у підлітковому і найчастіше пов’язаний із сколіозами, віковими ендокринопатіями, вегето-судинними дистоніями, патологією шлунково-кишкового тракту тощо. Порушення процесів кісткоутворення у дитини може відбуватися внаслідок неправильного харчування, недостатньої фізичної активності, порушень метаболічних процесів та інших факторів.
У формуванні остеопенічного синдрому важливу роль відіграють такі гормони, як паратиреоїдний гормон, кальцитонін, вітамін-D-гормональна система, гормони щитоподібної, підшлункової, статевих залоз, наднирників та деякі інші. Порушенням метаболізму цих гормонів відводиться суттєве місце в патогенезі патології кісткового обміну за вторинного остеопорозу. Остеопенічний синдром супроводжується також змінами обміну макро- та мікроелементів, амінокислотно-білкового обміну та інших ланок гомеостазу.
Проживання в йододефіцитних регіонах, у тих, які потерпіли від аварії на ЧАЕС, також є суттєвими факторами ризику розвитку остеопенічного синдрому у дітей та інволютивного остеопорозу.
 Дуже важливим показником повноцінності формування кісткової маси є так званий «пік кісткової маси» (ПКМ) – максимальна кількість кісткової тканини, накопиченої в процесі формування скелету. Близько 85 % піку кісткової маси людина в нормі набирає ще під час пубертатного періоду, причому її рівень генетично детермінований і визначає міцність кістки протягом усього подальшого життя людини.
Дуже важливим показником повноцінності формування кісткової маси є так званий «пік кісткової маси» (ПКМ) – максимальна кількість кісткової тканини, накопиченої в процесі формування скелету. Близько 85 % піку кісткової маси людина в нормі набирає ще під час пубертатного періоду, причому її рівень генетично детермінований і визначає міцність кістки протягом усього подальшого життя людини.
Кісткова тканина містить органічні та неорганічні компоненти. Органічні речовини (матрикс кісткової тканини) представлені в основному білками та ліпідами, неорганічні – в основному солями фосфату кальцію. Неорганічні (мінеральні) компоненти становлять 65 % маси кісткової тканини, вони визначаються як у компактній, так і в трабекулярній (губчастій) її частинах. Органічні та неорганічні компоненти в поєднанні один з одним утворюють дуже міцну структуру, що має здатність чинити опір розтягненню, стисненню тощо. Крім цього, кісткова тканина є своєрідним депо і забезпечує організм кальцієм, фосфором, натрієм та іншими іонами, необхідними для підтримки гомеостазу.
Основним структурним компонентом кісткової тканини є кальцій, оскільки саме він забезпечує її постійне поновлення та формування пікової кісткової маси у дітей. Загальна кількість кальцію в організмі зростає від 25 г у новонародженого до 1,5 кг у дорослої людини. Однак надходження кальцію в кістки не зводиться до простого його накопичення. Кісткова тканина ніколи не перебуває в стані метаболічного спокою. Структурна цілісність скелету людини підтримується безперервним процесом перебудови (ремоделювання). Швидкість ремоделювання кісткової тканини становить 2 – 10% на рік.

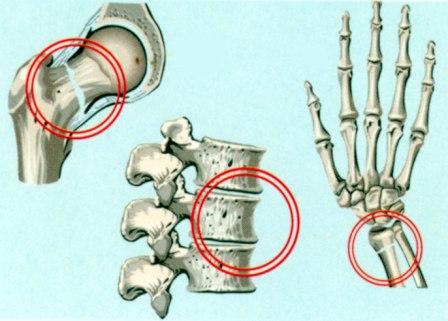
Рис.1. Рентгенограма поперекового відділу хребта (бокова проекція) хворого на системний остеопороз: відзначається зниження рентгенологічної щільності тіл хребців (остеопенія), склероз субхондральних пластинок і вдавлені переломи в їх центральних відділах (показані стрілками).
Особливо інтенсивний метаболізм кальцію у дітей. У підлітковому періоді повністю оновлюється кісткова тканина скелета кожні 1-2 роки.
Гомеостаз кальцію в організмі перебуває під жорстким багаторівневим контролем, насамперед – гормональним, чим досягається оптимальний баланс між кальцієм, що надходить в організм, тією кількістю, що всмоктується в кишечнику, та співвідношенням його рівнів у плазмі крові і кістковій тканині й виведенням кальцію з організму. Кісткова тканина досить вразлива до недостатнього надходження кальцію в організм. Дефіцит кальцію незмінно веде до його недостатнього вмісту в кістковій тканині. В міру дорослішання дитини щоденна потреба в даному елементі суттєво зростає, досягаючи максимуму в підлітковому віці (коли відбувається накопичення піка кісткової маси). В подальшому кількість кальцію знижується до рівня, що відповідає показнику дорослої людини.
На резорбцію кістки впливають три основні гормони – паратиреоїдний, кальцитріол (метаболіт вітаміну D) та кальцитонін. Основна функція паратиреоїдного гормону – це підтримка в організмі гомеостазу кальцію. Крім того, на процеси резорбції, гальмуючи їх, впливають статеві гормони (естрогени у жінок та тестостерон у чоловіків). Зниження рівня статевих гормонів у пубертатному періоді (наприклад, у разі вродженого гіпогонадизму) та підвищення рівня пролактину негативно впливають на формування кісткової тканини.
 Значну роль у процесах кісткового метаболізму відіграють глюкокортикоїди, впливаючи на синтез статевих гормонів на всіх рівнях. Тиреоїдні гормони також впливають на процеси остеосинтезу та резорбції: в разі гіпертиреозу спостерігається зменшення мінеральної щільності кісток, збільшення втрат кальцію та фосфору з сечею.
Значну роль у процесах кісткового метаболізму відіграють глюкокортикоїди, впливаючи на синтез статевих гормонів на всіх рівнях. Тиреоїдні гормони також впливають на процеси остеосинтезу та резорбції: в разі гіпертиреозу спостерігається зменшення мінеральної щільності кісток, збільшення втрат кальцію та фосфору з сечею.
Важливими факторами формування щільності кісток у дитячому віці є зріст дитини та фізична активність, яка сприяє посиленій мінералізації кісток. Динаміка мінеральної насиченості кісток залежить від статі – у дівчаток вона зростає більш інтенсивно, починаючи з 10, а у хлопців – з 13 років.
У дорослих мінеральний склад кісткової тканини визначається дією низки факторів: спадковості, дієтичних звичок, рухової активності, гормонального статусу тощо. Вже з віку 30-35 років починається втрата кісткової тканини, яка є універсальним феноменом біології людини. Середня втрата кісткової маси у жінки становить приблизно 1 % на рік щодо рівня піку маси кісткової тканини в репродуктивному віці. Прискорення темпів цього процесу спостерігається в перші 5 років менопаузи.
Провідну роль у порушеннях кісткового обміну у разі постменопаузального остеопорозу відіграє стресовий гормональний дисбаланс. Інволюційний остеопороз розвивається поступово, прояви його характерних симптомів сягають максимуму через 10-15 років після початку захворювання.
Основні клінічні ознаки первинного остеопорозу такі: біль у кістках, найчастіше – в поперековому чи грудному відділі хребта, повільне зменшення зросту, зміна постави, прогресуюче обмеження рухової активності хребта, втрата маси тіла. Переломи – це пізні та найбільш яскраві прояви остеопорозу. Особливо трагічними є переломи шийки стегна, смертність за яких сягає 20-25 % протягом перших 6 місяців, а тяжка інвалідизація загрожує 40-45 % таких хворих.
Враховуючи масштаб і соціально-економічну значимість проблеми, експертами ВООЗ розроблена глобальна стратегія з профілактики остеопорозу, важливе місце в якій відводиться ранній діагностиці.
 «Золотим стандартом» діагностики остеопорозу експертами ВООЗ визнана двоенергетична рентгенівська денситометрія, яка використовується з цією метою з 1994 року. Метод має високу чутливість і специфічність, точність та низьку похибку відтворення, мінімальну дозу опромінення, відзначається швидкістю обстеження, можливістю дослідження осьового та периферичного скелету, оцінку співвідношення жирової та м’язової тканини.
«Золотим стандартом» діагностики остеопорозу експертами ВООЗ визнана двоенергетична рентгенівська денситометрія, яка використовується з цією метою з 1994 року. Метод має високу чутливість і специфічність, точність та низьку похибку відтворення, мінімальну дозу опромінення, відзначається швидкістю обстеження, можливістю дослідження осьового та периферичного скелету, оцінку співвідношення жирової та м’язової тканини.
Діагностика остеопенічного синдрому в педіатричній практиці має свої особливості. Сучасні денситометри обов’язково враховують не тільки паспортний, а й кістковий вік дитини, масу й довжину її тіла, стадію пубертата тощо. Питання про найбільш безпечний для застосування в педіатрії метод денситометрії без втрат для його точності, чутливості, відтворення більшістю дослідників вирішується на користь рентгенівської денситометрії. Проте в сучасних наукових дослідженнях, так само, як і в клінічній практиці, для дослідження структурно-функціонального стану кісткової тканини (щільність, еластичність та міцність кістки), ступеня остеопенії чи остеопорозу все частіше віддається перевага ультразвуковій денситометрії.
Нині ультразвукова денситометрія (ультрасонометрія) є загальноприйнятим методом оцінки кісткової тканини, який клінічно не поступається аксіальній рентгеноденситометрії.
На початок 1999 року в усьому світі налічувалося близько 5000 типів ультрасонометрів, якими здійснюють вимірювання трабекулярної кісткової тканини в п’ятковій кістці. Інші 1000 приладів використовують для вимірювання компактних кісток (великогомілкової кістки, передпліччя, фаланги пальця).
 Основні переваги ультразвукової денситометрії наступні. Ультразвукова оцінка проводиться неінвазивним шляхом; пацієнт не зазнає іонізуючого опромінення і тому не уникає участі в дослідженні; ультразвукова апаратура дешевша, порівняно з приладами для рентгенівської денситометрії; сучасні ультразвукові пристрої компактні та портативні; метод забезпечує велику точність отримуваних результатів; швидкий час сканування (5 хв); заслуговує на увагу також легкість в обслуговуванні апаратури тощо. Під час обстеження дітей ці переваги особливо суттєві, адже вони виключають побоювання батьків щодо рентгенівського опромінювання, а також не викликають спротиву чи будь-якого дискомфорту в дитини.
Основні переваги ультразвукової денситометрії наступні. Ультразвукова оцінка проводиться неінвазивним шляхом; пацієнт не зазнає іонізуючого опромінення і тому не уникає участі в дослідженні; ультразвукова апаратура дешевша, порівняно з приладами для рентгенівської денситометрії; сучасні ультразвукові пристрої компактні та портативні; метод забезпечує велику точність отримуваних результатів; швидкий час сканування (5 хв); заслуговує на увагу також легкість в обслуговуванні апаратури тощо. Під час обстеження дітей ці переваги особливо суттєві, адже вони виключають побоювання батьків щодо рентгенівського опромінювання, а також не викликають спротиву чи будь-якого дискомфорту в дитини.
Ультразвукова денситометрія має переваги також у разі обстеження жінок у менопаузі, оскільки на тлі дефіциту естрогенів первинно вражаються трабекулярні кості. Об’єктом дослідження, зазвичай, слугує п’яткова кістка. В Україні ця методика успішно застосовується з середини 90-х років минулого століття.
Вищенаведені дослідження є, безперечно, найбільш надійними сучасними маркерами стану кісткової системи. Водночас під час встановлення діагнозу первинного чи вторинного остеопорозу враховуються також дані анамнезу, оцінюються фактори ризику, клінічні прояви, результати загальноклінічних методів обстеження, зокрема показники фосфорно-кальцієвого обміну, аналіз маркерів кісткового метаболізму (кальцій/креатинін сечі; гідроксипролін/креатинін сечі; піридолін і дезоксипролін сечі).
 Глобальна стратегія ВООЗ передбачає, на підставі застосування надійних методів діагностики та вивчення особливостей клініки остеопорозу, розробку дієвих методів профілактики та лікування, починаючи з антенатального періоду і аж до похилого віку.
Глобальна стратегія ВООЗ передбачає, на підставі застосування надійних методів діагностики та вивчення особливостей клініки остеопорозу, розробку дієвих методів профілактики та лікування, починаючи з антенатального періоду і аж до похилого віку.
Доведено, що клінічні прояви й лабораторні показники остеопенії у дітей раннього та підліткового віку значно відрізняються. Причини остеопорозу в дітей першого року життя переважної більшості випадків пов’язані з дефіцитом кальцію у вагітної, а надалі – матері, що годує дитину груддю.
Лише з 3 років життя відповідальними за вміст кальцію в організмі дитини переважно є характер її харчування, рухова активність та вітамінотерапія. В період посиленного росту (від 3 до 5 років) особливо велике значення має збалансований прийом кальцію та вітаміну D. Недостатнє споживання кальцію в перші 30 років життя підвищує удвічі ризик розвитку остеопорозу та патологічних переломів.
Переважна більшість учених і лікарів-практиків у всьому світі вважають основою лікування остеопорозу будь-якого генезу раціональне харчування і фізичну активність пацієнта, відмову від шкідливих звичок. Тільки в разі дотримання цих умов фармакологічна корекція буде ефективною.
Між іншим, популяційні дослідження показали, що близько 60 % людей споживають недостатню кількість кальцію.
Деякі вітчизняні вчені вважають, що надходження необхідної кількості кальцію з продуктами харчування має переваги порівняно з фармакологічними засобами. Норми добового споживання кальцію в різні вікові періоди коливаються від 1000 до 1600 мг. Основним джерелом кальцію є молочні продукти: твердий сир (від 600 до 1000 мг кальцію в 100 г), плавлені сири (300 мг), нежирне молоко (120 мг), йогурт. Крім того, значну кількість кальцію містять горіхи, особливо лісові (290 мг в 100 г), деякі овочі, наприклад, селера (240 мг), риба з кістками (залежно від способу її приготування кількість кальцію коливається від 3000 до 350 мг). Необхідно зазначити, що збереження кісткової маси – завдання значно легше, ніж її відновлення. В зв’язку з цим особливого значення набуває профілактика остеопорозу, яку слід здійснювати протягом усього життя. В цьому разі потрібно приділяти серйозну увагу формуванню пікової маси кісткової тканини, а також попередженню вікового дефіциту мінерального складу кісток. Оскільки генетичні детермінанти кісткової тканини зумовлені наперед, основну увагу слід приділити середовищним факторам, періоду росту кісток у дитячому та юнацькому віці, вагітності, лактації та періоду перименопаузи.






