Термохимические уравнения
Химические уравнения, в которых указан тепловой эффект называются термохимическими уравнениями.
1/2H2(г) + 1/2Cl2(г) = HCl(г) DH = -92 кДж (*)
Zn(к) + H2SO4(р) = ZnSO4(р) + Н2(г) DН = -163.2 кДж
1) Знак теплового эффекта - если тепло выделяется, внутренняя энергия системы уменьшается (-), для эндотермических процессов (+).
2) При написании термохимических уравнений необходимо указывать агрегатное состояние вещества, поскольку переход из одного агрегатного состояния в другое также сопровождается тепловым эффектом. Пишем либо (г), (ж), (тв), либо газ - формула берется в круглые скобки (Cl2), жидкость не обозначается, твердые вещества в квадратных скобках [Zn].
3) DH зависит от количества вещества, поэтому важно уравнивать реакции, при этом коэффициенты могут быть дробными. Уравнение (*) можно записать и так (H2) + (Cl2) = 2(HCl), но тогда DH’ = 2DH.
4) DН зависит от условий - от температуры и давления. Поэтому обычно приводятся стандартные значения DНo
Cтандартные условия - p = 1 атм (101 кПа), температура 25оС (298 К) - отличие от нормальных условий.
Энтальпия
Энтальпия системы (от греч. enthalpo нагреваю) – это однозначная функция H состояния термодинамической системы при независимых параметрах энтропии S и давлении P, которая связана с внутренней энергией U соотношением
|
где V – объем системы.
В химии чаще всего рассматривают изобарические процессы (P = const), и тепловой эффект в этом случае называют изменением энтальпии системы или энтальпией процесса:
|
| (4.1) |
Энтальпия имеет размерность энергии (кДж). Ее величина пропорциональна количеству вещества; энтальпия единицы количества вещества (моль) измеряется в кДж∙моль–1.
В термодинамической системе выделяющуюся теплоту химического процесса условились считать отрицательной (экзотермический процесс, Δ H < 0), а поглощение системой теплоты соответствует эндотермическому процессу, Δ H > 0.
Уравнения химических реакций с указанием энтальпии процесса называют термохимическими. Численные значения энтальпии Δ H указывают через запятую в кДж и относят ко всей реакции с учетом стехиометрических коэффициентов всех реагирующих веществ. Поскольку реагирующие вещества могут находиться в разных агрегатных состояниях, то оно указывается нижним правым индексом в скобках: (т) – твердое, (к) – кристаллическое, (ж) – жидкое, (г) – газообразное, (р) – растворенное. Например, при взаимодействии газообразных H2 и Cl2 образуются два моля газообразного HCl. Термохимическое уравнение записывается так:

|
При взаимодействии газообразных H2 и O2 образующаяся H2O может находиться в трех агрегатных состояниях, что скажется на изменении энтальпии:

|

|
Приведенные энтальпии образования веществ и энтальпии реакций отнесены к стандартным условиям (P = 101,325 кПа) и взяты для температуры T = 298 K. Стандартное состояние термодинамической функции, например, энтальпии, обозначается нижним и верхним индексами:  нижний индекс обычно опускают: Δ
нижний индекс обычно опускают: Δ 
Закон Гесса
Пользуясь табличными значениями 
 и
и  , можно рассчитать энтальпии различных химических процессов и фазовых превращений. Основанием для таких расчетов является закон Гесса, сформулированный петербургским профессором Г. И. Гессом (1841 г.): «Тепловой эффект (энтальпия) процесса зависит только от начального и конечного состояния и не зависит от пути перехода его из одного состояния в другое».
, можно рассчитать энтальпии различных химических процессов и фазовых превращений. Основанием для таких расчетов является закон Гесса, сформулированный петербургским профессором Г. И. Гессом (1841 г.): «Тепловой эффект (энтальпия) процесса зависит только от начального и конечного состояния и не зависит от пути перехода его из одного состояния в другое».
Анализ закона Гесса позволяет сформулировать следующие следствия:
1. Энтальпия реакции равна разности сумм энтальпий образования конечных и начальных участников реакций с учетом их стехиометрических коэффициентов.
| Δ H = ΣΔ H обр.конечн – ΣΔ H обр.нач |
2. Энтальпия реакции равна разности сумм энтальпий сгорания начальных и конечных реагентов с учетом их стехиометрических коэффициентов.
| Δ H = ΣΔ H сгор.нач – ΣΔ H сгор.конечн |
3. Энтальпия реакции равна разности сумм энергий связей E св исходных и конечных реагентов с учетом их стехиометрических коэффициентов.
В ходе химической реакции энергия затрачивается на разрушение связей в исходных веществах (Σ E исх) и выделяется при образованиии продуктов реакции (–Σ E прод). Отсюда
| Δ H ° = Σ E исх – Σ E прод |
Следовательно, экзотермический эффект реакции свидетельствует о том, что образуются соединения с более прочными связями, чем исходные. В случае эндотермической реакции, наоборот, прочнее исходные вещества.
При определении энтальпии реакции по энергиям связей уравнение реакции пишут с помощью структурных формул для удобства определения числа и характера связей.
4. Энтальпия реакции образования вещества равна энтальпии реакции разложения его до исходных веществ с обратным знаком.
| Δ H обр = –Δ H разл |
5. Энтальпия гидратации равна разности энтальпий растворения безводной соли  и кристаллогидрата
и кристаллогидрата 
Из вышесказанного видно, что закон Гесса позволяет обращаться с термохимическими уравнениями как с алгебраическими, т. е. складывать и вычитать их, если термодинамические функции относятся к одинаковым условиям.
Теплоемкость. Газовые смеси
При расчетах тепловых устройств очень важным моментом является определение количества теплоты, участвующего в процессах. Точное его определение обеспечивает правильную оценку работы аппарата с технической и экономической точки зрения.
Сообщение телу теплоты вызывает изменение его состояния и в общем случае сопровождается изменением температуры. Было замечено, что для нагрева до одной и той же температуры двух различных тел одинаковой массы и в одинаковых условиях требуется различное количество теплоты. Следовательно, существует какое-то свойство тела, определяющее изменение его температуры в процессе подвода или отвода теплоты. Это свойство называют теплоемкостью тела. Таким образом, теплоемкость тела – это величина, характеризующая способность тела изменять свою температуру с подводом или отводом теплоты. Она равна количеству теплоты, которое надо подвести к телу, чтобы изменить его температуру на 1 К:
 ,
,  Дж / К,
Дж / К,
в дифференциальной форме, т. е. при подводе элементарного количества тепла:
 . (1)
. (1)
Теплоемкость тела в общем случае не является характеристикой вещества (материала), из которого тело состоит. Она, в частности, будет зависеть от размеров тела. В зависимости от того, в каких единицах измеряется количество вещества – в килограммах, кубометрах, киломолях, различают:
- массовую (удельную) теплоемкость:
 ,
,
т.е. теплоемкость одного килограмма вещества;
- объемную теплоемкость:
 ,
,
т.е. теплоемкость одного кубометра вещества;
- мольную теплоемкость:
 ,
,
т.е. теплоемкость одного киломоля вещества.
Очевидная связь между этими величинами имеет вид:
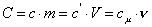 .
.
Например, массовую теплоемкость через объемную можно определить следующим образом:
 .
.
Однако и эти величины еще не являются характеристиками вещества. Процесс нагревания или охлаждения может происходить в различных условиях: р = const, V = const, T = const, а также многих других. Значения теплоемкостей одного и того же вещества в разных процессах также будут различными. В частности, в соответствии с (1) теплоемкость в процессе при постоянной температуре оказывается бесконечно большой. В связи с этим теплоемкость называют функцией процесса.







