Раздел 3. Основы теории сплавов и диаграммы их состояния
Лекция 6
- Основные типы диаграмм состояния.
- Правило отрезков.
Правило Курнакова
Основные типы диаграмм состояния.
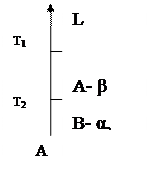
Вид диаграммы определяется характером взаимодействий, которые возникают между компонентами в жидком и твердом состояниях. Однокомпонентная диаграмма представляет собой температурную шкалу с нанесенными на нее точками фазовых превращений:
 |
Двухкомпонентная диаграмма помимо температурной оси (оси ординат), имеет ось концентраций (ось абсцисс). Один конец оси абсцисс соответствует чистому компоненту А, другой – В. Промежуточные точки соответствуют сплавам с различным соотношением компонентов.
Трехкомпонентные диаграммы имеют вид трехгранной равносторонней призмы, в основании которой лежит концентрационный треугольник, а ребра являются температурными осями.
Рассмотрим наиболее типичные двухкомпонентные диаграммы:
1 типа. Для сплавов, образующих при затвердевании механическую смесь. Их компоненты в твердом состоянии нерастворимы, и не образуют химических соединений.
2 типа. Для сплавов с полной взаимной растворимостью, как в жидком, так и в твердом состоянии.
3 типа. Для сплавов с ограниченной растворимостью в твердом состоянии.
4 типа. Для сплавов с устойчивым химическим соединением.
Диаграмма 1 типа.
Компоненты: вещества А и В. Фазы: жидкий раствор L, кристаллы А и кристаллы В. Максимальное значение фаз – 3.
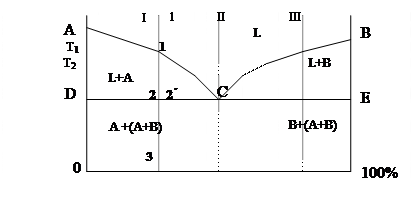
АСВ – ликвидус. DСЕ – солидус. При охлаждении по АС начинают выделяться кристаллы А, по СВ – кристаллы В. На линии DСЕ из жидкости концентрации С одновременно выделяются кристаллы А и В, образуя эвтектику. DСЕ – линия эвтектических превращений.
Ниже линии АС область двухфазная. Здесь существуют одновременно жидкий раствор L и твердая фаза – кристаллы А.
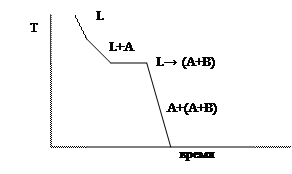
Рассмотрим кривую охлаждения для сплава I. В точке 1 – начало кристаллизации сплава. На кривой охлаждения наблюдается перегиб. В процессе кристаллизации состав жидкости будет меняться по линии АС. В т.2 жидкость будет иметь концентрацию точки С. При этой температуре из жидкости одновременно выделяются кристаллы А и В, образуя механическую смесь – эвтектику (А+В), т.е. образуются двухфазные кристаллы. Этот процесс изотермический и происходит по линии DСЕ, кот. называется линией эвтектических превращений. С – тройная точка: при данной температуре и данном составе в системе существует 3 фазы: L, А, В. Кривая охлаждения для сплава I:
 |
Сплав 1 – доэвтектический. Структура: А + эвтектика (А+В)
Сплав 2 – эвтектический. Структура: эвтектика (А+В)
Сплав 3 – заэвтектический. Структура В + эвтектика (А + В).
Диаграмма 2 типа.
Компоненты А и В. Фазы: L, α..
Если два компонента неограниченно растворяются в жидком и твердом состояниях, то возможно существование только двух фаз – жидкого раствора L и твердого раствора α. Трех фаз быть не может. Кристаллизация при постоянной температуре не наблюдается и горизонтальной линии на диаграмме нет.
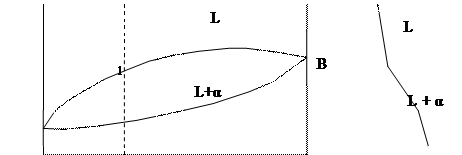 |
Диаграмма состояния 3 типа.
Компоненты А, В. Фазы: L, α., β.
В сплавах такого рода возможно существование жидкой фазы L, твердого раствора компонента В в А - α.- твердый раствор и твердого раствора компонента А в В – β-твердый раствор. В таких сплавах возможно нонвариантное равновесие при одновременном существовании трех фаз: L, α., β. В этой системе не образуется фазы, представляющей собой чистые компоненты. Из жидкости могут выделяться только твердые растворы α. и β.
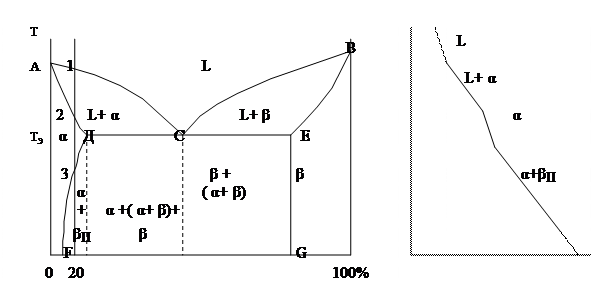
Около вертикалей А и В находятся области существования твердых растворов α. и β.
Предельная растворимость В в А определяется линией DF, а предельная растворимость А в В линией ЕG. Сплавы, находящиеся между этими двумя линиями находятся за пределами растворимости и являются двухфазными, состоящими из
α. + β. Линия АСВ является на этой диаграмме линией ликвидуса, АDСЕВ – солидуса. Линия DСЕ – линия эвтектических превращений, С- тройная точка.
Рассмотрим кристаллизацию сплава 1. Выше т.1 сплав находится в жидком состоянии. В т.1 – начинается выделение кристаллов твердого раствора α.. В т.2 – кристаллизация заканчивается. Эти кристаллы не претерпевают изменений до т.3. Ниже т.3 твердый раствор α является пересыщенным и выделяет избыточные кристаллы – βII -твердого раствора, которые называются вторичными. Сплав, концентрация которого лежит левее DF, не будет иметь вторичных выделений.
Линия ЕG, в отличие от линии DF, изображена вертикальной, т.е. растворимость А в В не зависит от температуры. Поэтому вторичных α2- кристаллов нет.
Построение кривых охлаждения
1. Провести вертикаль через данный состав сплава (например, для сплава 1: 20%В и 80%А).
2. Отметить точки пересечения вертикали с линиями диаграммы (1,2,3,4)
3. Сделать горизонтальную проекцию на ось температур.
4. Построить кривые охлаждения, учитывая фазовые превращения. При простом охлаждении процесс идет быстро. При фазовых превращениях охлаждение сплавов замедляется и меняется наклон кривой. При кристаллизации эвтектики на кривой наблюдается горизонтальный участок.






