Провоторов В.М., Будневский А.В., Семенкова Г.Г., Семынина Н.М., Гречушкина И.В., Малыш Е.Ю.
ОСОБЕННОСТИ КЛИНИЧЕСКОГО ТЕЧЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ У КУРЯЩИХ ПАЦИЕНТОВ МОЛОДОГО ВОЗРАСТА
Воронежская государственная медицинская академия им. Н.Н. Бурденко
Актуальность. Распространенность бронхиальной астмы (БА) в России среди детей составляет от 5,6 до 12,1%, а среди взрослых – 5,6–7,3% [5, 6]. Рост распространенности данного заболевания неуклонно увеличивается [5, 6]. В развитых странах на лечение БА затрачивается от 1 до 2% всего бюджета здравоохранения [5, 6]. Традиционная тактика ведения больных БА не приводит к существенному сокращению частоты обострений, увеличения продолжительности жизни больных, что может быть связано с большой распространенностью курения среди пациентов. Изучение особенностей течения БА у курящих больных необходимо для оптимизации лечения этих пациентов, что позволит снизить уровень инвалидизации и смертности от астмы.
Цель исследования. Изучение влияния курения на клиническое течение бронхиальной астмы у лиц молодого возраста и качество их жизни.
Материалы и методы исследования. Было обследовано 120 пациентов, из них 64 мужчины (53,3%) и 56 женщин (46,7%), в возрасте 27,0 (21,5; 34,0) лет, находившихся на лечении в пульмонологическом отделении БУЗ ВО «Воронежская городская клиническая больница скорой медицинской помощи №1», с ноября 2007 по май 2009 г. с клиникой смешанной БА средней тяжести. Из 120 обследованных больных БА 88 курящих составили основную группу и 32 некурящих – контрольную группу.
Со всеми пациентами проводилось комплексное клинико-лабораторное и инструментальное обследование, включающее физикальный осмотр, сбор анамнеза, исследование клеточного состава мокроты, запись электрокардиограммы, рентгенографию органов грудной клетки, пикфлоуметрию, спирометрию с пробой с бронхолитиком («Беротеком», Boeringer ingelheim, Австрия), а также иммунологических методов (определение уровня фактора некроза опухоли-α (ФНО-α), интерлейкина 4 (ИЛ-4), интерлейкина 8 (ИЛ-8)). Обследование проводилось с целью уточнения диагноза БА, а также для исключения синдромно сходных с БА заболеваний. Диагноз БА устанавливался согласно рекомендациям, изложенным в GINA, 2008 [6].
Спирометрию осуществляли с использованием спироанализатора «Диамант» (ООО «Алекс Медика», Россия). Проводили измерение следующих показателей функции внешнего дыхания (ФВД): жизненная емкость легких (ЖЕЛ), форсированная жизненная емкость легких (ФЖЕЛ), объем форсированного выдоха за первую секунду (ОФВ1), ОФВ1 / ФЖЕЛ, пиковая объемная скорость выдоха (ПОСвыд), максимальная объёмная скорость при выдохе 25-75 % ЖЕЛ (МОС25, МОС50, МОС75), прироста ОФВ1 после ингаляции β2-агониста «Беротека». За должные принимали величины, рекомендованные Клементом Р.Ф. (1993) [6]. Пиковую скорость выдоха (ПСВ) определяли при помощи пикфлоуметра (фирма "Аэромед", Россия). Исследование индуцированной мокроты проводили после ингаляции аэрозоля 4,5%-го раствора натрия хлорида с помощью ультразвукового распылителя «Муссон-2» в гемоцитометре. Исследование цитокинового профиля в периферической крови пациентов проводили методом иммуноферментного анализа с тест системами ЗАО «Вектор-Бест» (Новосибирск).
Критерии включения в исследование: БА средней тяжести частично контролируемая, возраст от 18 до 35 лет, способность больного выполнять определенные процедуры, связанные с исследованием.
Критерии исключения из исследования: тяжелая БА, наличие сопутствующих заболеваний, сопровождающихся выраженной дыхательной и сердечной недостаточностью, сопутствующие заболевания органов дыхания (рак, туберкулез, хроническая обструктивная болезнь легких, пневмония, пороки развития легких и др.).
По данным анамнеза у курящих пациентов, страдающих БА, вычисляли индекс курящего человека (ИКЧ), выражаемый числом пачка-лет, который вычисляли по следующей формуле:
ИКЧ = (число сигарет, выкуриваемых в сутки)*(количество лет курения)/20 [3].
Для исследования влияния курения на течение БА у лиц молодого возраста и их качество жизни было произведено сравнение следующих параметров основной и контрольной групп:
а) клинических симптомов - числа дневных, ночных симптомов астмы, потребности в β2-агонистах короткого действия по данным дневников самоконтроля, уровня контроля БА по данным Аsthma Control Test (АСТ) [2], выраженности одышки по Borg [1], кашля по визуальной аналоговой шкале (ВАШ) [1], количеству обострений и длительности обострений БА за год;
б) данных спирометрии и пикфлоуметрии, клеточного состава мокроты, а также уровня провоспалительных цитокинов – ФНО-α, ИЛ-4, ИЛ-8 в периферической крови.
в) показателей качества жизни по данным опросника «SF-36v2TM Health Status Survey» [4].
Статистический анализ полученных данных осуществляли с использованием непараметрических методов. Для численных параметров в пределах исследуемых групп рассчитывали медиану, 25 и 75 процентили. Для определения различий между исследуемыми группами использовали критерий Манна-Уитни. При сравнении двух повторных измерений использовали критерий Вилкоксона. Различия считали достоверными при уровне значимости р<0,05. Для статистической обработки результатов исследования был использован пакет прикладных программ STATISTICA 7.0 (StatSoft Inc.) для персонального компьютера в системе Windows.
Результаты собственного исследования. У курящих больных БА (основная группа), по сравнению с некурящими (контрольная группа), отмечалось статистически значимо большее среднее количество дневных симптомов БА в сутки, среднее количество ночных симптомов БА в неделю, средняя суточная потребность в бронхолитиках короткого действия, среднее количество и длительность обострений БА в год, более выражен кашель по ВАШ, одышка по Borg, ниже уровень контроля над астмой по данным АСТ.
В мокроте пациентов основной группы было обнаружено достоверно большее количество нейтрофилов и меньшее количество эозинофилов по сравнению с пациентами контрольной группы. В крови пациентов основной группы отмечалось более высокое содержание ИЛ-4, ИЛ-8 и ФНО-α по сравнению с пациентами контрольной группы (см. табл. 1).
Таблица 1. Клиническая характеристика больных основной и контрольной групп

Примечания: $ - статистически значимое отличие показателей основной группы от соответствующих показателей контрольной группы при р < 0,05; * - статистически значимое отличие показателей основной группы от соответствующих показателей контрольной группы при р < 0,01
Были установлены прямые положительные корреляционные связи средней силы между показателями ИЛ-4 и ИЛ-8 (r=0,70, p=0,001), ИЛ-4 и ФНО-α (r=0,52, p=0,027), ИЛ-8 и ФНО-? (r=0,65, p=0,003). Также прямая положительная корреляционная связь средней силы была обнаружена между содержанием нейтрофилов в мокроте больных БА и уровнем ФНО-α в периферической крови (r=0,57, р=0,009) и отрицательная – между количеством эозинофилов в мокроте и содержанием ФНО-α в крови (r=0,47, р=0,005). Установлена прямая положительная корреляционная связь между ИКЧ и самооценкой кашля по ВАШ (r=0,25, р=0,016), одышки по Borg (r=0,59, р=0,018), количеством обострений на 1 пациента в год (r=0,35, р=0,037), количеством дней обострения БА на 1 пациента в год (r=0,29, р=0,006).
У курящих пациентов были зарегистрированы статистически значимо более низкие значения показателей ФВД и пикфлоуметрии по сравнению с соответствующими показателями некурящих: ЖЕЛ, ФЖЕЛ, ОФВ1, ПОСвыд, утренних значений ПСВ. У курящих больных БА отмечался больший прирост ОФВ1 после пробы с бронхолитиком («Беротеком») и суточная вариабельность ПСВ. Значения отношения ОФВ1/ФЖЕЛ (индекса Тиффно), МОС25, МОС50, МОС75 достоверно не отличались в исследуемых группах (см. табл. 2).
Пациенты контрольной группы продемонстрировали статистически значимо более высокие показатели качества жизни по сравнению с пациентами основной группы по следующим критериям: «физическая активность», «роль физических проблем в ограничении жизнедеятельности», «телесная боль», «общее восприятие здоровья», «социальная активность», «роль эмоциональных проблем в ограничении жизнедеятельности» (см. табл. 3).
Таблица 2. Исходные показатели ФВД и пикфлоуметрии больных основной и контрольной групп

Примечания: # - статистически значимое отличие показателей основной группы от соответствующих показателей контрольной группы при р<0,05; * - статистически значимое отличие показателей основной группы от соответствующих показателей контрольной группы при р<0,01
Таблица 3. Показатели КЖ больных основной и контрольной групп по данным опросника «SF-36v2TM Health Status Survey»
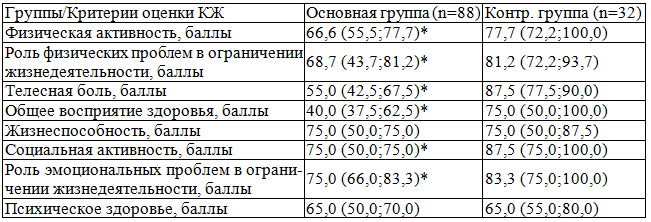
Примечание: * - статистически значимое отличие показателей основной группы от соответствующих показателей контрольной группы при р<0,01
Обсуждение результатов. На основании вышеперечисленных данных собственного исследования можно предположить, что, по сравнению с некурящими, у курящих больных БА, более выражен воспалительный процесс в дыхательных путях, о чем свидетельствует большая частота симптомов астмы, выраженность кашля по ВАШ, более низкий уровень контроля по данным АСТ, большее количество нейтрофилов в мокроте у курящих, большая вариабельность ПСВ, более высокое содержание провоспалительных цитокинов (ИЛ-4, ИЛ-8, ФНО-α) в крови у курящих. Более низкие показатели ФВД (ЖЕЛ, ФЖЕЛ, ОФВ1) и ПСВ, а также большая выраженность одышки по Borg, полученные при обследовании курящих по сравнению с некурящими, могут свидетельствовать о большей выраженности процесса ремоделирования бронхов у курильщиков, что, в конечном счете, может привести к необратимой под влиянием лечения тяжелой бронхиальной обструкции и инвалидизации больных. Таким образом, курение утяжеляет течение и ухудшает прогноз БА у лиц молодого возраста, что отражается в более низком качестве жизни курящих пациентов.
Выводы:
- Курение утяжеляет клиническое течение бронхиальной астмы у пациентов молодого возраста.
- Курение приводит к снижению качества жизни больных бронхиальной астмой по следующим компонентам: «физическая активность», «роль физических проблем в ограничении жизнедеятельности», «телесная боль», «общее восприятие здоровья», «социальная активность», «роль эмоциональных проблем в ограничении жизнедеятельности».
- Установленное отрицательное влияние курения на течение бронхиальной астмы требует настойчиво добиваться отказа от курения пациентов, страдающих бронхиальной астмой.
- Существует необходимость изменения стереотипа ведения курящих больных бронхиальной астмой: больше внимания уделять выработке мотивации к отказу от курения у пациентов и лечению табачной и никотиновой зависимости.
Список использованных источников:
1. Авдеев С.Н. Диспноэ: механизмы, оценка, терапия// Consilium medicum. – 2004. – Т. 6, № 4. – С. 23-27.
2. Белевский А.С. Тест контроля астмы - "новая игрушка" или важный инструмент// Пульмонология и аллергология. –2005. – № 1. – С. 33-34.
3. Комплексное лечение табачной зависимости и профилактика хронической обструктивной болезни легких, вызванной курением табака. Метод. рекомендации. № 2002/154. - М: МЗ РФ, 2003. - 48 с.
4. Руководство по исследованию качества жизни в медицине/ А.А. Новик, Т.И. Ионова. – СПб.; М., 2002.– 320 с.
5. Пульмонология: учеб. пособие/ М.А. Осадчук и др. – М.: Медицина, 2010. – 296 с. 6. GINA Report, Global Strategy for Asthma Management and Prevention. - 2008. - http://www.ginasthma.org.






