КИНЕТИЧЕСКИЕ ОСОБЕННОСТИ ИОННОЙ ПОЛИМЕРИЗАЦИИ
При ионной полимеризации скорость процесса описывается различными уравнениями для каждой системы «мономер–инициатор–растворитель».
Скорость ионной полимеризации складывается из скоростей четырех стадий: инициирования v И, роста цепи v Р, обрыва v О и передачи цепи v ПЕР. Упрощенные уравнения скоростей элементарных стадий имеют вид:
| 1) Инициирования | 
| 
|
| 2) Роста | 
| 
|
| 3) Обрыва | 
| 
|
| 4) Передачи | 
| 
|
Если при радикальной полимеризации протекают минимум 3 из этих реакций (1, 2 и 3), то ионная полимеризация часто реализуется благодаря только двум (1 и 2) или трем (1, 2 и 4) реакциям. Такие процессы называют безобрывными.
При протекании ионной полимеризации с медленным инициированием и обрывом кинетика процесса во многом совпадает с кинетикой радикальной полимеризации. Тут также возможны квазистационарные условия, когда скорость инициирования равна скорости обрыва  . В этих условиях, если концентрация мономера входит в уравнение скорости инициирования,
. В этих условиях, если концентрация мономера входит в уравнение скорости инициирования,

Следовательно, стационарная концентрация активных центров равна

Суммарная скорость процесса, т.е. скорость расходования мономера, определяется скоростью роста цепи. Тогда, подставляя в уравнение для скорости роста цепи значение концентрации активных центров, получаем уравнение для скорости ионной полимеризации, выраженной через начальные концентрации мономера и катализатора:

Это уравнение не является универсальным, так как не учитывается влияние природы среды, температуры и других факторов, которые оказывают влияние на состав активного центра и на характер всех протекающих в системе реакций.
Средняя степень полимеризации, а значит, и молекулярная масса полимера, будет зависеть от скоростей роста, обрыва и передачи цепи:

Подставляя значения скоростей элементарных стадий, получаем:
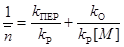
Из уравнения видно, что средняя степень полимеризации не зависит от концентрации инициатора. Если скорость реакции передачи цепи намного выше скорости реакции обрыва ( ), то молекулярная масса практически не зависит от концентрации мономера. Наоборот, если скорость реакции обрыва цепи существенно больше скорости реакции передачи цепи (
), то молекулярная масса практически не зависит от концентрации мономера. Наоборот, если скорость реакции обрыва цепи существенно больше скорости реакции передачи цепи ( ), то молекулярная масса пропорциональна концентрации мономера.
), то молекулярная масса пропорциональна концентрации мономера.
КАТИОННАЯ ПОЛИМЕРИЗАЦИЯ
Общие сведения
Катионная полимеризация – это цепная полимеризация, в которой носителями кинетической цепи являются катионы, т.е. растущая частица несет положительный заряд.
Под действием инициаторов катионного типа полимеризуются циклические соединения (циклопропан, циклические простые эфиры, циклические формали) и ненасыщенные соединения, имеющие избыточную электронную плотность на двойной связи, т.е. соединения с электронодонорными заместителями у a-углеродного атома. Этим методом полимеризуются стирол, a-метилстирол, изобутилен, формальдегид, пропиленоксид, эпихлоргидрин и др.
Инициаторами катионной полимеризации могут быть соединения, способные к ионизации на катион и анион:
1. Протонные кислоты (HClO4, H2SO4, H3PO4, СF3COOH и др.)
2. Апротонные кислоты (кислоты Льюиса) общей формулы MeX n, где Me – металл, X – галоген (BF3, BCl3, AlCl3, SbCl5, TiCl4, SnCl4, AlBr3, ZnCl2 и др.).
3. Ониевые соли RO3+X–, NR4+X–.
4. Галогены I2, ICl, IBr.
5. Алкилпроизводные металлов R3Al, R2Zn.
Одними из наиболее активных инициаторов являются апротонные кислоты. Порядок активности апротонных кислот зависит от природы мономера и может меняться с изменением условий реакции (Т, р, полярность среды). Для типичного мономера катионной полимеризации – изобутилена – активности инициаторов этой группы снижается в ряду:
BF3 > AlBr3 > TiCl4 > TiBr4 > SnCl4 > BCl3 > BBr3
Для инициирования катионной полимеризации апротонными кислотами кроме инициатора необходимо присутствие очень малых количеств другого ионогенного вещества – соинициатора (промотора). Это могут быть вода, галогенводородные кислоты типа НХ, спирты. Образующиеся при взаимодействии инициатора и промотора комплексные соединения проявляют свойства сильной кислоты и способны отщеплять протоны:





Экспериментального доказательства существования ионных форм комплексов типа  нет, и их часто изображают как
нет, и их часто изображают как  .
.
Механизм катионной полимеризации
Рассмотрим основные стадии катионной полимеризации (стадия инициирования, роста цепи и ограничения роста цепи).
Инициирование
В зависимости от структуры первичных частиц можно выделить несколько типов инициирования:
- свободными катионами K+;
- ионными парами [K+A-];
- цвиттерионами [K+—A-];
- катион-радикалами  ;
;
- координационными комплексами, не имеющими ярко выраженного ионного характера.
Наиболее распространено инициирование свободными катионами и ионными парами.
В качестве примера рассмотрим полимеризацию изобутилена в присутствии  .
.
На стадии инициирования комплексная кислота  отдает свой протон молекуле мономера с образованием карбониевого мономерного иона:
отдает свой протон молекуле мономера с образованием карбониевого мономерного иона:

Присоединение протона к мономеру происходит по месту наибольшей электронной плотности в молекуле (в соответствии с правилом Морковникова водород присоединяется к наиболее гидрогенизированному атому углерода).
Поскольку процесс ионной полимеризации проходит чаще всего в среде с низкой диэлектрической проницаемостью, то карбкатион существует в виде ионной пары.
Рост цепи
Рост цепи представляет собой процесс внедрения очередной молекулы мономера между катионом и противоионом:


Реакция роста цепи состоит из множества элементарных актов последовательного присоединения молекул мономера к растущему макрокатиону с регенерацией ионной пары в каждом элементарном акте. В этом случае обеспечивается регулярное присоединение звеньев мономера по типу «голова к хвосту».
Ограничение роста цепи
Ограничение роста цепи может произойти при взаимодействии активного центра с противоионом, мономером, растворителем, полимером.
1. Реакции с противоионом с перестройкой ионной пары и регенерацией иницирующего комплекса:

2. Соинициатор может реагировать с растущей цепью с образованием ковалентной связи с захватом фрагмента противоиона. Реакция сопровождается регенерацией инициатора:

Эта реакция проходит с обрывом как кинетической, так и материальной цепи.
3. Передача цепи на мономер:

Материальная цепь при этом обрывается, а кинетическая – нет. Интенсивность протекания этой реакции в большинстве случаев определяет молекулярную массу полимера.
Относительная скорость передачи цепи на мономер растет с увеличением кислотности инициатора (BF3 < FeCl3 < SnCl4 < TiCl4) и снижается с увеличением полярности среды.
В общем случае, несмотря на большую скорость катионной полимеризации по сравнению с радикальной, длина макромолекул, образующихся в катионных процессах, оказывается меньше, чем в радикальных, что в большой степени определяется интенсивностью протекания реакции передачи цепи на мономер.
4. Передача цепи на полимер может идти с разрывом молекулы и без него. В результате передачи цепи на полимер с разрывом макромолекул от основной цепи отщепляются небольшие осколки, дающие новые центры полимеризации (это приводит к расширению ММР). Передача цепи без разрыва макромолекул приводит к получению разветвленных полимеров.
Скорость и характер реакций ограничения роста цепи определяется активностью растущего катиона и стабильностьюпротивоиона. При оптимальном сочетании этих величин ограничения роста цепи не происходит, и полимеризация идет по механизму «живых» цепей.






