В колбу емкостью 200 мл наливают 100 мл 0,4-0,6 % раствора иодида калия и 5 мл 2-4 Н раствора серной кислоты. Колбу ставят на магнитную мешалку и включают ее. Из бюретки добавляют 0,5 мл 0,05 Н раствора тиосульфата натрия, 15-20 капель 0,5 % раствора крахмала. Добавляют 10 мл 0,05 Н раствора Н2О2 и, одновременно, включают секундомер.
Выделяющийся в результате реакции (2) иод взаимодействует с добавленным тиосульфатом, и смесь остается бесцветной. После того, как количество иода, эквивалентное введенному количеству тиосульфата натрия, будет израсходовано, смесь окрасится в синий цвет в результате появления в реакционной смеси свободного иода.
Не останавливая секундомер, записывают время появления окраски и тотчас добавляют 0,5 мл раствора тиосульфата натрия.
Подобным образом поступают каждый раз, когда появляется окраска. В связи с тем, что скорость реакции во времени уменьшается, после появления окраски в 8-й - 10-й раз раствор тиосульфата натрия добавляют по 0,25 мл.
Получаемые результаты заносят в таблицу:
| Cуммарный объем добавлен. р-ра тиосульфата Na (мл) | ... | |||
| Время от начала реакции до появления окраски, (мин, с). | ... |
Работу заканчивают тогда, когда при добавлении 0,25 мл раствора тиосульфата натрия окраска не появляется свыше 30 мин.
Полученные результаты обрабатывают следующим образом:
1. Строят график в координатах V(Na2S2O3)(мл) (ордината) - t (мин) (абсцисса).
2. Методом экстраполяции находят величину  (см. примечание);
(см. примечание);
3. Рассчитывают 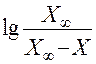 , строят график в координатах
, строят график в координатах
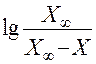 (ордината), t(абсцисса), и графически определяют константу скорости реакции.
(ордината), t(абсцисса), и графически определяют константу скорости реакции.
Примечание: предельный объем раствора тиосульфата натрия можно найти прямым титрованием после подогрева до 50 - 70 градусов Цельсия содержимого реакционного сосуда для ускорения реакции.
Вопросы для самоподготовки и контроля:
1. От каких факторов зависит скорость химической реакции и константа реакции?
2. Какая реакция является элементарной?
3. Что определяет молекулярность реакции?
4. Можно ли говорить о молекулярности сложной реакции?
5. Сформулируйте закон действия масс для элементарной и сложной реакции.
6. Напишите уравнения реакций, изучаемых в данной работе.
7. Какая из реакций является лимитирующей и почему она называется псевдомономолекулярной?
8. Напишите формулу для вычисления константы скорости реакции 1-го порядка.
9. Как находится предельный объем тиосульфата?
10. Какова размерность константы реакции первого порядка?
11. Дайте определение понятия "порядок реакции".
12. Напишите выражение для скорости лимитирующей (самой медленной) реакции.




