Национальный исследовательский технологический университет
«МИСиС»
НОВОТРОИЦКИЙ ФИЛИАЛ
Кафедра металлургических технологий и оборудования
Домашнее задание
по дисциплине «Теплотехника»
Вариант
Выполнил: студент гр.
Проверил: Куницина Н.Г.
Новотроицк, 2016
Для случая сжигания смешанного газа с теплотой сгорания 11 МДж/м3 определить расход воздуха, состав и количество продуктов сгорания, калориметрическую температуру горения при коэффициенте расхода (избытка) воздуха n=1,05. Температура подогрева воздуха 400 ˚ С. Топливо не подогревается. Составить материальный баланс процесса горения.
Состав топлива А, %: СО=3, Н2=12, СН4=58, С2H4=27. Влажность топлива А WА=14 г/м3.
Состав топлива Б, %: СО2=1, СО=32,5, Н2=0,5, N2=66. Влажность топлива Б WБ=22 г/м3.
Выполним пересчет каждого топлива с сухой массы на влажную, используя формулы:
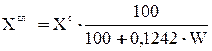 ;
;
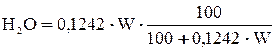 ,
,
где 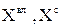 – содержание компонента топлива соответственно во влажной и сухой массе, %;
– содержание компонента топлива соответственно во влажной и сухой массе, %;
W – влажность топлива, г/м3;
H2О – количество воды во влажной массе топлива, %.
Для топлива А:
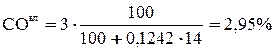 ;
;
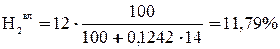 ;
;
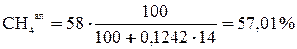 ;
;
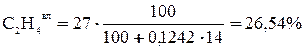 ;
;
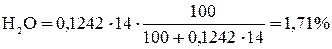 .
.
Проверяем правильность расчета, складывая все компоненты топлива А:
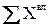 =2,95 +11,79 + 57,01 +26,54 +1,71= 100 %.
=2,95 +11,79 + 57,01 +26,54 +1,71= 100 %.
Для топлива Б:
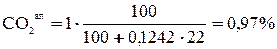 ;
;
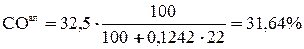 ;
;
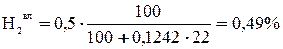 ;
;
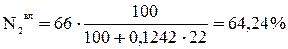 ;
;
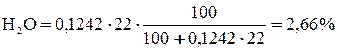 .
.
Проверяем правильность расчета, складывая все компоненты топлива Б:
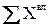 =0,97 +31,64 +0,49 +64,24 +2,66= 100 %.
=0,97 +31,64 +0,49 +64,24 +2,66= 100 %.
Определяем теплоту сгорания каждого топлива по формуле:
Qрн = 127.СО+108.Н2+358.СН4+590.С2Н4+555.С2Н2+635.С2Н6+913.С3Н8+
+1185.С4Н10+1465.С5Н12+234.Н2S,
где Qрн – низшая теплота сгорания топлива, кДж/м3.
Теплота сгорания топлива А:
Qрн (А) = 127·2,95+108·11,79+358·57,01+590.26,54=37716,15 кДж/м3.
Теплота сгорания топлива Б:
Qрн (Б) = 127·31,64+108·0,49=4071,2 кДж/м3.
Определяем состав смеси двух топлив.
Для этого необходимо определить долю топлива А в смеси топлив из выражения:
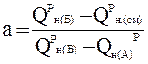 ,
,
где а – доля топлива А в смеси двух топлив;
Qрн(А), Qрн(Б) – теплота сгорания соответственно топлива Б и топлива А, кДж/м3;
Qрн(см) – теплота сгорания смеси топлив, кДж/м3,
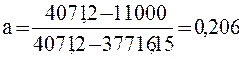 .
.
Состав смеси определяется по формуле:
Хвл(см) = Хвл(А).а + Хвл(Б).(1-а),
где Хвл(см), Хвл(А), Хвл(Б) – содержание компонента в смеси топлив и в топливах А и Б соответственно, %.
Тогда с учетом формулы состав смеси будет следующий:
СОсм =2,95·0,206+31,64.0,794=25,74 %;
СО2см =0,97· 0,794=0,77 %;
Н2см = 11,79.0,206+0,49.0,794=2,82 %;
СН4см =57,01·0,206=11,74 %;
С2Н4см =26,54· 0,206=5,47 %;
N2cм =64,24· 0,794=51,00 %;
Н2Осм =1,71· 0,206+2,66· 0,794 = 2,46 %.
Проверяем правильность расчета, складывая все компоненты смеси топлив:
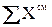 =25,74 +0,77 +2,82 +11,74 +5,47+51,00+2,46=100 %.
=25,74 +0,77 +2,82 +11,74 +5,47+51,00+2,46=100 %.
Определяем расход воздуха, состав и количество продуктов сгорания. Расчет ведём на 100 м3 смеси топлив.
Составляем реакции горения горючих компонентов смеси топлив и на их основе определяем количество требуемого для горения кислорода, а также количество образующихся продуктов сгорания.
а) СО + 1/2 02 = С02
1 м3СО - 0,5 м3 02
25,74 м3 СО - 12,87 м3 02 ;
1 м3СО - 1 м3 С02
25,74 м3 СО- 25,74 м3 С02.
б) Н2 + 1/202 = Н20
1 м3Н2 - 0,5 м3 02
2,82 м3 Н2 - 1,41 м3 02 ;
1 м3 Н2 - 1 м3 Н20
2,82 м3 Н2 - 2,82 м3Н20.
в) СН4 + 202 = С02 + 2Н20
1 м3 СН4 -2м3 02
11,74 м3 СН4 - 23,48 м3 02 ;
1 м3 СН4 - 1 м3 С02 и 2 м3 Н20
11,74 м3 СН4 - 11,74 м3 С02 и 23,48 м3Н20.
г) С2Н4 + 302 = 2С02 + 2Н20
1 м3 С2Н4 - 3 м3 02
5,47 м3 С2Н4 - 16,41 м3 02 ;
1 м3 С2Н4 - 2 м3 С02 и 2 м3 Н20
5,47 м3 С2Н4 - 10,94 м3 С02 и 10,94 м3 Н20.
Полученные данные заносим в таблицу 1.
Для определения количества воздуха с учетом коэффициента избытка воздуха, необходимо воспользоваться выражением:
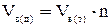 ,
,
где 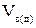 – действительный объем воздуха с учетом коэффициента избытка воздуха, м3;
– действительный объем воздуха с учетом коэффициента избытка воздуха, м3;
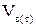 – теоретический объем воздуха (без учета коэффициента избытка воздуха), м3;
– теоретический объем воздуха (без учета коэффициента избытка воздуха), м3;
n – коэффициент избытка воздуха.
Таблица 1 – Результаты расчета расхода воздуха, состава и количества продуктов сгорания
| Участвуют в горении | Образуется продуктов сгорания, м3 | ||||||||
| Топливо, м3 | Воздух, м3 | ||||||||
| Составля-ющая | Содержа-ние, м3 | О2 | N2 | всего | СО2 | Н2О | О2 | N2 | всего |
| СО2 СО Н2 СН4 N2 C2Н4 Н2О | 0,77 25,74 2,82 11,74 5,47 2,46 | - 12,87 1,41 23,48 - 16,41 - | 54,17 · 3,762 = 203,79 | 54,17+203,79=257,96 | 0,77 25,74 - 11,74 - 10,94 - | - - 2,82 23,48 - 10,94 2,46 | 51+203,79=254,79 | ||
| n = 1 | 54,17 (21) | 203,79 (79) | 257,96 (100) | 49,19 (14,31) | 39,7 (11,55) | - | 254,79 (74,14) | 343,68 (100) | |
| n = 1,05 | 56,88 (21) | 213,98 (79) | 270,86 (100) | 49,19 (13,79) | 39,7 (11,14) | 2,71 (0,76) | 264,98 (74,31) | 356,58 (100) |
Для определения состава продуктов сгорания, воспользуемся формулой:
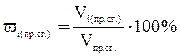 ,
,
где 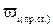 – содержание i-того компонента в продуктах сгорания, %
– содержание i-того компонента в продуктах сгорания, %
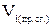 – объем i-того компонента в продуктах сгорания, м3;
– объем i-того компонента в продуктах сгорания, м3;
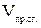 – общий объем продуктов сгорания, м3.
– общий объем продуктов сгорания, м3.
Таким образом, состав продуктов сгорания:
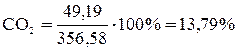 ;
;
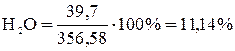 ;
;
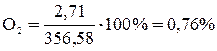 ;
;
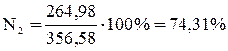 .
.
Для проверки правильности расчета составляется материальный баланс. Материальный баланс представлен в таблице 2.
Таблица 2 – Материальный баланс горения смеси двух топлив
| Поступило, кг | Получено, кг |
| Топливо: СО2 =0,77·44/22,4=1,51 СО =25,74·28/22,4=32,18 Н2О =2,46.18/22,4 =1,98 Н2 =2,82·2/22,4=0,25 СН4 =11,74·16/22,4=8,39 N2 =51·28/22,4=63,75 C2Н4 =5,47·28/22,4=6,84 Воздух: О2 =56,88.32/22,4=71,26 N2 =213,98.28/22,4=257,48 Итого: 443,64 кг. | Продукты сгорания: СО2 =49,19·44/22,4=96,62 Н2О =39,7.18/22,4 =11,90 N2 =264,98·28/22,4=331,23 О2 =2,71.32/22,4=3,87 Итого: 443,62 кг. |
Рассчитываем погрешность вычислений 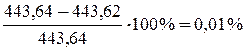 .
.
Из таблицы 1 следует, что для сжигания 100 м3 смеси топлив необходимо затратить 270,86 м3 воздуха при указанной величине коэффициента избытка воздуха, равной 1,05. При этом образуется продуктов сгорания 356,58 м3.
Определяем калориметрическую температуру горения. Для этого необходимо найти начальную энтальпию (теплосодержание) 1м3 продуктов сгорания:
I = Io + Iв + Iг,
где I – энтальпия продуктов сгорания, кДж/м3;
Io, Iв, Iг – соответственно количества тепла, получаемые от сжигания топлива и вносимые подогретым воздухом и топливом, кДж/м3.
Так как топливо не подогревается предварительно, то Iг=0.
Количество тепла, получаемое от сжигания топлива в расчете на единицу объема продуктов сгорания, определим из выражения:
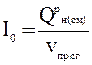 ,
,
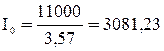 кДж/м3.
кДж/м3.
Количество тепла, вносимое подогретым воздухом, может быть определено следующим образом:
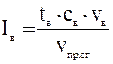 ,
,
где tв – температура подогрева воздуха, 0С;
св – теплоемкость воздуха при 400 оС, кДж/(м3.оС);
Vв – объем воздуха, вносимого в печь, м3,
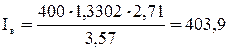 кДж/м3.
кДж/м3.
Таким образом, энтальпия продуктов сгорания составит:
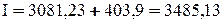 кДж/м3.
кДж/м3.
Далее искомую температуру находим методом подбора. Для этого задаемся возможной температурой горения, например, равной 2000˚ С, и определяем при этой температуре энтальпию продуктов сгорания с учетом табличных данных и состава продуктов сгорания:
СО2....................... 0,1379 ∙ 4919,51 = 678,40
Н2О....................... 0,1114∙ 3889,72 = 433,31
О2.........................0,0076 ∙ 3142,76 = 23,88
N2.........................0,7431 ∙ 2976,25 = 2211,65
––––––––––––––––––––––––––––––––––––––––––––––––
Итого...................................... 3347,24 кДж/м3.
Сравниваем полученную энтальпию с действительной энтальпией продуктов сгорания. Поскольку I>I2000 , следовательно, искомая температура горения больше, чем 2000 оС.
Задаемся температурой горения, равной 2100 0С. Энтальпия продуктов сгорания при этой температуре:
СО2....................... 0,1379 ∙ 5186,81 = 715,26
Н2О....................... 0,1114∙ 4121,79 = 459,17
О2.........................0,0076 ∙ 3314,85 = 25,19
N2.........................0,7431 ∙ 3131,96 = 2327,36
––––––––––––––––––––––––––––––––––––––––––––––––
Итого...................................... 3526,98 кДж/м3.
Т.к. I2100>I, то действительная калориметрическая температура горения лежит в пределах 2000 – 2100 оС.
Окончательно калориметрическую температуру горения определяем интерполяцией по формуле:
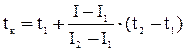 ,
,
где 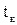 – калориметрическая температура горения, оС,
– калориметрическая температура горения, оС,
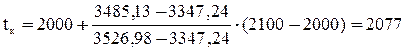 оС.
оС.
Список использованных источников
1 Куницина Н.Г. Расчет горения топлива. Методические указания для выполнения домашних заданий и контрольных работ по дисциплинам «Теплотехника», «Металлургическая теплотехника», Новотроицк: НФ НИТУ «МИСиС», 2015. – 31 с.






