Производные пурина
Пурин - это бициклическая система, которая имеет два цикла: пиримидин и имидазол:

Пурин синтезирован Э. Фишером из мочевой к-ты. Молекула плоского строения. В природе нет.
В природе производные: гидроксипурина, аминопурина; нуклеозиды (основание пурина + сахар), нуклеотиды (нуклеозид + Н3РО4); нуклеиновые к-ты.
Производные ксантина
Ксантин- 2,6-дигидроксипурин: Лактим Лактам

Гипоксантин - 6-гидроксипурин
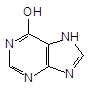
| Аденин - 6-аминопурин
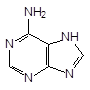
| Мочевая к-та - 2,6,8-триоксопурин
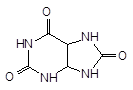
|
Значение производны пурина:
1. Лекарственное средство (кардиотоническое, диуретическое, бронхолитическое, стимуляторы ЦНС)
2. Некоторые пуриновые антиметаболиты обладают противоопухолевой и противовирусной активностью. Эти соединения незначительно отличаются по строению от природных и конкурируют (замещая их) в нуклеиновых кислотах.
Классификация ЛС:
1. Производные ксантина (Кофеин, Кофеин-бензоат натрия, Теобромин, Теофиллин, Эуфиллин)
Производные теофиллина: Дипрофиллин, Ксантинола никотинат
2. Нуклеозиды и нуклеотиды пурина (Рибоксин (производное гипоксантина), АТФ и ее динатриевая соль (производные аденина).
3. ЛС, близкие по строению к производным пурина (Аллопуринол (антиметаболит), Этимизол (аналептик), Фопурин (п/опухолевое средство)).
ЛС, производные ксантина
- это ди- и триметильные производные; производные 7Н-пурина. Алкалоиды.
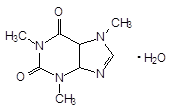
|
Кофеин - Coffeinum
1,3,7-триметилксантин моногидрат (производное 2,6-диоксопурина).
1819 г. - Рунге. В чае - 1,5-5%.
Специфика: 1) очень слабое органическое основание (как Папаверин, очень сильное основание - кодеин).

|
Кофеин-бензоат натрия - Coffeinum-natrium benzoas
Это комплексная соль кофеина и бензоата натрия.
Применяется: 10-20% р-р для инъекций; табл. 0,1 и 0,2.
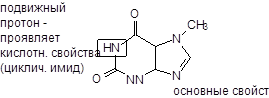
|
Теобромин - Theobrominum
3,7-диметилксантин (В 1-ом положении Н свободен).
1842 г. Воскресенский.
Это амфолит!
Спазмолитик и диуретик. Табл. по 0,25.

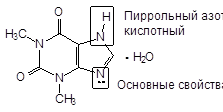
|
Теофиллин - Theofillinum
1,3-диметилксантина моногидрат (в 7-ом положении свободный Н).
1889 г. Коссель.
Спазмолитик, диуретик. Применяется в комбинированных ЛФ.
Эуфиллин (Аминофиллин) - Eufillinum
Это соль теофиллина с органическим основанием этилендиамином (2:1):
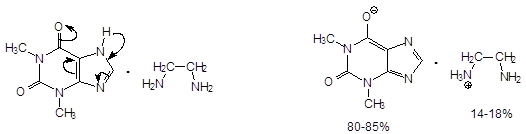
Для протонирования еще одной аминогруппы нужна еще одна молекула теофиллина (поэтому и 2: 1).
Соль образована по типу аммонийной соли.
На воздухе поглощает углекислый газ с высвобождением теофиллина Þ ухудшается растворимость.
ЛФ: табл. 0,15; р-р для инъекций 2,4% или 12%.
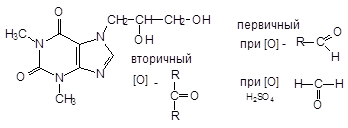
|
Производные теофиллина
Дипрофиллин - Diprophyllinum
7-(2,3-диоксипропил)-теофиллин
Табл. 0,2.
В 8-9 раз менее токсичен по сравнению с теофиллином. Спазмолитик.
Ксантинола никотинат (Компламин) - Xantinoli nicotinas

7-[2-окси-3-(N-метил-b-оксиэтиламино)-пропил]теофиллина никотинат
Улучшает периферическое и центральное кроветворение. Получают синтетическим путем.
Строение и растворимость производных ксантина:
Пурин - это ароматическая система с сильной делокализацей p-электронов. Обладает электродонорными свойствами Þ большая роль в образовании различных молекулярных комплексов. 7Н-пурин - неподеленная пара электронов отдает в цикл. Другие азоты (1,3 и 9) - пара электронов все в цикле.
Все производные пурина - слабые основания, поэтому протонируются по азоту в 9-ом положении. Соли с кислотами неустойчивые (нет г/хлоридов и других солей).
Производные ксантина - трудно растворимы в воде (лучше в горячей). Для получения хорошо растворимых в воде препаратов используется способность производных ксантина к комплексообразованию.
Растворимость в воде:
| Пурин | 1: 2 | Образуются водородные мостики с молекулами воды |
| Ксантин | 1: 15 000 | Образуются большие конгломераты молекул |
| Кофеин | 1: 60 | Лучше растворим в горячей воде, легко растворим в хлороформе. Мономер, не образует ассоциатов с водой и друг с другом |
| Теофиллин | 1: 120 | Димер, образуется сложная межмолекулярная связь с водой |
| Теобромин | 1: 3000 | Образует большие конгломераты молекул |
Различие в растворимости объясняется различием в межмолекулярном взаимодействии.
Растворимость кофеина повышается в присутствии солей органических кислот (бензойной, салициловой) - за счет образования комплексов (1: 1).
Комплексные соли: кофеин-бензоат натрия, эуфиллин - легко растворимы в воде.
Соли: ксантина никотинат - легко растворим в воде.
Физические свойства: белые кристаллические порошки.
Кофеин - белые шелковистые игольчатые кристаллы. Имеет характерную температуру плавления, ИК-спектр (от 400 см-1 до 4000 см-1); УФ-спектр - lmax = 274 нм - за счет ароматической системы.
Химические свойства:
кофеин - слабое органическое основание. Растворим в минеральных кислотах. Устойчивых солей не образует. Хорошо реагирует с общеалкалоидными реактивами:
1) с J2 в KJ (Люголя, Бушарда, Вагнера) - J2 /KJ + К-Б Na à нет осадка Þ + H2SO4 à Coff.·HJ·J4 - осадок коричневого цвета (образуется количественно!) Þ + NaOH Þ осадок растворяется.
2) + танин - осадок, растворимый в избытке реактива
3) Реактив Майера (HgJ2/KJ) - не осаждается! (см. чистоту).
В щелочи кофеин не растворим (все атомы водорода замещены на метильную группу).
ТЕОБРОМИН, ТЕОФИЛЛИН - имеют первичный протон. Это амфолиты.
Основные свойства: обусловлены не поделенной парой электронов азота в 9-ом положении.
Кислотные свойства: обусловлены протоном: а) в положении 1 - для Теобромина; б) в положении 7 - для Теофиллина. рКа = 9,9 (Теобромин), рКа = 8,8 (Теофиллин). Кислотные свойства Теофиллина сильнее Þ он, в отличие от Теобромина, растворим в не только в NaOH, но и растворе аммиака (! - подлинность и чистота теофиллина).

Препарат «Темисал» - это теобромин-натрий + салициловая к-та.
При растворении теофиллина в NaOH образуется натриевая соль по кислотному центру в положении 6:
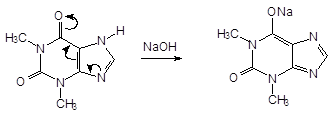
За счет кислотных свойств образуют: 1) водорастворимые соли с веществами основного характера; 2) не растворимые соли с солями Ag, Co, Cu. Ag и Co - ГФХ.
Условия реакции: препарат кислотного характера + эквивалент 0,1н щелочи. Теобромин, Теофиллин, салициламид, бензойная к-та - не д.б. избытка щелочи, иначе м.б. гидроксид металла.
С Cu2+ - нехарактерные голубые осадки
С Со3+: Теофиллин - бледно-розовый осадок, Теобромин - быстро исчезающее фиолетовое окрашивание и серо-голубой осадок.
С солями меди и кобальта м.б. написание комплексных солей через кислород.
AgNO3 - образуются растворимые (выделяется HNO3 в эквивалентных количествах) или не растворимые (при добавлении раствора аммиака) серебряные соли.
NB! - Как и в барбитуратах, серебряные соли образуются только по азоту.

Данная реакция используется как для подлинности, так и для К.О. (см. ниже)
Комплексы с Hg(CH3COO)2:
Кофеин - белый осадок комплекса; Теофиллин - белый микрокристаллический осадок, Эуфиллин - осадок.
Теобромин осадка не образует.
Реакция образования мурексида (мурексидная проба). При данной реакции происходит гидролиз и окисление. Препарат + окислитель (Н2О2, Br2, HNO3) Þ нагревают на водяной бане + раствор NH3 Þ возникает пурпурно-красное окрашивание. Данная реакция не специфична, ее дают оксопроизводные пиридина. Реакция основана на окислительно-гидролитическом разложении ксантина до пиримидин-производных (через цикл имидазола и окисление пиримидина), в которой 1 или 2 NH2-группа конденсирована с другой до пурпурно-красной окраски. М.б. различной степени метилирования.
Аммонийная соль пурпурной к-ты (?) окрашена в красно-пурпурный цвет. [Улитки murex Þ мурексид (краситель)].
1. Для мочевой к-ты возникает окрашивание с HNO3
2. Для метилированных производных ксантина вместо HNO3 применяют H2O2 + HCl, а затем добавляют NH3 (если NH3 образуется в результате реакции, то его не обязательно добавлять)
3. Для кофеина нельзя применять конц. HNO3, т.к. возможно нитрование его положению 8 с образованием нитропроизводного кофеина, который не дает реакцию образования мурексида.
ГФ Х и XI: препарат + 10 к.развед. HCl (8%), + 10 к. 30% H2O2 при нагревании на водяной бане выпаривают досуха, к остатку прибавляют несколько капель раствора NH3 - образуется мурексид. HCl и H2O2 удаляются при нагревании. Положение 4 и 5 будут полностью окислены, гидролиз между положение 9 и 4:

Заключительная стадия: добавление раствора NH3:

Данное соединение применяется как металлоиндикатор при определении солей кальция.
Реакции SE после щелочного гидролиза.
1. Кофеин, обладающий слабыми основными свойствами, не устойчив в щелочной среде. При рН > 9 происходит разложение кофеина до кофеиндикарбоновой к-ты - является антагонистом кофеина (учитывают при выделении кофеина при выделении его из ЛРС):

Кофеидин по строению близок к этинизолу.
Теофиллин разлагается аналогично. Образуется теофиллидин, который идентифицируется по реакции образования азокрасителя:

Частные реакции
1. кофеин-бензоат натрия. Реакция на бензоат-ион:
(бензоат-Na) + FeCl3 à (Ar-COO-)3Fe·Fe(OH)3·7H2O¯
2. Теофиллин. Сочетается в боратном буфере при рН = 8,5 - 9 с 2,6-дихлорхинониндофенолом (это реактив на свободное п -положение у фенолов).
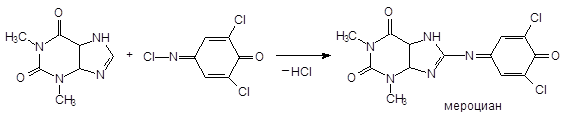
Образуется мероцианин - краситель голубого цвета.
3. Эуфиллин (резко щелочная реакция среды) реакция на этилендиамин: препарат + очень разбавленный CuSO4 Þ фиолетовое окрашивание Þ образуется комплекс, аналогичный [Cu(NH3)4]SO4:

этилендиамин из эуфиллина
4. Дипрофиллин. 1) Реакция образования мурексида; 2) + NaOH Þ NH3 (запах, лакмусовая бумага); 3) разложение препарата при нагревании с КHSO4 - на бумаге сверху пробирки, смоченной свежим раствором нитропруссида натрия и пиперидином появляется синее пятно, кот. при добавлении 1-2 капель NaOH превращается в розовое. Реакция не специфична. Возможно образование пропандиола.
5. Кстантинола никотинат. 1) Уф спектр; 2) ТСХ - относительно никотиновой к-ты.
Чистота ЛП.
1. Посторонние пуриновые соединения: а) Кофеин - нет осадка с реактивом Майера; б) Теофиллин - должен полностью растворяться в растворе NH3; в) Теобромин - примеси: триметилксантин Þ препарат + 0,1н NaOH + СоCl2 Þ фиолетовое окрашивание должно исчезнуть не более, чем через 3 минуты (если примесь есть - окрашивание не исчезает); теобромин - препарат взбалтывают с хлороформом в щелочной среде, выпаривают и нормируют вес сухого остатка. г) Дипрофиллин - не должно быть теофиллина (!) Þ + СоCl2 Þ не должно быть фиолетового окрашивания.
Общая тенденция - введение ТСХ и ВЭЖХ.
Общие требования для ЛВ, применяемых для приготовления инъекционных растворов: прозрачность, цветность, рН водного раствора (эуфиллин - рН» 9).
Количественное определение:
1. Кислотно-основное титрование в неводной среде.
А) Определение оснований кофеина, ксантинола никотината.

|
Кофеин - слабое основание Þ недостаточно растворить в лед. CH3COOH, поэтому растворяют в смеси: уксусный ангидрид + бензол - это апротонные основания, не влияющие на результат титрования. В результате образуется coff.·HClO4 - протонируется азот в 9-ом положении.
Б) Определение по кислотным свойствам: теофиллин, теобромин.
Растворяют в растворителях основного характера: ДМФА, бутиламин, пиридин. Титруют спиртовыми растворами щелочей, в данном случае - алкоголятами: CH3ОК (или Na, Li); С2Н5ОК.
2. Косвенный метод нейтрализации (прямой способ титрования).
3. Определяют теофиллин, теобромин: препарат + кип. Н2О + фиксированный избыток титранта или станд. Р-р AgNO3 Þ серебряная соль, которая растворима в выделившейся HNO3 (!) - [ реакция - см. выше ]. Эквивалентное количество HNO3 титруют NaOH по феноловому красному.
NB! Специфика для эуфиллина - т.к. ярко выраженная щелочная среда Þ нельзя добавлять AgNO3. Для субстанции эуфиллина - сушат в шкафу до удаления запах этилендиамина (в растворе остается только теофиллин).
3. Аргентометрия (обратное титрование)
Определяют теофиллин, теобромин, т.к. они содержат подвижный протон.
+ раствор NH3 определенное количество Þ в осадке образуется серебряная соль (для нейтрализации выделяется HNO3).
1) Образование серебряной соли:...à осадок + HNO3 (+ NH4ОН à NH4NO3 + H2O)
2) Изб. AgNO3 + NH4SCH à AgSCN + NH4NO3
3) 3NH4SCN + Fe(NH4)(SO4)2 à Fe(SCN)3 + 2(NH4)2SO4
Титруют до появления красного окрашивания.
4. Йодометрия
Определение кофеина и кофеин-бензоата натрия. Проводится в кислой среде, так как кофеин, если вы еще не запомнили - слабое основание. Образуется количественно перйодид кофеина Coff.·HJ·J4¯ - коричневый осадок. Раствор фильтруют, в фильтрате определяют избыток J2 с Na2S2O3.
5. Нейтрализация в водной среде.
Определяют кофеин-бензоат натрия. Препарат растворяют в воде, титруют раствором HCl в присутствии метилового оранжевого или метилового синего. Выделяется бензойная к-та, которую извлекают в органический растворитель (эфир).
В эуфиллине - определяют этилендиамин. Т = HCl. Конечный продукт: [N+H3-CH2-CH2-N+H3]2Cl-; z=2.
6. Определение азота в органических соединениях методом Кьельдаля.
Дипрофиллин. + конц. H2SO4 + мет., нагревают Þ (NH4)2SO4 Þ + NaOH Þ NH3 . Затем добавляют борную к-ту: В(ОН)3 + НОН à В(ОН)4 + NH3 à NH4В(ОН)4.
Затем: NH4В(ОН)4 + HCl à NH4Cl + Н3ВО3.
7. Весовой (гравиметрия).
Для многокомпонентных ЛФ, содержащих кофеин. Кофеин количественно извлекают хлороформом, затем хлороформ отгоняют. Остаток сушат и определяют по весу - это и будет кофеин (очень слабое основание).
8. Физико-химические методы.
А) За кордоном: USP 24: ВЭЖХ (субстанция - стандартные образцы)
Б) У нас: УФ-спектрофотометрия. lmax = 264 нм - ЛФ (стандартные образцы - субстанции)
В) У нас: Рефрактометрия: растворы и концентраты кофеин-бензоата натрия.
Производные пурина
1. Нуклеозиды и нуклеотиды пурина (Рибоксин, АТФ и ее динатриевая соль)
2. Результаты поиска новых ЛС группы пуринов (Аллопуринол, Этимизол, Фопурин).
Нуклеозиды и нуклеотиды пурина (9Н-пурина)
Нуклеозиды - это продукты взаимодействия азотсодержащих органических оснований (пурина или пиримидина) с сахаром.
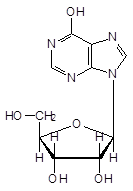 Рибоксин
Рибоксин
|
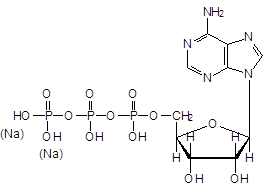 АТФ
АТФ
|
Рибоксин - Riboxinum (ГФ XI).
9b-D-рибофуранозилгипоксантин (гипоксантин-N-рибозид).
N-гликозид гидролизуется только в кислой среде. Получают биосинтезом, продуцируется бактериями. ЛФ - табл., покрытые оболочкой. Список Б. Применяется как сердечно-сосудистое средство.
Acidum adenosintriphosphoricum - Кислота аденозинтрифосфорная
Трифосфорнокислый эфир 9b-D-рибофуранозида аденина.
АТФ - это нуклеотид - продукт взаимодействия нуклеозида и фосфорной к-ты (3 шт.)
Связь с остатком рибозы - это N-гликозид.
Препарат применяется для приготовления натриевой соли раствора для инъекций (как сердечно-сосудистое средство): Natrii adenosintriphosphas - в/м 1% р-р.
Описание: оба препарата - белые кристаллические вещества, Рибоксин медленно растворим в воде, динатриевая соль АТФ хорошо растворима в воде.
Подлинность: 1) ИК, УФ спектры
2) Химическая реакция на остаток рибозы с орцином. Орциновый реактив: 5 мл HCl (для гидролиза)
+ 0,01 г орцина + 1 капля FeCl3.
Препарат растворяют в воде + 3 мл орцинового реактива, нагревают на кипящей водяной бане Þ образуется сине-зеленое окрашивание (пентозы) + дополнительно добавляют FeCl3 - появляется зеленое окрашивание (рибоза) Þ в результате реакции образуется свободный сахар:
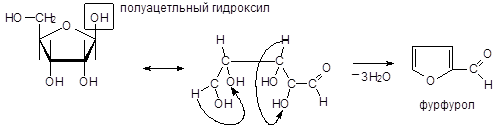
Рибоза имеет полуацетальный гидроксил (полуацеталь = альдегид + спирт в пределах одной молекулы).

Окисление происходит за счет FeCl3. В результате образуется продукт сине-зеленого цвета
Подлинность на АТФ:
3) Реакция на фосфат-ион после получения его в виде иона из фосфорнокислого эфира. Препарат нагревают обычно с разведенной HNO3 при нагревании Þ образуется фосфат-ион, затем раствор доводят до оптимальной рН.
А) с AgNO3 (при рН около 7): AgNO3 + PO43- à Ag3PO4¯
Образуется осадок желтого цвета, растворимый в разведенной HNO3 и в растворе аммиака.
Б) Образование аммония-магния фосфата NH4MgPO4 - белый осадок, растворимый в минеральных кислотах. Реактив: MgSO4 + NH4Cl + NH4OH. Данная реакция применима для АТФ.
В) С молибдатом аммония, образование магния аммония фосфата (NH4)3PO4·12MoO3¯ - кристаллический желтый осадок, растворимый в аммиаке.
Чистота: 1) прозрачность и цветность для динатриевой соли АТФ (т.к. это р-р для инъекций); 2) посторонние пуриновые основания и ксантин - методом ТСХ относительно стандарта примеси или в качестве рабочего стандартного образца (РСО) - сам препарат.
К.О.: 1) Рибоксин: СФМ в УФ области относительно стандартного образца рибоксина;
2) динатриевая соль АТФ - хломатоспектрофотометрия - разделение на колонке с ионообменной смолой.
Некоторые новые ЛС, производные пурина и близкие по структуре

|
Аллопуринол - Allopurinolum - 8-азагипоксантин.
Имеет ОН-кислотный центр, так же это NH-кислота (имеет имино-группу). По свойствам - амфолит. Это изомер гипоксантина, блокирует фермент, который превращает гипоксантин в ксантин Þ в мочевую к-ту (блокирует ее образование). Препарат применяют для лечения гиперурикемических обострений.
Описание: белый или с кремоватым оттенком мелкокристаллический порошок, практически не растворим в воде, легко растворим в растворах щелочей. Список Б. ЛФ - табл. по 0,1.

|
Этимизол - Aethymizolum.
Это замещенный амид имидазолдикарбоновой к-ты (близок по строению к кофеину)
бис-(метиламид)-1-этилимидазол-4,5-дикарбоновой к-ты.
Описание: белый кристаллический порошок. Мало растворим в воде, растворим в спирте.
Характерна гидроксамовая проба (не специфична). Проводится кислотный или щелочной гидролиз и определяются продукты реакции. Для замещенных амидов лучше щелочной гидролиз.
Список Б. В/м, в/в - 1-1,5% р-ры или табл. по 0,1. Аналептик, стимулятор дыхания.

|
Фопурин - Phopurinum
6-диэтиленимидофосфамидо-2-диметиламино-7-метилпурин
Описание: это белый со слегка зеленоватым оттенком кристаллический порошок, растворим в воде, спирте, легко - в хлороформе. Список А. Противоопухолевое средство, токсичен; хранить при температуре не выше 10оС, без доступа света.
Подлинность (общая): 1) УФ, ИК спектры
2) Этимизол - общие реакции на амидные связи:
а) гидроксамовая проба - это реакция ацилирования гидроксиламина. Ее дают все соединения, который в момент гидролиза дают ацильный остаток (или остаток к-ты), который ацилирует гидроксиламин (это сложные эфиры, лактоны (внутренние сложные эфиры), амиды, лактамы).
В результате образуется:

б) гидролиз в кислой или щелочной среде. Но щелочная - лучше.
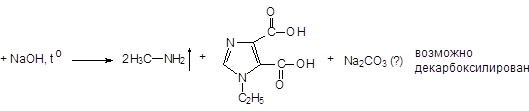
3) ФОПУРИН - а) Реакция на фосфат-ион после его получения. Препарат нагревают с HNO3, полученный фосфат обнаруживают любой из трех выше рассмотренных реакций. Наиболее часто - образование магния аммония фосфата.
б) реакции с общеалкалоидными осадительными реактивами.
Чистота: ТСХ - определяют посторонние пурины или родственные соединения.
К.О.: 1) Аллопуринол - кислотно-основное титрование в неводной среде как слабой кислоты. Препарат растворяют в ДМСО (диметилсульфоксид) и титруют спиртовым раствором NaOH по тимоловому синему. Возможно образование ONa-группы. Растворители - м.б. ДМФА, пиридин, бутиламин Þ протофильные растворители. Титрантом м.б. алкоголяты металлов Þ метоксиды или этоксиды натрия, калия, лития.
Табл. К.О. -СФМ в УФ области. При растворении препарата в щелочи.
2) Этимизол и фопурин - определяются кислотно-основным титрованием в неводной среде по основным свойствам (т.к. они преобладают). Растворитель - лед. CH3COOH; лед. CH3COOH + бензонал (апротонный растворитель); уксусный ангидрид; смесь уксусного ангидрида и CH3COOH; муравьиная к-та. Т = HClO4, которая готовится на лед. CH3COOH. Индикатор - кристаллический фиолетовый, который тоже готовится на CH3COOH.
Из фопурина получается перхлорат фопурина.
В ЛФ К.О. - СФМ в Ф области спектра.




