Алканами называются углеводородные соединения, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода. Они также называются парафинами. В молекулах алканов атомы углерода связаны одинарной связью, а все остальные валентности насыщены атомами водорода. Для предельных углеводородов является характерным окончание -ан. Метан – декан.
Когда речь идет о неразветвленных алканах к названию обычно добавляют приставку (н - – нормальный), например – бутан. При отрыве атома водорода от молекулы алкана образуются так называемые углеводородные радикалы (R). Названия радикалов происходят от названия соответствующих алканов с заменой окончания -ан на -ил. Метил – децил.
Для построения названий разветвленных углеводородов основой служит самая длинная углеводородная цепь, а все другие фрагменты рассматриваются как заместители. Главную цепь выбирают так, чтобы число боковых радикалов было минимальным. Атомы цепи нумеруют таким образом, чтобы сумма цифр радикалов, расположенных в боковых цепях, была минимальной. При названии углеводорода сначала называют номера углеродных атомов главной цепи, начиная с номеров простейших радикалов. Затем называют сам углеводород, которому соответствует самая длинная цепь. Если в молекуле содержится несколько одинаковых радикалов, то перед их названием указывают их количество прописью, а номера радикалов (цифрами) разделяют запятыми.
Например, гексан имеет 5 изомеров.
А вот более сложный пример: 2,3,5-триметил-5-этилгептан (15), а не 3,5,6-триметил-3-этилгептан (17).
Атом углерода, который связан только с одним атомом углерода, называется первичным, с двумя – вторичным, с тремя – третичным, с четырьмя – четвертичным. Так, в последнем примере, в главной цепи 1 и 7 атомы С – первичные; 4 и 6 – вторичные; 2 и 3 – третичные, а 5 – четвертичный.
Получение алканов. Метан, этан и пропан входят в состав природного газа, в основном это метан. В природе метан образуется при медленном разложении растительных остатков без доступа воздуха. Именно поэтому он выделяется в воздух из каменноугольных пластов в шахтах и рудниках. Для получения синтетического бензина применяют реакцию оксида углерода(II) с водородом в присутствии соединений кобальта и при повышенном давлении. Химические свойства.

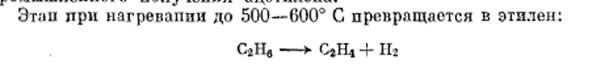


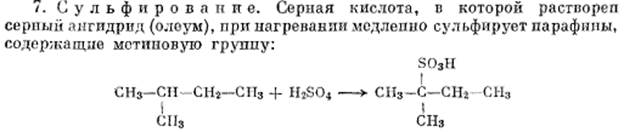
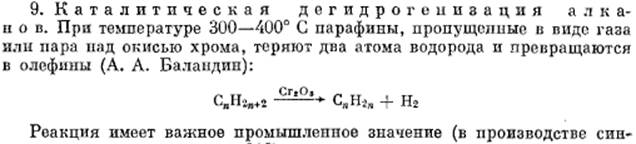
Применение алканов. В первую очередь в качестве топлива метан – природный газ. Основной компонент бензина – 2,2,4-триметилпентан (изооктан – характеризует октановое число бензина: если его 100%, то октановое число равно 100). Дизельное топливо характеризуется цетановым числом. Цетановое число 100 отвечает чистому цетану (гексадекану – С16Н34), а цетановое число 15 – чистому 2,3,4,5,6,7,8-гептаметилнонану. Бензиновый и дизельный двигатели работают по противоположным принципам. В бензиновом двигателе внутреннего сгорания топливо вводится мгновенно в период, предшествующий рабочему ходу и поэтому используются углеводороды с более разветвленной и короткой цепью, которые имеют слабую детонацию. Если взять неразветвленный н-гептан, то он детонирует очень сильно и его октановое число равно 0. Таким образом, бензин АИ-95 должен соответствовать смеси 95% изооктана (2,2,4-триметипентана) и 5% н-гептана.
Наоборот, в дизельном двигателе топливо разбрызгивается во время рабочего хода поршня и воспламеняется в момент поступления в цилиндр, поэтому для дизельного двигателя нужны углеводороды с более длинной и неразветвленной цепью. На нефтеперерабатывающих предприятиях содержание разветвленных углеводородов и укорачивание цепи углеводородов повышают путем их нагревания в присутствии катализатора. При этом от неразветвленных молекул отщепляются различного размера радикалы, которые затем присоединяются в других местах различных молекул, образуя разветвления.
Большое промышленное значение имеет окисление алканов с числом углеродных атомов 20-25 (парафин) в различные жирные кислоты, которые используются в производстве мыла, синтетических моющих средств, смазочных материалов, лаков, эмалей и красок.
Лекция 22.






