Процессы катаболизма в клетках животных сопровождаются потреблением кислорода, который необходим для реакций окисления. В результате этих реакций происходит освобождение энергии, которая необходима организмам в процессах жизнедеятельности для осуществления различных видов работы. Небиологические системы могут совершать работу за счёт тепловой энергии, биологические системы функционируют в изотермическом режиме и для осуществления
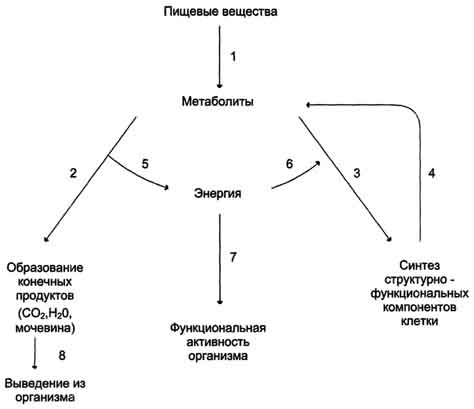
Рис. 6-1. Общая схема обмена веществ и энергии. 1 - пищеварение; 2 - катаболизм; 3 - анаболизм; 4 - распад структурно-функциональных компонентов клеток; 5 - экзергонические реакции; 6,7 - эндергонические реакции; 8 - выведение из организма.
процессов жизнедеятельности используют химическую энергию. Изучением превращений энергии, сопровождающих химические реакции, занимается биоэнергетика, или биохимическая термодинамика.
А. Свободная энергия и законы термодинамики
Живые организмы с точки зрения термодинамики - открытые системы. Между системой и окружающей средой возможен обмен энергии, который происходит в соответствии с законами термодинамики.
Законы термодинамики
Первый закон - закон сохранения энергии; его можно сформулировать так: общая энергия системы и окружающей среды - величина постоянная.
Внутри рассматриваемой системы энергия может переходить от одной её части к другой или превращаться из одной формы в другую.
Второй закон гласит, что все физические и химические процессы в системе стремятся к необратимому переходу полезной энергии в хаотическую, неуправляемую форму. Мерой перехода или неупорядоченности системы служит величина, называемая энтропией (S), она достигает максимума, когда система приходит в истинное равновесие с окружающей средой.
Свободная энергия
Каждое органическое соединение, поступающее в организм извне или входящее в состав живой материи, обладает определённым запасом внутренней энергии (Е). Часть этой внутренней энергии может быть использована для совершения полезной работы. Такую энергию системы называют свободной энергией (G).
При постоянных температуре и давлении соотношение между изменением свободной энергии системы (ΔG) и изменением энтропии (ΔS) можно представить следующим уравнением:
ΔG = ΔН - T×S, где ΔН - изменение энтальпии (внутренней энергии или теплоты, содержащейся в системе); Т - абсолютная температура. В условиях, при которых протекают биохимические реакции, ΔН приблизительно равно ΔЕ (изменению внутренней энергии системы в результате реакции). Для биологических систем измерение свободной энергии производят обычно при стандартных условиях, когда рН 7,0, температура 25 °С, все растворы находятся в концентрации Г моль/л, а все газы при давлении в 1 атм.
При стандартных условиях все функции обозначают как ΔG0', ΔS0' и ΔН0'. Изменение стандартной свободной энергии (AG0') можно вычислить, зная константу равновесия (K'eq) химической реакции.






