Утверждено
на заседании кафедры
Протокол № ___ от ___________ 2015 года
Заведующая кафедрой_______________
_____________Иванова Н.С.
Методические рекомендации
по проведению самостоятельной работы студентов
модуль №5 «Кинетика химических реакций и катализ»
учебной дисциплины Физическая и коллоидная химия
для специальности 33.05.01«Фармация»
курс IӀ семестр ӀII
Составитель Задорожная А.Н.
к.х.н., доцент
Рецензент Иванова Н.С.
к.х.н., доцент
Владивосток, 2015
1.Тема СРС: Кинетика химических реакций и катализ
2. Мотивация изучения темы: Кинетические исследования позволяют решить теоретические и практические проблемы в:
- биологической химии, биологии, фармакологии: оценка скоростей биохимических и физиологических процессов в норме и при патологии, оценка скоростей выведения из организма лекарственных препаратов, влияние лекарств на активность ферментов;
- органической химии: влияние различных факторов на скорость химических процессов;
- фармацевтической технологии: определение срока годности и условий хранения лекарственных средств, определение оптимальных условий производства лекарственных форм при разработке технологического процесса.
3.Цели самостоятельной работы студентов:
1. научиться оценивать влияние различных факторов на скорость химических и биохимических процессов;
2. обосновывать зависимость скорости реакций от температуры на основе теории активных столкновений и активированного комплекса;
3. ознакомиться с особенности протекания сложных реакций в открытых системах.
3.1.Общая цель: изучение темы направлено на формирование компетенции ПК-35, ПК-41 по ФГОС специальности Фармация.
Конкретные цели и задачи.
После изучения темы студент должен:
«Знать» -основные понятия, способы расчета сроков годности, периода полупревращения лекарственных веществ, механизм, виды катализа, роль промоторов, ингибиторов.
«Уметь» - решать типовые и ситуационные задачи, оценивать влияние различных факторов на скорость химических и биохимических процессов.
«Владеть» -навыками интерпретации рассчитанных значений с целью прогнозирования возможности осуществления и направление протекания химических процессов.
Контрольные вопросы.
1. Зависимость скорости реакции от концентрации:
-закон действующих масс для гомогенных и гетерогенных реакций;
-понятие о молекулярности и порядке реакции. Методы определения порядка реакции;
- кинетические уравнения 0, 1 и 2-го порядков. Период полупревращения, его использование в фармакокинетике.
2. Зависимость скорости реакции от температуры:
- правило Вант-Гоффа. Температурный коэффициент скорости реакции, его особенности для биохимических процессов. Методы определения сроков годности лекарственных препаратов;
-теория активных соударений. Энергии активации. Взаимосвязь скорости реакции и энергии активации. Уравнение Аррениуса;
-теория переходного состояния (активированного комплекса). Уравнение Эйринга, его анализ.
3. Сложные реакции:
-параллельные;
- последовательные;
- сопряженные;
- обратимые и необратимые;
- цепные реакции. Механизм цепных реакций;
- фотохимические реакции. Закон фотохимической эквивалентности Эйнштейна. Квантовый выход реакции.
4. Катализ:
- гомогенные и гетерогенные каталитические реакции. Катализаторы: требования, предъявляемые к катализаторам. Механизм действия катализаторов;
-особенности каталитических реакций в организме. Уравнение Мехаэлиса-Ментен, его анализ.
Задания для самостоятельной работы студентов.
| Вопросы для самостоятельного изучения | Виды и содержание самостоятельной работы | ||||||||||
| 1.Зависимость скорости реакции от концентрации. | Для закрепления и систематизации знаний:
- работа с конспектом лекции № 10,
- работа с обязательной и дополнительной литературой, интернет – ресурсами.
Вариант теста №1
При условии, что реакция 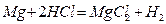 является элементарной (простой), ее скорость описывается уравнением:
а) является элементарной (простой), ее скорость описывается уравнением:
а) 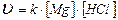 б)
б) 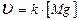 в)
в) 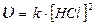 г)
г) 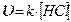 Вариант теста №2
Константа равновесия биохимического процесса в организме человека при понижении температуры и неизменной концентрации реагирующих веществ:
а) не изменится;
б) увеличится;
в) уменьшится.
Вариант теста № 3.
Реакция гидролиза новокаина протекает как реакция первого порядка. Это означает, что
а) скорость гидролиза прямо пропорционально концентрации новокаина;
б) скорость гидролиза не зависит от концентрации новокаина;
в) скорость гидролиза прямо пропорциональна квадрату концентрации новокаина.
Для формирования умений:
Задача №1
Указать порядок реакции СН3СОН (г) = СН4 (г) + СО (г) по веществу и написать кинетическое уравнение реакции. Как изменится скорость реакции при: а) уменьшении концентрации ацетальдегида в 2 раза; б) увеличении давления в 3 раза.
Задача №2
При лечении онкологических заболеваний в опухоль вводят препарат, содержащий радионуклид иридий-192. Какая часть введенного радионуклида останется в опухоли через 10 сут? t (192Ir)=74,08 сут.
Задача №3
Кинетика реакции первого порядка, в которой происходило образование кислоты, изучалась путем отбора проб реакционной смеси и их титрование одним и тем же раствором щелочи. Объемы, которые пошли на титрование:
Вариант теста №2
Константа равновесия биохимического процесса в организме человека при понижении температуры и неизменной концентрации реагирующих веществ:
а) не изменится;
б) увеличится;
в) уменьшится.
Вариант теста № 3.
Реакция гидролиза новокаина протекает как реакция первого порядка. Это означает, что
а) скорость гидролиза прямо пропорционально концентрации новокаина;
б) скорость гидролиза не зависит от концентрации новокаина;
в) скорость гидролиза прямо пропорциональна квадрату концентрации новокаина.
Для формирования умений:
Задача №1
Указать порядок реакции СН3СОН (г) = СН4 (г) + СО (г) по веществу и написать кинетическое уравнение реакции. Как изменится скорость реакции при: а) уменьшении концентрации ацетальдегида в 2 раза; б) увеличении давления в 3 раза.
Задача №2
При лечении онкологических заболеваний в опухоль вводят препарат, содержащий радионуклид иридий-192. Какая часть введенного радионуклида останется в опухоли через 10 сут? t (192Ir)=74,08 сут.
Задача №3
Кинетика реакции первого порядка, в которой происходило образование кислоты, изучалась путем отбора проб реакционной смеси и их титрование одним и тем же раствором щелочи. Объемы, которые пошли на титрование:
Докажите, что реакция имеет первый порядок. Рассчитайте период полураспада.
| ||||||||||
| 2. Зависимость скорости реакции от температуры. | Для закрепления и систематизации знаний:
- работа с конспектом лекции № 10;
- работа с обязательной и дополнительной литературой, интернет – ресурсами.
Вариант теста № 1
В уравнении Аррениуса 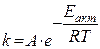 множитель А выражает:
а) количество активных молекул;
б) скорость реакции при концентрациях равных 1;
в) общее число эффективных столкновений молекул.
Вариант теста № 2.
Из пяти реакций быстрее протекает реакция с энергией активации:
а) 22;
б) 11;
в) 5.
Вариант теста № 3.
Энергией активации является
а) энтальпия реакции;
б) минимальная энергия, достаточная для перевода частицы в активное состояние;
в) внутренняя энергия частицы.
Вариант теста № 4.
Влияние температуры на скорость химической реакции описывается
а) законом действующих масс;
б) правилом Вант-Гоффа;
в) правилом Панета-Фаянса-Гана.
Для формирования умений:
Задача № 1.
При повышении температуры с 15 до 25°С период полураспада некоторой реакции первого порядка уменьшается в 3,5 раза. Вычислите энергию активации этой реакции.
Задача № 2
Вычислите энергию активации окисления сульфата железа (II) хлоратом калия в среде серной кислоты в интервале от 10 до 32°С, температурный коэффициент константы скорости равен 2,4.
Задача №3
С помощью правила Вант-Гоффа вычислите, при какой температуре реакция закончится через 15 мин., если при 20°С на это требуется 2 ч. Температурный коэффициент скорости равен 3. множитель А выражает:
а) количество активных молекул;
б) скорость реакции при концентрациях равных 1;
в) общее число эффективных столкновений молекул.
Вариант теста № 2.
Из пяти реакций быстрее протекает реакция с энергией активации:
а) 22;
б) 11;
в) 5.
Вариант теста № 3.
Энергией активации является
а) энтальпия реакции;
б) минимальная энергия, достаточная для перевода частицы в активное состояние;
в) внутренняя энергия частицы.
Вариант теста № 4.
Влияние температуры на скорость химической реакции описывается
а) законом действующих масс;
б) правилом Вант-Гоффа;
в) правилом Панета-Фаянса-Гана.
Для формирования умений:
Задача № 1.
При повышении температуры с 15 до 25°С период полураспада некоторой реакции первого порядка уменьшается в 3,5 раза. Вычислите энергию активации этой реакции.
Задача № 2
Вычислите энергию активации окисления сульфата железа (II) хлоратом калия в среде серной кислоты в интервале от 10 до 32°С, температурный коэффициент константы скорости равен 2,4.
Задача №3
С помощью правила Вант-Гоффа вычислите, при какой температуре реакция закончится через 15 мин., если при 20°С на это требуется 2 ч. Температурный коэффициент скорости равен 3.
| ||||||||||
| 3. Сложные реакции | Для закрепления и систематизации знаний:
- работа с обязательной и дополнительной литературой, интернет – ресурсами.
Вариант теста № 1
Кинетическое уравнение сложной последовательной реакции
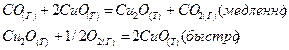 запишется так:
а)
запишется так:
а) 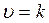 ;
б) ;
б) 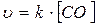 ;
в) ;
в) 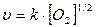 ;
г) ;
г) 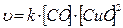 .
Вариант теста № 2.
Реакция, протекающая согласно уравнению .
Вариант теста № 2.
Реакция, протекающая согласно уравнению 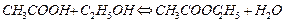 классифицируется как:
а) последовательная;
б) обратимая;
в) сопряженная;
г) параллельная.
Вариант теста № 3.
Реакция протекает по схеме: классифицируется как:
а) последовательная;
б) обратимая;
в) сопряженная;
г) параллельная.
Вариант теста № 3.
Реакция протекает по схеме:
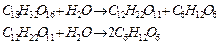 и классифицируется как:
а) последовательная;
б) обратимая;
в) сопряженная;
г) параллельная.
Вариант теста № 4.
Для последовательной реакции
и классифицируется как:
а) последовательная;
б) обратимая;
в) сопряженная;
г) параллельная.
Вариант теста № 4.
Для последовательной реакции 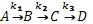 k1 = 0,02 с–1; k2 = 2 с–1; k3 = 200 с–1. Лимитирующей (скорость определяющей) стадией реакции является
а) превращение C → D;
б) превращение A → B;
в) превращение B → C. k1 = 0,02 с–1; k2 = 2 с–1; k3 = 200 с–1. Лимитирующей (скорость определяющей) стадией реакции является
а) превращение C → D;
б) превращение A → B;
в) превращение B → C.
| ||||||||||
| 4. Катализ | Для закрепления и систематизации знаний: - работа с конспектом лекции № 11; - работа с обязательной и дополнительной литературой, интернет – ресурсами. Вариант теста № 1 Ускоряющее действие ферментов связано с а) увеличением энергии активации соответствующего превращения; б) существенным уменьшением энергии активации превращения за счёт образования фермент-субстратного комплекса; в) увеличением концентраций реагирующих веществ. Вариант теста № 2. При неконкурентном ингибировании ингибитор взаимодействует с: а) аллостерическим центром фермента; б) поверхностью фермента; в) активным центром фермента. Вариант теста № 3. Функция активатора в биохимических процессах: а) инактивировать фермент; б) повышать активность фермента; в) замедлять реакцию. Вариант теста № 4. Теория гетерогенного катализа предполагает, что процесс идет: а) на активных центрах катализатора; б) на всей поверхности катализатора; в) в глубине катализатора. Для формирования умений: Задача № 1 Энергия активации разложения пероксида водорода составляет 75,3 кДж/моль, при катализе реакции платиной – 48,9 кДж/моль, а при ферментативном разложении – 23,0 кДж/моль. Рассчитать изменение констант скоростей. Задача № 2 Объясните, исходя из закономерностей ферментативного катализа, почему увеличение температуры тела на 5°С приводит, как правило, к необратимым изменениям, а снижение температуры даже на 10 °С (например, при хирургических операциях) – нет? |






