ПАТОГЕНЕЗ
В результате анализа значительного количества исследований стало очевидным, что развитие органно-системных повреждений при сепсисе, прежде всего, связано с неконтролируемым распространением из первичного очага инфекционного воспаления провоспалительных медиаторов эндогенного происхождения, с последующей активацией под их влиянием макрофагов, нейтрофилов, лимфоцитов и ряда других клеток в других органах и тканях, с вторичным выделением аналогичных эндогенных субстанций, повреждением эндотелия и снижением органной перегрузки и доставки кислорода.
Диссеминация микроорганизмов, может вообще отсутствовать или быть кратковременной, трудноуловимой. Однако, и в этот «проскок» способен запускать выброс провоспалительных цитокинов на дистанции от очага.
Суммарные эффекты, оказываемые медиаторами, формируют синдром системной воспалительной реакции. В ее развитии стали выделять три основных этапа:
1. Локальная продукция цитокинов в ответ на инфекцию. Особое место среди медиатров воспаления занимает сеть, которая контролирует процессы реализации иммунной и воспалительной реактивности. Основными продуцентами цитокинов являются Т-клетки и активированные макрофаги, а также в той или иной степени другие виды лейкоцитов, эндотелиоциты посткапиллярных венул, тромбоциты и различные типы стромальных клеток. Цитокины приоритетно действуют в очаге воспаления и на территории реагирующих лимоидных органов, выполняя в итоге ряд защитных функций, участвуя в процессах заживления ран и защиты клеток организма от патогенных микроорганизмов.
2-й этап. Выброс малого количества цитокинов в системный кровоток. Малые количества медиаторов способны активировать макрофаги, тромбоциты, выброс из эндотелия молекул адгезии, продукцию гормона роста. Развивающаяся острофазовая реакция контролируется провоспалительными медиаторами (ИЛ-1,6,8; ФНО и др.) и их эндогенными антагонистами, такими как ИЛ-4,10,13; растворимые рецепторы к ФНО и др., получивших название антивоспалительных медиаторов. За счет поддержки баланса и контролируемых взаимоотношений между про и антивоспалительными медиаторами, в нормальных условиях создаются предпосылки для заживления ран, уничтожения патогеных микроорганизмов, поддержки гомеостаза. К системным адаптационным изменениям при остром воспалении можно отнести стрессорную реактивность нейроэндокринной системы; лихорадку; выход нейтрофилов в циркуляцию из сосудистого и костно-мозгового депо; усиление лейкоцитоза в костном мозге; гиперпродукция белков острой фазы в печени; развитие генерализованных форм иммунного ответа.
3-й этап. Генерализация воспалительной реакции.
При выраженном воспалении или его системной несостоятельности некоторые виды цитокинов: ФНО-α, ИЛ – 1,6,10 могут запускаться в системную циркуляцию, накапливаться там в количествах достаточных эффектов. В случае неспособности регулирующих систем и поддержанию гомеостаза, деструктивные эффекты цитокинов и других медиаторов начинают доминировать, что приводит к нарушению проницаемости и функции эндотелия капилляров, запуску синдрома ДВС, формированию отдаленных очагов системного воспаления, развитию моно- и полиорганной дисфункции. В качестве факторов системного повреждения, по-видимому, могут выступать и любые нарушения гомеостаза, способные восприниматься иммунной системой как повреждающие или потенциально повреждающие на этой стадии ССВР с позиций взаимодействия про- и антивоспалительных медиаторов возможно условное выделение двух периодов. Первый, начальный, - период гипервоспаления, характеризующийся выбросами сверхвысоких концентраций провоспалительных цитокинов, окиси азота, что сопровождается развитием шока и ранним формированием СПОН. Однако уже в данный момент происходит компенсаторное выделение антивоспалительных цитокинов, скорость их секреции, концентрация в крови и тканях постепенно нарастает, с параллельным снижением функциональной активности иммунокомпетентных клеток – период «иммунного паралича». У некоторых больных в силу генетической детерминации или измененной под действием факторов внешней среды реактивности сразу регистрируется формирование устойчивой антивоспалительной реакции.
Грамположительные микрорганизмы не содержат в своей клеточной оболочке эндотоксины и вызывают септические рекции через другие механизмы. Запускающими септический ответ факторами могут являться компоненты клеточной стенки, гликокалекс, экзотоксины. В этой связи комплекс реакций в ответ на инвазию грамположительными микроорганизмами является более сложным.
Приложение № 4
ЦИТОКИНЫ В РАЗВИТИИ СИСТЕМНОЙ ВОСПАЛИТЕЛЬНОЙ РЕАКЦИИ
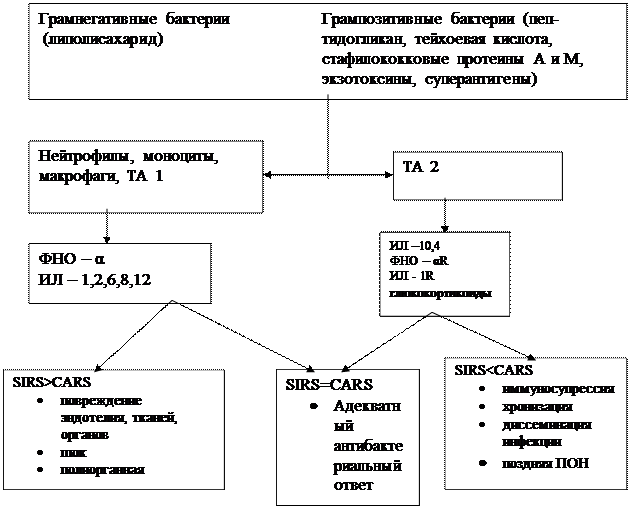 | |||
|
Приложение № 5
КРИТЕРИИ ДИАГНОСТИКИ СЕПСИСА И КЛАССИФИКАЦИЯ АССР/SССМ (1992) (согласительная конференция Американского колледжа пульмонологов и Общества специалистов критической медицины
| Патологический процесс | Клинико-лабораторные признаки |
| Синдром системной воспалительной реакции (SIRS) – системная реакция организма на воздействие различных сильных раздражителей | Характеризуется двумя или более из следующих признаков: - температура >38ºС или 36ºС< - ЧСС >90/мин - ЧД >20\мин или гипервентиляция (РаСО2 < 32 мм рт.ст) - Лейкоциты крови > 12 х 109\мл или 4х < 109/мл, или незрелых форм > 10% |
| Сепсис – синдром системной воспалительной реакции на инвазию микроорганизмов. | Наличие очага инфекции и 2-х или более признаков синдрома системного воспалительного ответа. |
| Тяжелый сепсис. | Сепсис сочетающийся с органной дисфункцией, гипотензией, нарушением тканевой перфузии. Проявлением последней, в частности, является повышение концентрации лактата, олигоурия, острое нарушение сознания. |
| Септический шок. | Тяжелый сепсис с признаками тканевой и органной гипоперфузии, и артериальной гипотонией, не устраняющейся с помощью инфузионной терапии и требующей назначения катехоламинов. |
| Дополнительные определения. | |
| Синдром полиорганной дисфункции. | Дисфункция по 2 и более системам. |
| Рефрактерный септический шок. | Сохраняющая артериальная гипотония, несмотря на адекватную инфузию, применение инотропной и вазопрессорной поддержки. |
Приложение № 6
КРИТЕРИИ ОРГАННОЙ ДИСФУНКЦИИ ПРИ СЕПСИСЕ
(A. Baue, E. Faist, D. Fray, 2000)
| Система/орган | Клинико-лабораторные критерии. |
| Сердечно-сосудистая система. | АДс< 90 мм рт.ст. или АДср< 70 мм рт.ст. в течение не менее 1 часа, несмотря на коррекцию гиповолемии. |
| Мочевыделительная система. | Диурез < 0,5 мг/кг/час в течение 1 часа при адекватном волемическом восполнении или повышение креатинина в 2р от нормы. |
| Дыхательная система. | РаО2/FiО2 < 250 или наличие билатеральных инфильтратов на R или необходимость проведения ИВЛ |
| Печень. | Увеличение содержания билирубина > 20 мкмоль/л в течение 2 дней или повышение уровня трансаминаз в 2 р. или более от нормы. |
| Свертывающая система. | Тромбоциты < 100 000 мм3 или их снижение на 50% от наивысшего значения в течение 3-х дней или увеличение протромбинового времени выше нормы. |
| Метаболическая дисфункция. | ph< 7,3 дефицит оснований > 5,0 мЭк/л лактат плазмы в 1,5 р. выше нормы. |
| ЦНС | Балл Глазго менее 15. |
Приложение № 7
КЛИНИКА СЕПСИСА:
Ведущая клиническая закономерность сепсиса – ацикличность – как непосредственное отражение септической иммунной недостаточности, проявляется неуклонным нарастанием тяжести общего состояния и появлением новых симптомов и синдромов в процессе развития болезни.
Выделяют четыре формы сепсиса:
Молниеносный сепсис, который развивается в течение 12-48 часов и который манифестируется клиникой септического шока.
Острый сепсис – начало в течение 7 дней, а продолжительность до 3 мес.
Подострый сепсис протекает от 3 до 6 месяцев и характеризуется периодами улучшений с периодами рецидивов симптомов сепсиса.
Хрониосепсис это септическое состояние, продолжающееся более 6 месяцев.
Каждая клиническая форма обладает оригинальной и достаточно сложной симптоматикой, на чем основывается клиническое распознавание.
Острейший сепсис регистрируется в пределах 1% общей септической заболеваемости. Хронический сепсис, в частности хронический септический инфекционный эндокардит, статистически может не причисляться к сепсису. Таким образом, основное количество септических заболеваний составляет острый сепсис.
При нелимитированном размножении возбудителя в первичном септическом очаге формируется острейший сепсис с катастрофическим нарастанием тяжести, развитием полиорганных дисфункций и инфекционно-токсического шока. Стафилококковый молниеносный сепсис это острая левожелудочковая сердечная недостаточность в первые сутки взрывоподобно начинает лихорадить. Если к этому добавить, что он с большим постоянством сопровождается острыми некрозами кожи, геморрагической сыпью, то этиологическая диагностика упрощается до примитивизма.
Грамотрицательный молниеносный сепсис, напротив – это инфекционно-токсический шок в первые же сутки лихорадки. Шок – обязательный клинический компонент острейшего сепсиса. Генерализованная форма менингококковой инфекции с инфекционно-токсическим шоком – клинический пример острейшего сепсиса.
При менее выраженной иммуносупрессии размножение возбудителя в первичном септическом очаге менее интенсивно, в связи с чем формируется менее злокачественный и более продолжительный вариант болезни – острый сепсис, который может развиваться в две стадии. Первая, начальная стадия острого сепсиса является септицемической. Далее процесс в соответствии с природой сепсиса развивается по нарастающей – возбудитель диссеминирует с формированием вторичных септических очагов и заболевание переходит во вторую заключительную септикопиемическую стадию острого сепсиса. При длительной персистенции возбудителя в первичном септическом очаге (например на клапанах сердца или иной локализации) формируется хронический сепсис. Симптоматика случаев хронического сепсиса развивается по общей септической закономерности и состоит из локальных проявлений и характерных признаков септического процесса. Продолжительность болезни месяцы и годы. Без противосепсисного лечения летальный исход неизбежен, чем подтверждается растянутая во времени септическая ацикличность.
Грибковый сепсис бывает либо вторичным, либо ассоциированным. Острейший грибковый сепсис не описан.
Неудовлетворительные результаты лечения инфекционного эндокардита в значительной мере обусловлены несвоевременностью установления диагноза. В 1985 г. Ослер писал: «Имеется мало болезней, которые представляли бы большие трудности на пути диагноза, чем злокачественный эндокардит. Многие опытные врачи указывают, что почти у половины больных диагноз поставлен после смерти». С тех пор прошло более 100 лет, но и в наши дни, несмотря на достижения современной медицины, проблема своевременной диагностики инфекционного эндокардита далека от разрешения.
Инфекционный эндокардит – это заболевание инфекционной природы, характеризующееся локализацией возбудителя на клапанах сердца, реже – на пристеночном эндокарде, и, сопровождающееся, как правило, бактериемией. В современных классификациях общепринято выделять острый и подострый инфекционный эндокардит. В ряде работ для разграничения этих двух форм рекомендуется ориентироваться на временной фактор (4-6 недель). Хотя такое деление весьма относительно, все же темпы прогрессирования заболевания и деструкция клапана значительно выше при острых формах. Острый эндокардит не диагностируется прижизненно в 60% случаев. Это связано, во первых, с тем, что особенность пороков сердца, образующихся при инфекционном эндокардите, заключается в преобладании недостаточности клапана над стенозом клапанного отверстия. Но при остром инфекционном эндокардите, а также на начальных стадиях подострого может иметь место лишь клапанный стеноз в результате тромботических наложений, которые находясь на аортальных створках, приводят к сужению устья аорты. Клинически это проявляется наличием систолического шума аортальной или в зоне Боткина-Эрба при отсутствии диастолического шума аортальной недостаточности. Об этом необходимо помнить, так как в ряде случаев на основании отсутствия шума аортальной недостаточности отвергается диагноз инфекционного эндокардита. Во-вторых, именно при остром инфекционном эндокардите часто наблюдается правосердечный вариант клапанных или пристеночных поражений., который обычно дает скудные аускультивные феномены, но очень часто осложняется тромбоэмболизацией в сосуды малого круга. Возникающая при этом легочная симптоматика зачастую расценивается как обычная пневмония.
Клинически острый инфекционный эндокардит характеризуется острым началом, гектической лихорадкой с ознобами, профузным потоотделением, бурным развитием симптоматики и быстрым (несколько недель и даже несколько дней) формированием порока сердца. В ОАК – гиперлейкоцитоз, выраженный палочкоядерный сдвиг, увеличение СОЭ до 70-80 мм/ч., быстрое снижение уровня гемоглобина за короткий срок.
Закономерное проявление острого инфекционного эндокардита – множественные пиемические очаги во внутренних органах, возникающие в результате гематогенного распространения тромбобактериальных эмболов.
Как показали недавние клинико-морфологические сопоставления, подострый инфекционный эндокардит может иметь два варианта течения: при первом заболевание развивается исподволь, постепенно, как первично-подострый инфекционый эндокардит, а в дальнейшем (нередко только через 3-5 месяцев) появляется высокая температура; при втором, заболевание дебютирует как острый процесс с гектической лихорадкой продолжительностью от нескольких дней до 1-1,5 месяцев, а в дальнейшем приобретает стертое течение с периодически возникающими рецидивами.
Подострый инфекционный эндокардит обычно развивается в порядке аутоинфекции, когда микробы распространяются из инфекционного очага по лимфатической системе, встречая на своем пути мощные барьеры в виде лимфатических узлов и ретикулоэндотелиального аппарата, так что организм успевает мобилизовать защитно приспособительные механизмы. В связи с этим, подострый инфекционный эндокардит имеет более доброкачественное течение.
Острый инфекционный эндокардит, как правило, является «второй болезнью» - осложнением различного по происхождению сепсиса, а подострый инфекционный эндокардит предстает перед клиницистом как самостоятельное заболевание.
Клинические критерии:
Большие критерии: положительная гемокультура из 2 раздельно взятых посевов, рост типичных для инфекционного эндокардита микроорганизмов, признаки патологии эндокарда по данным ЭхоКС – осциллирующие наложения на клапанах и подклапанных структурах, наличие клапанной регургитации, абсцессы клапанов.
Малые критерии: предшествующие заболевания сердца или внутривенное введение наркотиков, лихорадка с Т выше 38С, васкулиты, иммунологические феномены, артериальные эмболии или в легочной артерии при правосердечном, положительная гемокультура.
Из клинических критериев для определенного эндокардита необходимо присутствие 2 больших, или 1 большого и 3 малых критериев, или только 5 малых.
Критерии диагноза инфекционного эндокардита (Виноградова Т.Л.)
Клинические критерии:
1. Лихорадка свыше 38С.
2. Появление шума регургитации.
3. Спленомегалия.
4. Кожные васкулиты.
5. Ознобы.
Дополнительные критерии:
1. Гломерулонефрит.
2. Тромбоэмболии.
Параклинические критерии:
1. Положительная гемокультура.
2. Вегетации и клапанная деструкция, формирование регургитации, абсцессы клапанов по данным ЭхоКС.
3. повышение СОЭ более 30 мм/час.
4. Анемия.
Сочетание 2 основных критериев, одним из которых является шум регуртации с одним дополнительным, делает диагноз эндокардита вероятным даже при отсутствии параклинического подтверждения. Сочетание двух основных клинических критериев с одним дополнительным и не менее, чем с двумя параклиническими позволяет считать диагноз инфекционного эндокардита достоверным. Сочетание основных и дополнительных клинических и параклинических критериев, но без регуртации и положительных данных ЭхоКС, может говорить о возможном диагнозе инфекционного эндокардита, но не исключает и другие направления диагностического поиска.
Приложение № 8
ДИАГНОСТИКА СЕПСИСА
1. Наличие входных ворот:
- наличие очага инфекции или ситуации (в том числе и ятрогенной), которая могла привести к бактериемии.
2. Клиническая картина:
- гектическая лихорадка;
- потрясающие ознобы;
- проливные поты;
- бледность кожных покровов;
- геморрагические сыпи;
- гепатоспленомегалия;
- признаки септицемии.
Ацикличность течения.
- неуклонное нарастание тяжести общего состояния и появление новых симптомов и синдромов в процессе развития болезни.
4. Общий анализ крови:
- выраженные островоспалительные изменения;
- нарастающая анемия;
- увеличение СОЭ.
5. Иммунологические методы:
- НСТ-тест (однако, сложность интерпретации показателей иммуногомеостаза и их изменений при сепсисе заключается в отсутствии преморбидных характеристик состояния иммунитета, а также нарастающим угнетением его по мере нарастания тяжести септического состояния).
6. Исследование системы свертывания крови:
- истощение тромбоцитов;
- потребление факторов свертывания;
- вторичный фибринолиз.
7. Бактериологическое исследование крови:
Поскольку информация, полученная в результате посева крови, имеет важное прогностическое и тактическое значение, то у пациентов с впервые выявленной лихорадкой посевы крови всегда выполняются в тех случаях, когда у больного нет указаний на неинфекционные причины лихорадки.
Один посев крови – это образец, полученный в одно время и из одного места. Каждый посев осуществляется путем пункции отдельной вены. Высеваемость возбудителей в крови, полученной из артерии, такая же как и из вены, за исключением особого случая – инфекции артериального катетера. Получение двух посевов из двух разных вен с интервалом в 10 минут – наилучший способ определить, истинный это патоген (обычно оба посева положительны) или же контаминирующий организм (один положительный, второй отрицательный), к сожалению, нельзя назвать результаты этого метода абсолютно достоверными: как известно, бактериемия бывает интермиттирующей.
Сроки взятия проб крови: целесообразно во время лихорадочного периода (1) за 1 час предполагаемого подъема температуры, ориентируясь на температурную кривую предыдущих суток, (2) на высоте лихорадки и (3) через час после снижения температуры (как минимум 3 посева в сутки).
Условия и методика:
1) взятие крови проводят с соблюдением правил асептики стерильными одноразовыми шприцами;
2) запрещается проверять проходимость иглы, присасывая через нее воздух шприцем;
3) кровь берут у постели больного или в перевязочной и тут же засевают на питательные среды. Засеянные флаконы сразу должны быть доставлены в лабораторию или поставлены в термостат (t=37º). Забор крови из внутрисосудистых катетеров допускается в исключительных случаях и только с соблюдением правил 10 минутных интервалов.
4) для исследования необходимо взять кровь в соотношении 1:10 к объему питательной среды;
5) кожу над пунктируемой веной обрабатывают 70% спиртом, затем 5% настойкой йода и опять спиртом. Венопункцию проводят после полного высыхания дезинфектанта;
6) нельзя пальпировать вену в месте пункци;
7) -если флакон со средой закрыт ватно-марлевой пробкой, то процедуру рекомендуется осуществлять вдвоем: один мед.работник обрабатывает кожу больного, делает венопункцию и взятие крови, а второй в это время открывает над пламенем спиртовки пробки флаконов, подставляет их под струю крови из шприца (иглу со шприца надо снять и надеть стерильную), обжигает горлышки флаконов и закрывает их пробками;
-если флакон со средой закрыт герметично резиновый пробкой, то после ее обработки 70% спиртом в течение 1 мин. вносят кровь из шприца путем прокаливания пробки иглой (иглу сменить на стерильную).
- Эхокардиоскопия:
- наличие вегетаций, потоков регургитации;
- исследование проводится в динамике и особенно показано при отмене антибиотика.
- Прокальцитониновый тест:
Прокальцитонин – это предшественник гормона кальцитонин. Совершенно случайно было открыто, что при бактериальной инфекции повышается концентрация прокальцитонина в крови. Этот факт способствовал тому, что прокальцитонин стали использовать в качестве маркера бактериальных инфекций. Установлено, что после стимуляции ФНО или ИЛ-6 печеночная ткань человека продуцирует прокальцитонин в большом количестве.
Концентрация циркулирующего в крови прокальцитонина чрезвычайно низкая. У здоровых и доноров она определяется на уровне 0,01 нг/мл. При тяжелых бактериальных инфекциях он может возрастать от 20 до 200 нг/мг. Концентрация прокальцитонина в 1,6 нг/мл является пороговой для разделения лихорадок бактериальной и не бактериальной природы. Для больных с нейтропениями этот порог ниже: между 0,5 и 1 нг/мл. При тяжелых инфекциях высокие уровни, а особенно отсутствие снижения показателей прокальцитонина на фоне лечения антибиотиками, имеет серьезное прогностическое значение. С другой стороны, клиническому улучшению предшествует снижение показателей прокальцитонина.
- ИФА ВИЧ:
- по 113 коду.
- УЗИ органов брюшной полости, КТ (МРТ) структур черепа:
- поиск очагов отсевов.
Приложение № 9
Расширенные клинико-лабораторные критерии международной конференции экспертов (2001г.):
Инфекция, предполагаемая или подтвержденная в сочетании с несколькими
из следующих критериев:
Общие критерии
Лихорадка температура >38,3 С
Гипотермия температура <36,0 С
Частота сердечных сокращений >90/мин (>2 стандартных отклонений от нормального возрастного диапазона)
Тахипное
Нарушение сознания
Необходимость инфузионной поддержки (>20 мл/кг за 24 часа)
Гипергликемия (>7,7 ммоль/л) в отсутствие сахарного диабета
Критерии воспаления
Лейкоцитоз >12х10/л
Лейкопения <4х10/л
Сдвиг в сторону незрелых форм (>10%) при нормальном содержании лейкоцитов
Содержание С реактивного белка в крови >2 стандартных отклонений от нормы
Содержание прокальцитонина в крови >2 стандартных отклонений от нормы
Гемодинамические критерии
Артериальная гипотензия: АДсист(а)<90 мм рт. ст., или снижение АДсист более, чем на 40 мм рт. ст. (у взрослых) или снижение Адср. как минимум на 2 стандартных отклонения ниже возрастной нормы
Сатурация >70%
Сердечный индекс >3,5 л/мин/М2
Критерии органной дисфункции
Артериальная гипоксемия <300
Острая олигурия <0,5 мл/кг х час
Повышение креатинина более чем на 44 мкмоль/л
Нарушение коагуляции: АПТВ >60 сек. или МНО >1,5
Тромбоцитопения <100х10/л
Гипербилирубинемия >70 ммоль/л
Кишечная непроходимость (отсутствие кишечных шумов)
Индикаторы тканевой гипоперфузии
Гиперлактатемия >1 ммоль/л
Синдром замедленного заполнения капилляров,
Мраморность конечностей
Примечания:
АДсист - систолическое артериальное давление,
АДср - среднее артериальное давление,
АПТВ - активированное парциальное тромбопластиновое время,
МНО - международное нормализованное отношение
Приложение № 11
КРИТЕРИИ ДОКАЗАТЕЛЬСТВ ДЛЯ ОБОСНОВАННОСТИ ПРИМЕНЕНИЯ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ.
| Категория доказательств | Источник доказательств | Определение |
| А | Рандомизированные контролируемые исследования | Доказательства, основание на хорошо спланированных рандомизированных исследованиях, проведение на достаточном количестве пациентов, необходимом для получения достоверных результатов. Могут быть обоснованно рекомендованы для широкого применения. |
| В | Рандомизированные контролируемые исследования | Доказательства основаны на рандомизированных контролируемых исследованиях, однако, количество включенных пациентов недостаточно для достоверно статистического анализа. Рекомендации могут быть распространены на ограниченную популяцию. |
| С | Нерандомизированные контролируемые исследования | Доказательства основаны на нерандомизированных Клинических исследованиях или проведенных на ограниченном количестве пациентов. |
| Д | Мнение экспертов | Доказательства основаны на выработанном группой экспертов конценсуса. |
Приложение № 12
АНТИМИКРОБНАЯ ТЕРАПИЯ СЕПСИСА
Антимикробные средства являются важнейшим компонентом комплексной терапии сепсиса. В последние годы были получены убедительные данные, что ранняя адекватная эмпирическая антибактериальная терапия сепсиса приводит к снижению летальности и частоты осложнений (категория доказательности С). Адекватная антибактериальная терапия снижает летальность при сепсисе, вызванном грамотрицательными микроорганизмами (категория доказательности С), грамположительными микроорганизмами (категория доказательности Д) и грибами (категория доказательности С).
Антибиотики при сепсисе должны назначаться неотложно после уточнения нозологического диагноза и до получения результатов бактериологического исследования (эмпирическая терапия). После получения результатов бактериологического исследования режим антибактериальной терапии может быть скорректирован с учетом выделенной микрофлоры и ее антибиотикочувствительности.
Продолжительность антибактериальной терапии.
В общем виде критерии достаточности антибактериальной терапии сепсиса могут быть представлены следующим образом:
1. Стойкая нормализация температуры тела.
2. Положительная динамика основных симптомов инфекции.
3. Отсутствие признаков системной воспалительной реакции.
4. нормализация функции ЖКТ.
5. Нормализация количества лейкоцитов в крови и лейкоцитарной формулы.
Обычные сроки антибактериальной терапии хирургических инфекций различной локализации 5-10 дней.
Более длительные режимы (несколько недель) требуют остеомиелит, инфекционный эндокардит, вторичный гнойный менингит, а также инфекции, вызванные золотистым стафилококком.
Приложение № 13
РЕКОМЕНДАЦИИ ПО АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ СЕПСИСА С НЕСТАНОВЛЕННЫМ ПЕРВИЧНЫМ ОЧАГОМ
| Условия возникновения | Средства 1-го ряда | Альтернативные средства |
| Сепсис внебольничный | Левофлоксацин+/-метронизадол моксифлоксацин цефотаксим+/-метронидазол цефтриаксон+/-метронидазол | амоксициллин/клавуланат+/-аминогликозид ампициллин/сульбактам+/- аминогликозид офлоксацин+/- метронизадол перфлоксацин+/- метронизадол ципрофлоксацин±метронизадол |
| Сепсис нозокомиальный АРАСНЕ<15, без ПОН | цефепим+/- метронизадол цефоперазон /сульбактам | имипенем меропенем цефтазидим +/-метронизадол ципрофлоксацин+/-метронизадол |
| Сепсис нозокомиальный АРАСНЕ<15 и/или ПОН | имипенем меропенем | цефепим+/- метронизадол цефоперазон /сульбактам ципрофлоксацин+/-метронизадол |
Приложение № 15
РЕКОМЕНДАЦИИ ПО ЭТИОТРОПНОЙ ТЕРАПИИ СЕПСИСА
| Микроорганизмы | Средства 1-го ряда | Альтернативные средства |
| Золотистый стафилококк, оr | Оксациллин Цефазолин | Амоксициллин/клавуланат Клиндамицин Линкомицин Цефуроксим |
| Золотистый стафилококк, ОР, эпидермальный стафилококк | Ванкомицин Линезолид | Рифампицин+ципрофлоскацин Фузидиевая кислота + ципрофлоксацин |
| Зеленящий стрептококк | Ампициллин | Бензилпенициллин |
| Пневмококк | Цефотаксим Цефриаксон | Ампициллин Бензилпенициллин Имипинем Левофлоксацин Меропенем Моксифлоксацин Цефепим |
| Энтерококк фекалис | Ампициллин+гентамицин | Ванкомицин+/-гентамицин Линезолид |
| Энтерококк фециум | Линезолид | Ванкомицин+/-гентамицин |
| Кишечная палочка протей | Амоксициллин/клавуланаг Цефотаксим Цефтриаксон | Имипенем Меропенем Фторхинолон Цефепим |
| Клебсиелла пневмонии | Имипенем Меропинем Цефепим | Амикацин Цефоперазон/сульбактам Цефотаксим Цефтриаксон Ципрофлоксацин |
| Ацинетобактер | Имипенем Меропенем Цефоперазон/сульбактам | Ампициллин/ сультактам Цефтазидим + амикацин Ципрофлоксацин+амикацин |
| Синегнойная палочка | Меропенем Цефтазидим± амикацин Цефепим±амикацим | Имипенем Полимиксин Цефоперазон/ сульбактам + амикацин |
| Кандиды | Флюконазол | Амфотерицин В |
Приложение № 14
РЕКОМЕНДАЦИИ ПО АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ СЕПСИСА С УСТАНОВЛЕННЫМ ПЕРВИЧНЫМ ОЧАГОМ
| Характер инфекции | Средства 1 ряда | Альтернативные |
| Брюшная полость | ||
| Внебольничная | Амоксициллин/клавуланат +/-аминогликозид Цефотаксим+ метронидазол Цефтриаксон+ метронидазол | Ампициллин/сульбактам ± аминогликозид Левофлоксацин+ метронидазол Моксифлоксацин Офлоксацин+ метронидазол Цефуроксим+ метронидазол |
| Нозокомиальная АРАСНЕ < 15 без ПОН | Цефепим± метронидазол Цеферазон/ сультактам | Имипенем Левофлоксацин+ метронидазол Меропенем Цефтазидим+ метронидазол |
| Нозокомиальная АРАСНЕ >15 и/или ПОН | Имипенем Меропенем | Цефепим+метронидазол +/- Цефоперазон/сульбактам+/-амикацин Ципрофлоксацим+ метронидазол |
| Легкие | ||
| Нозокомиальная пневмония вне ОРИТ | Левофлоксацин Цефотаксим Цефтриаксон | Имипенем Меропенем Офлоксацин Пефлоксацин Цефепим Эртапенем |
| Нозокомиальная пневмония в ОРИТ, АРАСНЕ <15 без ПОН | Цефепим Цефтазидим + амикацин | Имипенем Меропенем Цефоперазон/ сульбактам± амикацин |
| Нозокомиальная пневммония ОРИТ, АРАСНЕ >15 и/или ПОН | Имипенем Меропенем | Цефепим± амикацин |
| Катетер ассоциированный | ||
| Ванкомицин Линезолид | Оксациллин+гентамицин Цефазолин+гентамицин Рифампицин+ципрофлоксацин | |
| ЦНС | ||
| Внебольничные | Цефотаксим Цефтриаксон | Пефлоксацин Хлорамфеникол |
| Нозокомиальные | Меропенем Цефепим | Хлорамфеникол Пефлоксацин |
| После спленэктомии | ||
| Внебольничный | Цефотаксим Цефриаксон | Имипенем Левофлоксацин Меропенем Цефепим |
| Почки | ||
| Внебольничный | Офлоксацин Цефотаксим Цефриаксон | Левофлоксацин Моксифлоксацин Ципрофлоксацим |
| Нозокомиальный | Левофлоксацин Офлоксацин Ципрофлоксацин | Имипенем Меропенем Цефепим |
| Кожа, мягкие ткани, кости | ||
| Укусы | Амоксициллин Клавуланат | Доксициклин |
| Некротизирующие инфекции | Имипенем Меропенем | Цефепим+клиндамицин Цефриаксон+ клиндамицин |
| С вовлечением костей | Имипенем Меропенем Цефепим+метронидазол или клиндамицин | Левофлоксацин+ метронидазол Цефотаксим+ клиндамицин |
| III уровень поражения (кожа, подкожная клетчатка, фасции, мышцы) | Амоксициллин/ клавуланат Левофлоксацин+ клиндамицин или метронидазол | Имипенем Меропенем Цефепим+ клиндамицин или метронидазол |
Приложение № 16
ИНТЕНСИВНАЯ ТЕРАПИЯ СЕПСИСА






