¬ыберите один правильный ответ
01. ћќЋя–Ќјя ќЌ÷≈Ќ“–ј÷»я ¬≈ў≈—“¬ј ¬ –ј—“¬ќ–≈ ѕќ ј«џ¬ј≈“
††† 1) ќтношение массы вещества к объему раствора
2) ќтношение количества вещества к массе раствора
3) ќтношение количества вещества к объему раствора
4) ќбъем вещества к объему раствора
02. “»“– –ј—“¬ќ–ј ќѕ–≈ƒ≈Ћя≈“—я ¬ –ј«ћ≈–Ќќ—“»
1) моль·дм-3
2) г·дм-3
3) г·см-3
4) моль·см-3
03. ћј——ј —”Ћ№‘ј“ј ћј√Ќ»я, —ќƒ≈–∆јўјя—я ¬ 500 ћЋ –ј—“¬ќ–ј — ћќЋя–Ќќ… ќЌ÷≈Ќ“–ј÷»≈… 0,2 ћќЋ№/Ћ, –ј¬Ќј
1) 12
2) 12000
3) 6000
4) 6
”становите соответствие
04. ќЌ÷≈Ќ“–ј÷»ќЌЌџ≈ ѕќЌя“»я » ≈ƒ»Ќ»÷џ »«ћ≈–≈Ќ»я:
| ќЌ÷≈Ќ“–ј÷»ќЌЌџ≈ ѕќЌя“»я | ≈ƒ»Ќ»÷џ »«ћ≈–≈Ќ»я |
| ј) ћол€рна€ масса вещества | 1) мг, г, кг |
| Ѕ) ћол€рна€ концентраци€ вещества в растворе | 2) безразмерна€ величина |
| ¬) ћол€рна€ масса эквивалента | 3) г/см3; г/мл |
| √) ѕлотность раствора | 4) см3, дм3, м3, мл, л |
| ƒ) оличество вещества | 5) г/моль |
| ≈) ћасса вещества | 6) моль·дм-3 |
| ∆) ћассова€ дол€ вещества в растворе | 7) % |
| «) ‘актор эквивалентности | 8) моль |
05. ќЌ÷≈Ќ“–ј÷»ќЌЌјя ’ј–ј “≈–»—“» ј –ј—“¬ќ–ј » —ќќ“¬≈“—“¬”ёў≈≈ ≈… ќѕ–≈ƒ≈Ћ≈Ќ»≈:
| ќЌ÷≈Ќ“–ј÷»ќЌЌјя ’ј–ј “≈–»—“» ј | ќѕ–≈ƒ≈Ћ≈Ќ»≈ ќЌ÷≈Ќ“–ј÷»ќЌЌќ… ’ј–ј “≈–»—“» » |
| ј) ’имический эквивалент Ц это Е | 1. число моль вещества в одном кубическом дециметре (литре) раствора. |
| Ѕ) ћассова€ дол€ растворЄнного вещества - это Е | 2. выражение 1/z, показывающее кака€ дол€ реальной частицы вещества соответствует эквиваленту. |
| ¬) ¬ о/в реакци€х число z это Е | 3. число отданных или прин€тых электронов. |
| √) ‘актор эквивалентности Ц это Е | 4. число моль эквивалента вещества в одном кубическом дециметре (литре) раствора. |
| ƒ) ћол€рна€ концентраци€ Ц это Е | 5. отношение массы растворЄнного вещества к объЄму раствора. |
| ≈) “итр Ц это Е | 6. отношение массы растворЄнного вещества к массе раствора. |
| ∆) ¬ обменных реакци€х число z это Е | 7. реальна€ или условна€ частица вещества, котора€ в обменной реакции эквивалентна одному протону, а в о/в реакции Ц одному электрону. |
| «) ћол€рна€ концентраци€ эквивалента вещества Ц это Е | 8. суммарный зар€д обменивающихс€ ионов. |
ƒополните высказывание
06. ћќЋя–Ќјя ћј——ј Ё ¬»¬јЋ≈Ќ“ј ќ—Ќќ¬јЌ»я ≈—“№ ќ“ЌќЎ≈Ќ»≈ ћќЋя–Ќќ… ћј——џ ќ—Ќќ¬јЌ»я „»—Ћ” _____________”„ј—“¬”ёў»’ ¬ –≈ј ÷»».
† 07. √ќћќ√≈ЌЌџ≈ (ќƒЌќ‘ј«Ќџ≈) —»—“≈ћџ ѕ≈–≈ћ≈ЌЌќ√ќ —ќ—“ј¬ј, —ќ—“ќяў»≈ »« ƒ¬”’ »Ћ» ЅќЋ≈≈ ќћѕќЌ≈Ќ“ќ¬ Ќј«џ¬јё“—я ______.
онтрольные задани€
08. ¬ простокваше, йогурте, кефире содержитс€ 0,6 Ц 1% молочной кислоты, котора€ обладает противомикробным действием. ¬от почему кисломолочные продукты широко рекомендуютс€ дл€ лечебного питани€. –ассчитайте мол€рную концентрацию молочной кислоты в этих продуктах (плотность раствора примите равной 0,99 г/мл). ††††††††
|
|
|
09. ¬ медицинской практике используют гормональный препарат адреналин в виде растворов. ¬ ампуле содержитс€ 1 мл 0,1%-ного раствора (ρ = 1 г/мл). ¬ычислите мол€рную концентрацию этого раствора и массу адреналина в 1 мл раствора, введенного в организм (ћадр = 219,7 г/моль).
10. ’лорид цинка используетс€ в качестве в€жущего и асептического средства. ќпределите мол€рную концентрацию, мол€рную концентрацию эквивалента, массовую долю и титр раствора, содержащего 5 г ZnCl2 в 100 г раствора (ρ = 1 г/мл).
Ћитература
1. ќбща€ хими€. ”чебник дл€ медицинских вузов / ¬. ј. ѕопков, —. ј. ѕузаков.Ц
ћосква.: ¬ысша€ школа, 2010 г.Ц —. 66 Ц73.
2. ѕрактикум по общей химии. Ѕиофизическа€ хими€. ’ими€ биогенных элементов: ”чеб. пособие дл€ студентов медицинских спец. вузов / ё.ј. ≈ршов, ј.ћ. ононов, —.ј. ѕузаков и др.; ѕод ред. ё.ј. ≈ршова, ¬.ј. ѕопкова. Ц ћосква.: ¬ысш. шк., 2008. Ц
†—.5 Ц 17.
¬¬≈ƒ≈Ќ»≈ ¬ “»“–»ћ≈“–»„≈— »… јЌјЋ»«. ћ≈“ќƒ Ќ≈…“–јЋ»«ј÷»»
¬ведение в титриметрический анализ
јналитическа€ хими€ Ц наука о методах определени€ качественного и количественного состава вещества или их смесей.
ачественный анализ позвол€ет определить, какие элементы, группы атомов, ионов, молекул, радикалов вход€т в состав анализируемого вещества или смеси веществ.
оличественный анализ позвол€ет установить количественные соотношени€ компонентов данного соединени€ или смеси веществ.
»сследу€ новое соединение, прежде всего, устанавливают, из каких компонентов оно состоит, а затем наход€т их количественные соотношени€. ѕоэтому качественный анализ вещества предшествует количественному. ≈сли качественный состав анализируемого материала известен, то приступают к количественному анализу, выбрав наиболее подход€щий метод.
¬ насто€щее врем€ аналитическа€ хими€ пользуетс€ многочисленными и разнообразными методами, которые подраздел€ют на физические, физико-химические и химические. ’имические методы, в свою очередь, включают гравиметрию (весовой анализ) и титриметрию (объемный анализ). ѕреимущество титриметрического анализа перед гравиметрическим состоит в быстроте определений.
¬ клинических лаборатори€х и лаборатори€х промсанхимии широкое распространение получил титриметрический анализ, так как дл€ его проведени€ требуетс€ простейшее лабораторное оборудование, не значительные затраты труда и времени, достаточно больша€ универсальность и высока€ точность.
“итриметрический анализ основан на измерении объема титранта (раствора точно известной концентрации), израсходованного на реакцию с определ€емым веществом, при этом вещества должны реагировать в строго эквивалентных количествах.
ѕроцесс постепенного добавлени€ титранта к анализируемому веществу называетс€ титрованием, а момент завершени€ реакции Ц моментом эквивалентности.
“итриметрическое определение вещества сводитс€ к проведению химической реакции смешиванием растворов двух реагирующих веществ. Ёта операци€ проводитс€ титрованием Ц добавлением небольших порций раствора одного из веществ к известному объему раствора второго вещества.
ќдин из двух растворов содержит вещество с неизвестной концентрацией и представл€ет собой анализируемый раствор. ¬торой раствор содержит реагент с точно известной концентрацией и называетс€ рабочим раствором или титрантом.
ƒл€ проведени€ титриметрического анализа необходимо:
|
|
|
1) знать точную концентрацию титранта;
2) точно измерить объемы растворов титранта и исследуемого вещества;
3) точно фиксировать момент эквивалентности.
ƒл€ точного измерени€ объемов растворов реагирующих веществ используют мерную посуду Ц бюретки, пипетки, мерные колбы и пр.
¬ процессе титровани€ достигаетс€ точка эквивалентности (момент эквивалентности), т. е. момент, когда количество вещества эквивалента в добавленном растворе титранта становитьс€ равным количеству анализируемого вещества.
’имические вещества реагируют между собой в определенных количественных соотношени€х. ”равнение реакции показывает минимальные целочисленные количества химических веществ, вступающих в реакцию, а так же образующихс€ в результате реакции. ¬ общем случае эти количества различны. ќднако дл€ удобства расчетов в химии используют особое пон€тие Ц химический эквивалент вещества, дающее возможность выразить количества реагирующих и образующихс€ веществ одинаковыми числами.
»з самого определени€ пон€ти€ химического эквивалента вытекает, что в химической реакции об€зательно участвует равное число эквивалентов двух веществ (кислоты и основани€, окислител€ и восстановител€ и т. д.).
–авными оказываютс€ и количества вещества эквивалента тех же веществ:
n(1/zT) = n(1/z’)
это равенство представл€ет собой математическое выражение закона эквивалентов. ¬ыразим количество вещества эквивалента через концентрацию и объем раствора:
n(1/z’) = —(1/z’) · Vх
n(1/zT) = —(1/zT) · Vт
—(1/z“) Ц мол€рна€ концентраци€ эквивалента титранта, моль/дм3
V(“) Ц объем титранта, см3
—(1/z’) Ц мол€рна€ концентраци€ эквивалента исследуемого вещества, моль/дм3
V(’) Ц объем раствора исследуемого вещества, см3
—(1/zT) ∙ V(T) = C(1/zX) ∙ V(X)
“аким образом, в момент эквивалентности число эквивалентов титранта и анализируемого вещества равны.
ѕо достижении точки эквивалентности титрование обычно заканчивают и отмечают затраченный объем раствора. —ледовательно, при выполнении титриметрического анализа необходимо располагать методом определени€ момента эквивалентности. ƒл€ этого используют свойства растворов, которые резко мен€ютс€ в точке эквивалентности.
ћомент эквивалентности определ€ют:
1) с помощью индикаторов;
2) по изменению окраски раствора одного из реагирующих веществ;
3) по прекращению выпадени€ осадка или изменению цвета осадка;
4) с помощью приборов, например, потенциометров, кондуктометров и пр.
«на€ точную концентрацию титранта —(1/z“), объем исследуемого раствора и объем раствора титранта V(“) в момент эквивалентности, можно легко рассчитать концентрацию раствора исследуемого вещества —(1/z’):

»з выше указанного уравнени€ можно определить титр раствора исследуемого вещества t(’):

¬ титриметрическом анализе могут использоватьс€ не все химические реакции, а только те, которые отвечают определенным требовани€м:
1) реакци€ должна быть практически необратимой;
2) реакци€ должна протекать быстро, в строгом соответствии с законом эквивалентов, без побочных процессов;
3) необходимо точно фиксировать момент эквивалентности.
–азнообразные методы титриметрического анализа можно классифицировать в зависимости от характера химической реакции, лежащей в их основе, и по способу проведени€ анализа.††††††††††††
»спользуют следующие основные типы химических реакций:
Ø ислотно-основное титрование Ч основано на взаимодействии кислот и оснований.
Ø ќксидиметри€ Ч основана на протекании окислительно-восстановительных реакций.
Ø ќсадительное титрование Ч основано на образовании осадков.
Ø омплексонометри€ Ч основана на реакци€х комплексообразовани€.
—ущность кислотно-основного титровани€ (метод нейтрализации)
¬ основе кислотно-основного титровани€ лежит соединение ионов Ќ3ќ+ и гидроксид-ионов ќЌ Ц †с образованием малодиссоциирующих молекул воды. ¬ упрощенном виде
Ќ+ + ќЌЦ ††= Ќ2ќ
|
|
|
ћетод позвол€ет определ€ть в растворах не только концентрацию кислот или оснований, но также и концентрацию гидролизующихс€ солей.
ƒл€ определени€ в растворах концентрации оснований или солей, дающих при протолизе щелочную реакцию, используют в качестве титранта растворы кислот. Ёти определени€ называют ацидиметрией (от лат. аcidum Ч кислота).
онцентрацию кислот и гидролитически кислых солей определ€ют с помощью титрантов растворов сильных оснований. “акие определени€ называют алкалиметрией (от лат. alkali Ц щелочь).
ѕоскольку реакци€ нейтрализации не сопровождаетс€ каким-нибудь внешним эффектом, например изменением окраски раствора, точку эквивалентности определ€ют с помощью индикаторов.
—огласно ионной теории индикаторов ќствальда (1894г.), индикаторы в методе кислотно-основного титровани€ представл€ют собой такие слабые органические кислоты или основани€, у которых недиссоциированные молекулы и ионы имеют различную окраску.
»ндикаторы, обладающие свойством присоедин€ть протоны, называют основными индикаторами и обозначают через IndOH, где Ind+ - катион индикатора. “акие индикаторы диссоциируют по схеме:

»ндикаторы, обладающие свойством отдавать протоны, называют кислотными индикаторами и обозначают через HInd. ћолекула такого индикатора играет роль донора протона, т. е. дает при диссоциации катион Ќ+ и анион IndЦ:
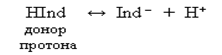
¬се индикаторы измен€ют свою окраску плавно в определенном интервале значений рЌ, называемом интервалом перехода, или зоной перехода окраски индикатора. ¬нутри зоны перехода имеетс€ такое значение рЌ, при котором индикатор наиболее резко измен€ет свою окраску. ¬ этот момент концентрации молекул€рной и ионной форм индикатора равны [HInd] = [IndЦ]. «начение рЌ, при котором индикатор наиболее резко мен€ет свою окраску, называетс€ показателем титровани€ (р“).
¬ табл. 1 указаны область перехода, показатель титровани€, окраска недиссоциированных молекул и анионов некоторых индикаторов.
“аблица1
’арактеристики некоторых индикаторов
| индикатор | область перехода рЌ | показатель титровани€ р“ | окраска недиссоциированных молекул | окраска анионов |
| метилоранж | 3,1 Ч 4,0 | 4,0 | красна€ | оранжево-желта€ |
| метилрот | 4,2 Ч 6,2 | 5,5 | красна€ | желта€ |
| лакмус | 5,0 Ч 8,0 | 7,0 | красна€ | син€€ |
| фенолфталеин | 8,0 Ч 10,0 | 9,0 | бесцветна€ | малинова€ |
≈сли упрощенно обозначить молекулы фенолфталеина через HInd, а анионы его через IndЦ, то уравнение диссоциации будет иметь вид

ƒостаточно к раствору, содержащему фенолфталеин, прибавить немного щелочи, как введенные ионы ќЌЦ станут св€зывать протоны с образованием малодиссоциирующих молекул воды. ѕри этом равновесие диссоциации индикатора сместитс€ вправо и накопление анионов IndЦ †вызовет окрашивание раствора в малиновый цвет.
Ќаоборот, если к раствору фенолфталеина прилить несколько капель кислоты, то повышение концентрации протонов будет подавл€ть диссоциацию молекул индикатора. –авновесие сместитс€ влево и раствор обесцветитс€. јналогичным образом объ€сн€ют поведение лакмуса, молекулы которого окрашены в красный цвет, а анионы в синий; нейтральные растворы лакмуса имеют промежуточную фиолетовую окраску. Ёто подтверждает, что цвет водного раствора индикатора зависит от соотношени€ между его молекул€рной и ионной формами.
“аким образом, окраска молекул индикаторов, обладающих кислотными свойствами, про€вл€етс€ в кислой среде, а окраска аниона Ч в щелочной.
¬ каждом конкретном случае кислотно-основного титровани€ индикатор подбираетс€ таким образом, чтобы показатель титровани€ его как можно точнее совпадал с истинным моментом эквивалентности.
|
|
|
Ќа правильный выбор индикатора вли€ет гидролиз солей, образующихс€ в процессе титровани€. –азличают четыре случа€ выбора индикаторов.
1. “итрование сильного основани€ сильной кислотой (или наоборот)
Ќапример: HCl + NaOH = NaCl + H2O
—оли катионов сильных оснований и анионов сильных кислот гидролизу не подвергаютс€, рЌ раствора 7, поэтому и момент эквивалентности будет при рЌ = 7. ƒл€ фиксировани€ момента эквивалентности в этом случае примен€ютс€ любые индикаторы с р“ = 7 (например, лакмус и др.)
2. “итрование сильной кислотой слабого основани€
Ќапример: HCl + NH4OH = NH4Cl + H2O
ќбразующа€с€ соль подвергаетс€ гидролизу: NH4+ + H2O ↔ NH4OH + H+
—реда раствора кисла€, рЌ < 7, поэтому и момент эквивалентности будет при рЌ < 7. ƒл€ фиксировани€ момента эквивалентности применимы любые индикаторы с р“ < 7 (например, метилоранж, метилрот и др.).
3. “итрование слабой кислоты сильным основанием
Ќапример: CH3COOH + NaOH = CH3COONa + H2O
ќбразующа€с€ соль подвергаетс€ гидролизу: —Ќ3—ќќ Ц †+ Ќ2ќ ↔ CH3COOЌ + OЌ Ц
—реда щелочна€, рЌ > 7, поэтому и момент эквивалентности будет при рЌ > 7. ƒл€ фиксировани€ момента эквивалентности применимы любые индикаторы с р“ > 7 (например, фенолфталеин и др.).
4. “итрование слабой кислоты слабым основанием (или наоборот)
Ќапример: NH4OH + CH3COOH = CH3COONЌ4 + H2O
“акое титрование практически не примен€етс€, т.к. соли катионов слабых оснований и анионов слабых кислот в растворах легко гидролизуютс€:
NH4+ + —Ќ3—ќќЦ †+ Ќ2ќ ↔ NH4OH + CH3COOЌ
¬ результате гидролиза образуютс€ слабые электролиты, среда раствора остаетс€ практически нейтральной, рЌ = 7. “ак как концентрации ионов Ќ+ и ќЌЦ в растворе мен€ютс€ незначительно, то они не оказывают существенного вли€ни€ на смещение индикаторного равновеси€. ¬ этом случае индикаторы свою окраску не измен€ют, следовательно, слабые кислоты слабыми основани€ми (или наоборот) точно не титруютс€.
Ѕолее точно выбор индикаторов провод€т по кривым титровани€.
ислотно-основное титрование примен€етс€ в клинических лаборатори€х при определении кислотности желудочного сока, буферной емкости крови, спинномозговой жидкости и пр., что используетс€ при постановке диагноза и лечении больных.
— помощью этого метода анализируютс€ лекарственные вещества, устанавливаетс€ доброкачественность пищевых продуктов (молока, хлеба, муки и др.). Ѕольшое значение метод нейтрализации имеет при санитарно-гигиенической оценке состо€ни€ окружающей среды (природных водоемов, почвы, промышленных стоков и др.).
онтрольные вопросы
1. ѕринципы титриметрического анализа.
2. лассификаци€ методов титриметрического анализа.
3. “итрование, требовани€ к реакци€м объемного анализа.
4. ћомент эквивалентности реакции, методы фиксировани€ момента эквивалентности.
5. «акон эквивалентов, количественные расчеты в объемном анализе.
6. —ущность метода нейтрализации. јцидиметри€. јлкалиметри€. ѕрименение метода в клинических и санитарно-гигиенических анализах.
7. »ндикаторы метода нейтрализации. »онна€ теори€ индикаторов ќствальда.
8. «она перехода окраски индикатора. ѕоказатель титровани€, его значение.
“иповые задачи
«адача 1.–ассчитайте объем (см3) раствора серной кислоты с массовой долей 26 % (плотность раствора 1,19 г/см3), необходимого дл€ приготовлени€ 150 см3 раствора серной кислоты с мол€рной концентрацией 0,2 моль/дм3.
| ƒано: | –ешение: |
| W(H2SO4) = 26 % | 1. ќпределить мол€рную массу серной кислоты: ћ(H2SO4) = 98 г/моль |
| ρ р(H2SO4) = 1,19 г/см3 | |
| V1(р-ра) = 150 см3 = 0,15 дм3 | 2. Ќайти массу вещества серной кислоты в 0,15 дм3 раствора с мол€рной концентрацией 0,2 моль/дм3: |
| —(H2SO4) = 0,2 моль/дм3 | |
| V2(р-ра) =? | m(H2SO4) = C(H2SO4) Ј M(H2SO4) Ј V1 = = 0,2 Ј 98 Ј 0,15 = 2,94 (г) |
|
3. Ќайти массу раствора серной кислоты с W (H2SO4) = 26 % ††††††††† m(H2SO4)††† †††††††††2,94 † mр = ---------------- Ј 100 = --------- Ј 100 = 11,3 (г) ††††††††† W(H2SO4)†††††††††††† 26†††††††††††††††††††††††
| |
| 4. Ќайти требуемый объем (см3) раствора серной кислоты: †††† mр†††† 11,3 V2 = ------- = --------- = 9,5 (см3) ††††† ρр†††† 1,19
| |
| ќтвет: V(H2SO4) = 9,5 см3 | |
«адача 2. –аствор кали€ перманганата примен€етс€ в медицине как дезинфицирующее средство. –ассчитайте титр раствора KMnO4, содержащего 0,02 моль кали€ перманганата в 250 см3 раствора.
| ƒано: | –ешение: | ||
| n(KMnO4) = 0,02 моль | 1. ќпределить мол€рную массу калий перманганата: | ||
| Vр = 250 см3 | ћ(KMnO4) = 158 г/моль | ||
| t(KMnO4) =? | †2. Ќайти массу вещества калий перманганата: | ||
| m(KMnO4) = n(KMnO4) Ј ћ(KMnO4) = 0,02 Ј 158 = 3,16 (г) | |||
| 3. ќпределить титр раствора калий перманганата:
†††††††††††††††††††† m(KMnO4)†† 3,16 t(KMnO4) = ------------------ = -------- = 0,01264 (г/см3) †††††††††††††††††††††††††† Vр†††††††††† 250 | |||
| ќтвет: t(KMnO4) = 0,01264 г/см3 | |||
«адача 3. –аствор натри€ сульфата примен€ют в медицине перрорально как слабительное средство. —колько граммов натрий сульфата необходимо дл€ приготовлени€ 200 см3 раствора с мол€рной концентрацией эквивалента —(½ Na2SO4) = 0,5 моль/дм3?
| ƒано: | –ешение: |
| —(½ Na2SO4) = 0,5 моль/дм3 | 1. ќпределить мол€рную массу эквивалента Na2SO4 |
| V р = 200 см3 = 0,2 дм3 | M (½ Na2SO4) = ћ(Na2SO4): 2 = 142: 2 = 71 г/моль |
| m(Na2SO4) =? | 2. Ќайти искомую массу натри€ сульфата: |
| m(½ Na2SO4) = C(½ Na2SO4) Ј M(½ Na2SO4) Ј Vр = = 0,5 Ј 71 Ј 0,2 = 7,1 (г) | |
| †††††††††††††††††††††††††††††††††††††††††† ќтвет: m(Na2SO4) = 7,1 г | |
«адача 4. ќпределите титр раствора натри€ гидроксида, если на тирование 5 см3 его раствора израсходовано 5,4 см3 раствора Ќ2SO4, с мол€рной концентрацией эквивалента —(½ Ќ2SO4) = 0,5 моль/дм3.
| ƒано: | –ешение: |
| V(NaOH) = 5 cм3 | 1. ќпределить мол€рную концентрацию эквивалента раствора натрий гидроксида, использу€ закон эквивалентов: —(NaOH) Ј V(NaOH) = C(½ Ќ2SO4) Ј V(½ Ќ2SO4) |
| V(Ќ2SO4) = 5,4 см3 | |
| —(½ Ќ2SO4) = 0,5 моль/дм3 | ††††††††††††††††††† ††††††††††††††† C(½ Ќ2SO4) Ј V(½ Ќ2SO4) 0,5 Ј 5,4†††††† моль —(NaOH) = ---------------------------------- = ---------- = 0,54 ------ †††††††††††††††††††††††††††† V(NaOH)†††††††††††††††††† 5††† †††††††††††дм3 |
| t(NaOH) =? | |
| 2. ќпределить титр раствора натрий гидроксида: †††††††††††††††† C(NaOH) Ј M(NaOH)†† 0,54 Ј 40 t(NaOH) = -------------------------------- = ------------- = 0,0216 (г/см3) †††††††††††††††††††††††††††††††† 1000 †††††††††††††††††††††1000
| |
| ќтвет: t(NaOH) = 0,0216 г/см3 | |






