Ќекоторых растворителей

ѕример 7. –аствор, содержащий 1,7 г ZnCl2 в 250 г воды, замерзает при -0,23 ∞—. ќпределить кажущуюс€ степень диссоциации хлорида цинка в этом растворе.
–ешение. ¬ычисл€ем понижение температуры замерзани€ данного раствора D “ замерз = 0 - (-0,23) = 0,23;  . ѕо формуле (7.13) с учетом (6.5) находим изотонический коэффициент:
. ѕо формуле (7.13) с учетом (6.5) находим изотонический коэффициент:
 ,
,
использу€ формулу (7.11), получаем  , или 73,65 %.
, или 73,65 %.
ѕример 8. ќпределить температуру кипени€ водного раствора едкого кали, содержащего в 100 г воды 14 г KOH. ажуща€с€ степень диссоциации KOH равна 60 %.
–ешение. ќпределим изотонический коэффициент по формуле (7.10) i = 1 + (2-1)×0,6 = 1,6. ћол€льность раствора найдем по формуле (6.5):  где 56 г/моль Ц мол€рна€ масса KOH. ƒл€ воды э = 0,516. ѕовышение температуры кипени€ раствора определим по формуле (7.14):
где 56 г/моль Ц мол€рна€ масса KOH. ƒл€ воды э = 0,516. ѕовышение температуры кипени€ раствора определим по формуле (7.14):
 ∞—.
∞—.
“емпература кипени€ раствора следующа€: 100 + 2,06 = 102,06 ∞—.
ѕример 9. ќсмотическое давление 0,1 н. ZnSO4 при 0 ∞— равно 1,59×105 ѕа. ќпределить кажущуюс€ степень диссоциации соли в данном растворе.
–ешение. онцентраци€ раствора ZnSO4 (в моль/л) равна 0,05, или 50 моль/м3. »з уравнени€ (7.15) дл€ растворов электролитов найдем изотонический коэффициент:
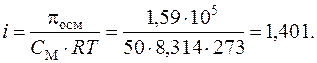
—оль ZnSO4 диссоциирует на два иона (n = 2). —огласно формуле (7.11)  или 40,1 %.
или 40,1 %.
ѕример 10. ќпределить концентрацию раствора глюкозы, если при 18 ∞— он изотоничен с раствором, содержащим 0,5 моль/л CaCl2. ажуща€с€ степень диссоциации хлорида кальци€ в растворе составл€ет 65,4 %.
–ешение. —огласно формулам (7.15) 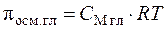 ,
,  . –астворы изотоничны, т. е. имеют одинаковое осмотическое давление:
. –астворы изотоничны, т. е. имеют одинаковое осмотическое давление:  ѕри диссоциации CaCl2 n = 3; a = 0,654, тогда по формуле (7.11) i = 1 + (n - 1) × a = 1 + (3 - 1) × 0,654 = 2,308, следовательно,
ѕри диссоциации CaCl2 n = 3; a = 0,654, тогда по формуле (7.11) i = 1 + (n - 1) × a = 1 + (3 - 1) × 0,654 = 2,308, следовательно, 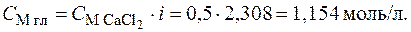
«јƒј„»*
7.1. ¬ каком случае эффективнее происходит распределение ионов электролита в этиловом спирте или в воде; в этиловом спирте или глицерине? ѕочему?
7.2. ќпределить теплоты гидратации 1 мол€ нитрата натри€ и 1 мол€ гидроксида натри€ и сравнить устойчивость гидратированных ионов.
ќтвет: -732,2 кƒж/моль; 933,1 кƒж/моль.
7.3. ќпределить теплоты гидратации 1 моль сульфата аммони€ и 1 моль сол€ной кислоты и сравнить устойчивость гидратированных ионов.
ќтвет: -1762 кƒж/моль; 1461 кƒж/моль.
7.4. ќпределить теплоту гидратации 1 моль гидроксида магни€ и 1 моль хлорида магни€ и сравнить устойчивость гидратированных ионов.
ќтвет: -2975 кƒж/моль; -2657 кƒж/моль.
7.5. Ќаписать уравнени€ диссоциации следующих соединений: KOH, H2SiO3, Al2(SO4)3, HF. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
7.6. Ќаписать уравнени€ диссоциации следующих соединений: Al(OH)3, CH3COOH, Fe(OH)2NO3, HI. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
7.7. Ќаписать уравнени€ диссоциации следующих соединений: H3PO4, RbOH, (NH4)2CO3, KHS. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
7.8. Ќаписать уравнени€ диссоциации следующих соединений: H2SeO4, NH4OH, FeCl3, HNO2. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
|
|
|
7.9. Ќаписать уравнени€ диссоциации следующих соединений: NaOH, H2S, NaHSO3, CuCl2. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
7.10. Ќаписать уравнени€ диссоциации следующих соединений: FeCl2, H2CO3, KHSO4, NH4OH. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
7.11. Ќаписать уравнени€ диссоциации следующих соединений: CrOH(NO3)2, CsOH, H2SiO3, ZnBr2. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
7.12. Ќаписать уравнени€ диссоциации следующих соединений: Ba(OH)2, H2Se, KAl(SO4)2, K2HPO4. ƒл€ слабых электролитов привести выражени€ констант диссоциации.
7.13. ¬о сколько раз уменьшитс€ концентраци€ ионов водорода, если к одному литру 0,005 ћ раствора уксусной кислоты добавить 0,05 мол€ ацетата натри€?
ќтвет: в 169 раз.
7.14. ¬ычислить степень диссоциации и концентрацию ионов водорода в 0,1 ћ растворе масл€ной кислоты.
ќтвет: 1,22 %, 1,2×10-3 моль/л.
7.15. ¬о сколько раз [H+] в растворе муравьиной кислоты больше, чем в растворе уксусной кислоты той же концентрации?
ќтвет: в 3,17 раза.
7.16. ѕри какой концентрации (в моль/л) фтороводородной кислоты 95 % ее находитс€ в недиссоциированном состо€нии?
ќтвет: 0,288 моль/л.
7.17. ¬ычислить a и [H+]: а) в 0,3 ћ растворе хлорноватистой кислоты HOCl и б) в 0,01 ћ растворе этой же кислоты.
ќтвет: a) 0,06 %, 1,7×10-4 моль/л; б) 1,73 %, 1,7×10-4 моль/л.
7.18. –ассчитать степень диссоциации уксусной кислоты в 1 ћ растворе. ак изменитс€ a, если этот раствор разбавить в 10 раз?
ќтвет: 0,42 %; увеличитс€ в 3,15 раза.
7.19. ¬ычислить осмотическое давление морской воды при 27 ∞—, если ее состав (в г/л) следующий: NaCl Ц 27,2; MgCl2 Ц 3,4; MgSO4 Ц 2,3; CaSO4 Ц 1,3; KC1 Ц 0,6. ажуща€с€ степень диссоциации указанных солей равна единице.
ќтвет: 2,77×106 ѕа.
7.20. ќсмотическое давление 0,05 ћ раствора электролита 2,72×105 ѕа при 0 ∞—. ажуща€с€ степень диссоциации электролита в растворе 70 %. Ќа сколько ионов диссоциирует молекула электролита?
ќтвет: на 3 иона.
7.21. акова концентраци€ (в % мас.) физиологического раствора поваренной соли, примен€емого дл€ внутривенного вливани€, если этот раствор изотоничен с плазмой крови, осмотическое давление которой равно 7,6×105 ѕа при нормальной температуре человеческого тела 37 ∞—? —читать, что соль полностью диссоциирована, плотность раствора соли прин€ть равной 1 г/см3.
ќтвет: 0,86.
7.22. ¬ычислить концентрацию водного раствора мочевины, если раствор при 27 ∞— изотоничен с 0,5 ћ раствора Ca—l2. ажуща€с€ степень диссоциации в 0,5 ћ —а—12 Ц 65,4 %.
ќтвет: 1,154 моль/л.
7.23. –аствор, содержащий 0,05 моль сульфата алюмини€ в 100 г воды, замерзает при -4,19 ∞—. ќпределить кажущуюс€ степень диссоциации соли в растворе.
ќтвет: 87,2 %.
7.24. »меютс€ растворы, содержащие в равных массах воды: первый Ц 0,25 моль сахара, второй Ц 0,13 моль хлорида кальци€. ќба раствора кип€т при одинаковой температуре. ќпределить кажущуюс€ степень диссоциации Ca—l2 в растворе.
ќтвет: 46,15 %.
7.25. ¬одный раствор, содержащий нелетучее растворенное вещество (неэлектролит), замерзает при -2,2 ∞—. ќпределить температуру кипени€ раствора и давление пара раствора при 20 ∞—. ƒавление пара чистой воды при 20 ∞— составл€ет 2337,8 ѕа.
ќтвет: 2289 ѕа, 100,61 ∞—.
7.26. ¬ычислить температуру замерзани€ раствора 7,308 г хлорида натри€ в 250 г воды, если при 18 ∞— осмотическое давление указанного раствора равно 2,1077×106 ѕа. ѕлотность раствора прин€ть за 1.
|
|
|
ќтвет: -1,667 ∞—.
7.27. ¬ычислить активность ионов Cu+2 и SO4-2 в 0,2 н. растворе CuSO4, содержащем, кроме того, 0,01 моль/л HCl.
ќтвет: по 0,015 моль/л.
7.28. ¬ 1 л раствора содержитс€ 0,1 моль NaCl и 0,1 моль NaOH. –ассчитать ионную силу раствора и активность иона натри€.
ќтвет: 0,2; 0,014 моль/л.
7.29. ¬ычислить ионную силу раствора и активность ионов: а) 0,05; ћ AgNO3; б) 0,003 ћ MgCl2.
ќтвет: а) 0,05, по 0,0405 моль/л; б) ~ 0,01; 0,002 и 0,005 моль/л.
7.30. ¬ычислить активность ионов Ca+2 и NO3- в 0,05 ћ растворе Ca(NO3)2, содержащем, кроме того, 0,05 моль/л HNO3.
ќтвет: 0,012, 0,105 и 0,035 моль/л.
–аздел 8. »онное произведение воды.
¬одородный показатель
∆идка€ вода €вл€етс€ сложной системой, дл€ которой характерно образование ассоциатов (H2O)n за счет водородных св€зей. ¬ода, будучи слабым электролитом, относитс€ к амфотерным растворител€м, молекулы которых могут служить как донорами, так и акцепторами протонов H+. ќна в незначительной степени диссоциирует на ионы водорода и гидроксид-ионы:
H2O ЂOH- + H+ (8.1)
онстанта диссоциации (самоионизации) воды определ€етс€ уравнением
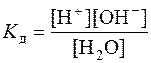 . (8.2)
. (8.2)
где в квадратных скобках указана концентраци€. Ѕолее точным выражением дл€ константы диссоциации K д €вл€етс€ уравнение с использованием активности ионов (a i), однако, здесь и далее будут использоватьс€ концентрации, так как в разбавленных растворах значени€ концентраций и активностей совпадают.
ѕри 25 ∞— константа диссоциации воды K д = 1,8×10-16. ѕлотность воды равна единице, откуда получим, что в 1 л воды содержитс€ количество воды  —ледовательно, [H2O] = 55,6 моль/л. “огда получим
—ледовательно, [H2O] = 55,6 моль/л. “огда получим
[H+][OH-] = K д× [H2O] = 1,0×10-14 = Kw .(8.3)
¬еличина w, равна€ произведению концентраций ионов водорода и гидроксид-ионов, называетс€ ионным произведением воды. ƒиссоциаци€ воды происходит с поглощением теплоты (процесс эндотермический), поэтому с увеличением температуры w возрастает. ѕри 100 ∞— w = 7,4 10-13. ѕри обычных услови€х (20Ц25 ∞—) величину w приближенно считают посто€нной и равной 1×10-14.
ислотность и щелочность растворов лучше всего характеризовать величиной концентрации ионов водорода и гидроксид-ионов. ¬ 1909 г. —ерензен предложил примен€ть вместо подлинных значений [H+] и [ќH-] их отрицательные логарифмы с обратным знаком Ц так называемые водородный и гидроксидный показатели.
¬одородный показатель pH:
pH = - lg[H+] (8.4)
гидроксидный показатель pOH:
pќH = - lg[ќH-] (8.5)
ќчевидно, что при 25 ∞— получим
pH + pOH = 14. (8.6)
ƒл€ чистой воды pH = pOH = 7. ¬ кислых растворах pH < 7, в щелочных pH > 7. ѕри расчетах pH и pOH следует иметь в виду, что под знаком логарифма сто€т не собственно концентрации, а равные им по значению безразмерные величины.
»змерение и регулирование величины рЌ среды €вл€етс€ необходимым при проведении различных технологических процессов, оценке качества почв в сельском хоз€йстве, а также при проведении исследовательских работ, особенно в области химии. ¬еличина рЌ природных, грунтовых и промышленных вод €вл€етс€ важнейшей экологической характеристикой, а также позвол€ет оценить веро€тность процессов коррозии строительных конструкций в подобных средах. Ќапример, при соприкосновении покрытых бетоном поверхностей с кислыми водными растворами возможно вымывание легкорастворимых солей, что приводит к разрыхлению структуры бетона. —ледует подчеркнуть особую роль кислотности среды в биологии и медицине. «начени€ рЌ крови и других биологических жидкостей существенно вли€ют на процессы жизнеде€тельности животных и растительных организмов. ¬еличины рЌ биологических систем наход€тс€ в узком диапазоне значений. Ќапример, рЌ крови колеблетс€ в области 7,35Ц7,45; рЌ молока Ц в интервале от 6,6 до 6,9; рЌ слюны Ц в области 6,35Ц6,85. ќтклонение от указанных пределов свидетельствует о наличии патологии в организме.
|
|
|
»змерение рЌ обычно производитс€ потенциометрическим методом. ¬ основе этого метода лежит определение электродвижущей силы (Ёƒ—) обратимого гальванического элемента, который состоит из электрода с водородной функцией, например стекл€нного и электрода сравнени€. ѕреимущества потенциометрического метода в том, что он позвол€ет производить измерени€ в мутных и загр€зненных растворах и характеризуетс€ относительной простотой приборного оформлени€. ќсновными элементами потенциометрической установки €вл€ютс€ гальванический элемент и измерительное устройство (иономер, рЌ-метр), работа которого основана на использовании компенсационного метода измерени€ Ёƒ—.
ислотность растворов можно приближенно оценить с помощью специальных реактивов Ц индикаторов. »ндикаторы Ц это вещества, которые могут измен€ть цвет при изменении рЌ среды. »ндикаторы представл€ют собой слабые кислоты или основани€ и отличаютс€ тем, что их молекул€рные и ионные формы имеют различную окраску. ѕереход от одной окраски к другой происходит в узком диапазоне рЌ. —войства некоторых индикаторов представлены в табл. 9.
“аблица 9






