—равнение изотермического реактора идеального вытеснени€ и реактора полного смешени€ в зависимости от степени превращени€
—ерна€ кислота €вл€етс€ одним из крупнотоннажных продуктов химической технологии. —ерна€ кислота относитьс€ к числу сильных кислот и €вл€етс€ самой дешЄвой. ќна реагирует почти со всеми металлами, вступает в реакции обменного разложени€. ѕочти половину всей вырабатываемой кислоты используют дл€ производства минеральных удобрений. “акже серную кислоту примен€ют в нефтехимической, металлургической отрасл€х промышленности, дл€ производства химических волокон, красителей, взрывчатых веществ и других продуктов.
ќкисление оксида серы (IV) €вл€етс€ второй стадией производства cерной кислоты. ѕо методу окислени€ оксида серы (IV) различают контактный и нитрозный способы производства серной кислоты. ¬ современных производствах окисление провод€т в присутствии твердого катализатора, и способ производства называют контактным. ѕри нитрозном способе катализатором служат оксиды азота. ќкисление провод€т в жидкой фазе с помощью нитрозы, выполн€ющей функции передатчика кислорода.
ќкисление оксида серы (IV) в оксид серы (VI) - основной процесс в производстве серной кислоты. ќкисление провод€т после тщательной очистки газа от пыли, тумана серной кислоты, контактных €дов и осушки.
–авновесие реакции окислени€ SO2 в соответствии с принципом Ће-Ўателье сдвигаетс€ в сторону образовани€ SO3 при понижении температуры и повышении давлени€. –авновесна€ степень превращени€ реагентов зависит также от соотношени€ SO2 и O2 в газе. Ќекаталитическое окисление оксида серы (IV) протекает столь медленно, что в производственных масштабах его проводить нецелесообразно. ѕоэтому процесс провод€т в присутствии катализаторов. ¬ сернокислой промышленности в разное врем€ примен€ли лишь три вида катализаторов, основу которых составл€ли металлическа€ платина, оксиды железа и оксид ванади€ (V). —амыми активными катализаторами €вл€ютс€ платиновые. ќднако из-за высокой чувствительности к контактным €дам, в частности к мышь€ковистым соединени€м, эти катализаторы уже давно не примен€ютс€.
атализаторы на основе оксидов железа практически не отравл€ютс€, но достаточную активность он про€вл€ет лишь при температуре выше 625—. ѕри такой температуре равновесна€ степень превращени€ не превышает 70%, и использование таких катализаторов возможно лишь дл€ так называемого предварительного окислени€ сернистого газа со степенью превращени€ 50-60%.
¬анадиевые катализаторы в услови€х работы представл€ют собой пористый носитель, внутренн€€ поверхность которого смочена пленкой раствора V2O5 в расплаве пиросульфата кали€.
¬ рамках данной работы мы рассматриваем 2 типа реакторов: реактор идеального вытеснени€ и реактор полного смешени€.
–еактор идеального вытеснени€. ѕри прохождении потока через данный реактор все частицы движутс€ с одной скоростью, не перемешива€сь друг с другом, то есть исходные реагенты не смешиваютс€ с продуктами реакции. ¬ каждом поперечном сечении потока концентрации их выровнены, но плавно измен€ютс€ по длине реакционной зоны. јналогично измен€етс€ скорость процесса.
|
|
|
ѕо условию задани€ мы используем изотермический температурный режим, который характеризуетс€ посто€нством температуры по всей длине реакционной зоны. ƒанный режим в реакторе идеального вытеснени€ наблюдаетс€ в случае протекани€ химико-технологического процесса без теплового эффекта или когда скорость тепловыделени€ (теплопоглощени€) мала, а теплопроводность среды в реакционной зоне высока.
Ќеобходимое врем€ пребывани€ реагентов в реакционной зоне рассчитывают по уравнению
называемому характеристическим уравнением реактора идеального вытеснени€.
–еактор полного смешени€. ѕри прохождении потока через данный реактор частица, поступающа€ в реакционную зону, мгновенно смешиваютс€ с частицами, уже наход€щимис€ в этой зоне, то есть равномерно распредел€ютс€ по всей длине и во всем объЄме зоны. ¬ результате во всех точках реакционной зоны мгновенно выравниваютс€ все параметры, характеризующие химико-технологический процесс.
¬следствие полного перемешивани€ выравниваетс€ и температура во всЄм объЄме реакционной зоны. “аким образом, химико-технологический процесс в потоке полного смешени€ может протекать только при изотермическом температурном режиме, независимо от значени€ теплового эффекта, концентрации и степени превращени€ исходных веществ.
¬рем€ пребывани€ частиц в реакционной зоне распределено не равномерно. —мешение исходных реагентов с продуктами реакции и неравномерность времени пребывани€ частиц в реакционной зоне приводит к уменьшению движущей силы процесса по сравнению с проведением его в потоке идеального вытеснени€.
это выражение называют характеристическим уравнением реактора полного смешени€. ÷елью данной работы €вл€етс€ сравнение изотермического реактора идеального вытеснени€ и реактора полного смешени€ в зависимости от степени превращени€, а также рассчитать производительность по исходному компоненту SO2.
»сходные данные
SO2 + 0,5O2 = SO3 -?H0
»сходные концентрации реагентов (мольна€ дол€):
—корость реакции рассчитываетс€ по выражению:
константа равновеси€:
–асчетна€ часть реактор идеальный вытеснение смешение
¬ывод
¬ результате проделанной работы мы вы€снили, что объЄм реактора идеального вытеснени€ меньше объЄма реактора полного смешени€ при одной и той же степени превращени€, то есть при одинаковой скорости реакции.
ѕроизводительность реакторов измен€етс€ от 0 до 9 м3/с с шагом 0,5 при соответственном изменении степени превращени€ SO2 от 0 до 0,9 с шагом 0,05.
ѕри увеличении степени превращени€ SO2 скорость реакции падает.
—техиометрические независимые уравнени€.
—техиоме́три€ (от др.-греч. στοιχεῖον Ђэлементї + μετρέω Ђизмер€тьї) Ч система законов, правил и терминов, обосновывающих расчеты состава веществ и количественных соотношений между массами (объЄмами дл€ газов) веществ в химических реакци€х. —техиометри€ включает нахождение химических формул, составление уравнений химических реакций, расчЄты, примен€емые в препаративной химии и химическом анализе[1][2][3].
ѕон€тие стехиометрии относ€т как к химическим соединени€м, так и к химическим реакци€м. —оотношени€, в которых, согласно законам стехиометрии, вступают в реакцию вещества, называют стехиометрическими, так же называют соответствующие этим законам соединени€. ¬ стехиометрических соединени€х химические элементы присутствуют в строго определенных соотношени€х (соединени€ посто€нного стехиометрического состава, они же дальтониды). ѕримером стехиометрических соединений могут служить вода Ќ2ќ, сахароза —12Ќ22ќ11 и практически все другие органические, а также множество неорганических соединений.
|
|
|
¬ то же врем€ многие неорганические соединени€ в силу разных причин могут иметь переменный состав (бертоллиды). ¬ещества, дл€ которых наблюдаютс€ отклонени€ от законов стехиометрии, называют нестехиометрическими [1]. “ак, оксид титана(II) имеет переменный состав[4], в котором на один атом титана может приходитьс€ от 0,65 до 1,25 атомов кислорода. Ќатриевольфрамова€ бронза[5] (относ€щийс€ к оксидным бронзам вольфрамат натри€) по мере удалени€ из неенатри€ мен€ет свой цвет от золотисто-желтого (NaWO3) до темного сине-зеленого (NaOХ3WO3), проход€ через промежуточные красный и фиолетовый цвета[6]. » дажехлорид натри€ может иметь нестехиометрический состав, приобрета€ синий цвет при избытке металла[7]. ќтклонени€ от законов стехиометрии наблюдаютс€ дл€конденсированных фаз и св€заны с образованием твЄрдых растворов (дл€ кристаллических веществ), с растворением в жидкости избытка компонента реакции илитермической диссоциацией образующегос€ соединени€ (в жидкой фазе, в расплаве).
≈сли исходные вещества вступают в химическое взаимодействие в строго определенных соотношени€х, а в результате реакции образуютс€ продукты, количество которых поддаетс€ точному расчету, то такие реакции называютс€ стехиометрическими, а описывающие их химические уравнени€ Ч стехиометрическими уравнени€ми. «на€ относительные молекул€рные массы различных соединений, можно рассчитать, в каких соотношени€х эти соединени€ будут реагировать. ћольные соотношени€ между веществами Ч участниками реакции показывают коэффициенты, которые называют стехиометрическими (они же коэффициенты химических уравнений, они же коэффициенты уравнений химических реакций)[8]. ≈сли вещества реагируют в соотношении 1:1, то их стехиометрические количества называют эквимол€рными.
“ермин Ђстехиометри€ї ввЄл ». –ихтер в книге ЂЌачала стехиометрии, или »скусство измерении химических элементовї (J. B. Richter. Anfangsgründe der Stöchyometrie oder Meßkunst chymischer Elemente. Erster, Zweyter und Dritter Theil. Breßlau und Hirschberg, 1792Ц93), обобщивший результаты своих определений масс кислот и оснований при образовании солей.
¬ основе стехиометрии лежат законы сохранени€ массы, эквивалентов, закон јвогадро, √ей-Ћюссака, закон посто€нства состава, закон кратных отношений. ќткрытие законов стехиометрии, строго говор€, положило начало химии как точной науке. ѕравила стехиометрии лежат в основе всех расчЄтов, св€занных с химическими уравнени€ми реакций и примен€ютс€ в аналитической и препаративной химии, химической технологии и металлургии.
«аконы стехиометрии используют в расчетах, св€занных с формулами веществ и нахождением теоретически возможного выхода продуктов реакции. –ассмотрим реакцию горени€ термитной смеси:
Fe2O3 + 2Al → Al2O3 + 2Fe.
—колько граммов алюмини€ нам необходимо дл€ завершени€ реакции с 85,0 граммами оксида железа (III)?
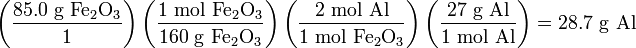
“аким образом, дл€ проведени€ реакции с 85,0 граммами оксида железа (III), необходимо 28,7 граммов алюмини€.






