1. ќпределите массу йода и объем спирта, необходимые дл€ приготовлени€ 300 г 10%-ного раствора йода (плотность спирта 0,8 г/мл).
2. —колько граммов хлорида железа (III) необходимо дл€ приготовлени€ 2 л 0,5Ќ раствора? ќпределите титр этого раствора.
3. ¬ычислите мол€рную концентрацию раствора, в 0,04 л которого содержитс€ 1,74 г сульфата кали€. ќпределите титр этого раствора.
4. ¬одный раствор содержит 577 г серной кислоты в 1 литре, плотность раствора 1,335 г/мл. ќпределить массовую долю серной кислоты.
5. ¬ычислите мол€рную концентрацию 15%-ного раствора сульфата меди, плотность которого 1,107 г/мл.
6. ѕлотность 1,4 ћ раствора серной кислоты составл€ет 1,085 г/мл. ¬ычислите массовую долю серной кислоты.
7. акое количество воды и нитрата кали€ необходимо дл€ приготовлени€ 400 г 20%-ного раствора?
8. ¬ычислите мол€рную концентрацию эквивалента (нормальность) 10%-ного раствора сульфата меди, плотность которого равна 1,107 г/мл.
9. ¬ычислите мол€рную концентрацию и мол€рную концентрацию эквивалента (нормальность) 16%-ного раствора хлорида алюмини€ плотностью 1,149 г/мл.
10. ќпределите мол€рную концентрацию раствора, полученного при растворении сульфата натри€ массой 42,6 г в воде массой 300 г, если плотность полученного раствора равна 1,12 г/мл.
11. ќпределите мол€рную концентрацию и мол€рную концентрацию эквивалента (нормальность) 47,7%-ного раствора фосфорной кислоты, плотность которого равна 1,315 г/мл.
12. ¬ычислите, какие массы 60%-ного раствора и воды потребуютс€ дл€ приготовлени€ 3 кг 10%-ного раствора некоторого вещества.
13. акой объем раствора серной кислоты плотностью 1,8 г/мл с массовой долей Ќ2SO4 88% надо вз€ть дл€ приготовлени€ раствора кислоты объемом 200 мл и плотностью 1,3 г/мл с массовой долей серной кислоты 40%?
14. ќпределить объем аммиака (услови€ нормальные), который необходимо растворить в 249 г воды дл€ получени€ 25%-ного раствора гидроксида аммони€.
15. ќпределить массу воды, в которой нужно растворить 188 г оксида кали€ дл€ получени€ 5,6%-ного раствора гидроксида кали€.
16. ќпределить массу 7,93%-ного раствора ќЌ, в котором нужно растворить 47 г оксида кали€ дл€ получени€ 21%-ного раствора ќЌ.
17. ќпределить мол€рную концентрацию раствора, полученного при смешении 200 мл 8 ћ и 300 мл 2 ћ растворов серной кислоты.
18. —колько граммов CuSO4 содержитс€ в 10,0 мл 0,20 ћ раствора? акова мол€рна€ концентраци€ эквивалента (нормальность) этого раствора?
19. —колько миллилитров 60%-ного раствора серной кислоты, плотность которого 1,5 г/мл, нужно вз€ть, чтобы приготовить 5,0 л 12%-ного раствора, плотность которого 1,08 г/мл?
20. —колько миллилитров 30%-ного раствора гидроксида кали€ с плотностью 1,29 г/мл нужно вз€ть, чтобы приготовить 3,0 л 0,50 ћ раствора?
21. ƒо какого объема нужно разбавить 20,2 мл 20%-ного раствора хлорида меди (II), плотность которого 1,20 г/мл, чтобы получить 0,05 ћ раствор?
22. 10 мл 12,8%-ного раствора хлорида бари€, плотность которого 1,12 г/мл, прибавлен раствор сульфата натри€, в результате чего выпал осадок сульфата бари€. ¬ычислите массу осадка.
|
|
|
23. 3,5 ћ раствору хлорида аммони€ объемом 30 мл и плотностью 1,05 г/мл прилили 40 мл воды (плотность воды 1,00 г/мл). ќпределите массовую долю соли в полученном растворе.
24. акой объем раствора с массовой долей карбоната натри€ 15% (плотность 1,16 г/мл) надо вз€ть дл€ приготовлени€ 0,45 ћ раствора карбоната натри€ объемом 120 мл?
25. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) NaHCO3 и NaOH; б) K2SiO3 и HCl; в) BaCl2 и Na2SO4.
26. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) K2S и HCl; б) FeSO4 и (NH4)2S; в) Cr(OH)3 и KOH.
27. —оставьте по три молекул€рных уравнени€ реакций, которые выражаютс€ ионно-молекул€рными уравнени€ми: а) Mg2+ + CO32- = MgCO3; б) H+ + OH- = H2O.
28. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) Ќ—ќ3 и H2SO4; б) Zn(OH)2 и NaOH; в) CaCl2 и AgNO3.
29. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) CuSO4 и H2S; б) BaCO3 и HNO3; в) FeCl3 и KOH.
30. —оставьте по три молекул€рных уравнени€ реакций, которые выражаютс€ ионно-молекул€рными уравнени€ми: а) Cu2+ + S2- = CuS; б) SiO32- + 2H+ = H2SiO3.
31. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) Sn(OH)2 и HCl; б) BeSO4 и KOH; в) NH4Cl и Ba(OH)2.
32. —оставьте молекул€рные уравнени€ реакций, которые выражаютс€ ионно-молекул€рными уравнени€ми: а) —а—ќ3 + 2Ќ+ = —а2+ + Ќ2ќ + —ќ2; б) Al(OH)3 + OHЦ = [Al(OH4)]Ц; в) Pb2+ + 2IЦ = PbI2.
33. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) Be(OH)2 и NaOH; б) Cu(OH)2 и HNO3; в) Zn(OH)NO3 и HNO3.
34. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) Na3PO4 и CaCl2; б) K2CO3 и BaCl2; в) Zn(OH)2 и KOH.
35. —оставьте молекул€рные уравнени€ реакций, которые выражаютс€ ионно-молекул€рными уравнени€ми: а) Fe(OH)3 + 2H+ = Fe3+ + 3H2O; б) Cd2+ + 2OHЦ = Cd(OH)2; в) H+ + NO2Ц = HNO2.
36. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) CdS и HCl; б) —r(OH)3 и NaOH; в) Ba(OH)2 и CoCl2.
37. —оставьте молекул€рные уравнени€ реакций, которые выражаютс€ ионно-молекул€рными уравнени€ми: а) Zn2+ + H2S = ZnS + 2H+; б) Ќ—ќ3Ц + Ќ+ = Ќ2ќ + —ќ2; в) Ag+ + ClЦ = AgCl.
38. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) H2SO4 и Ba (OH)2; б) FeCl3 и NH4OH; в) —Ќ3—ќќNa и HCl.
39. —оставьте молекул€рные и ионно-молекул€рные уравнени€ реакций взаимодействи€ в растворах между: а) FeCl3 и ќЌ; б) NiSO4 и (NH4)2S; в) MgCO3 и HNO3.
40. —оставьте молекул€рные уравнени€ реакций, которые выражаютс€ ионно-молекул€рными уравнени€ми: а) Be(OH)2 + 2OHЦ = BeO 22Ц + 2H2O; б) —Ќ3—ќќЦ + Ќ+ = —Ќ3—ќќЌ; в) Ba 2+ + SO 42Ц = BaSO4.
41. акие из веществ: NaCl, NiSO4, Be(OH)2, KHCO3, взаимодействуют с раствором гидроксида натри€. «апишите молекул€рные и ионно-молекул€рные уравнени€ этих реакций.
42. ѕроизведение растворимости сульфата кальци€ CaSO4 равно  . ¬ыпадет ли осадок, если смешать равные объемы 0,01Ќ раствора CaCl2 и 0,02Ќ раствора Na2SO4?
. ¬ыпадет ли осадок, если смешать равные объемы 0,01Ќ раствора CaCl2 и 0,02Ќ раствора Na2SO4?
43. –астворимость BaCO3 равна  моль/л. ¬ычислите произведение растворимости карбоната бари€.
моль/л. ¬ычислите произведение растворимости карбоната бари€.
|
|
|
44. ѕроизведение растворимости PbI 2 равно  . ¬ычислите концентрацию ионов Pb 2+ и ионов I Ц в насыщенном растворе иодида свинца.
. ¬ычислите концентрацию ионов Pb 2+ и ионов I Ц в насыщенном растворе иодида свинца.
45. ѕри t=  C в 1л насыщенного раствора иодида серебра AgI содержитс€ 0,044г соли. ¬ычислите произведение растворимости этой соли.
C в 1л насыщенного раствора иодида серебра AgI содержитс€ 0,044г соли. ¬ычислите произведение растворимости этой соли.
46. ¬ 0,6 л насыщенного раствора PbSO4 содержитс€ 0,186 г ионов свинца (II). ¬ычислите произведение растворимости этой соли.
47. ѕроизведение растворимости Ag3PO4 равно  . ¬ычислите концентрацию ионов Ag+ и PO4 3Ц в насыщенном растворе этой соли.
. ¬ычислите концентрацию ионов Ag+ и PO4 3Ц в насыщенном растворе этой соли.
48. ѕроизведение растворимости дихромата серебра Ag2Cr2O7 равно  . ¬ыпадет ли осадок при смешивании равных объемов 0,01Ќ растворов AgNO3 и K2Cr2O7?
. ¬ыпадет ли осадок при смешивании равных объемов 0,01Ќ растворов AgNO3 и K2Cr2O7?
49. ѕроизведение растворимости сульфата свинца ѕ– ( )=
)=  . ќбразуетс€ ли осадок, если к 0,1ћ раствору Na2SO4 прибавить равный объем 0,1Ќ раствора ацетата свинца Pb(CH3COO)2?
. ќбразуетс€ ли осадок, если к 0,1ћ раствору Na2SO4 прибавить равный объем 0,1Ќ раствора ацетата свинца Pb(CH3COO)2?
50. ¬ пробирке при комнатной температуре смешаны 1,0 мл 0,2Ќ раствора нитрата свинца и 2,0 мл 0,01Ќ раствора хлорида натри€. ¬ыпадет ли осадок, если ѕ– ( )=
)=  ?
?
51. ѕроизведение растворимости иодида серебра  . ќбразуетс€ ли осадок, если смешать равные объемы 0,02Ќ раствора KI и 0,04Ќ раствора AgNO3?
. ќбразуетс€ ли осадок, если смешать равные объемы 0,02Ќ раствора KI и 0,04Ќ раствора AgNO3?
52. ¬о сколько раз концентраци€ водородных ионов в 0,1Ќ растворе HCl  больше, чем в 0,01Ќ растворе HCl
больше, чем в 0,01Ќ растворе HCl  ?
?
53. —тепень диссоциации H3PO4 по первой ступени в 0,1ћ растворе равна 0,17. Ќе учитыва€ диссоциацию по следующим ступен€м, вычислите концентрацию водородных ионов в растворе.
54. —тепень диссоциации NH4OH равна 1,3%. —колько растворенных частиц (молекул и ионов) содержитс€ в 1л такого раствора?
55. ѕри какой мол€рной концентрации муравьиной кислоты HCOOH 95% ее молекул будут находитьс€ в недиссоциированном состо€нии, если ƒ = 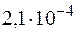 ?
?
56. онстанта диссоциации сероводородной кислоты по первой ступени ƒ =  . ќпределите концентрацию водородных ионов в 0,1 ћ растворе H2S.
. ќпределите концентрацию водородных ионов в 0,1 ћ растворе H2S.
57. ¬ычислите степень диссоциации азотистой кислоты в ее 0,01 ћ растворе и концентрацию ионов водорода в растворе, если ƒ = 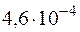 .
.
58. акова концентраци€ водородных ионов [H+] в 0,1Ќ растворе синильной кислоты HCN, если ее константа диссоциации ƒ =  ?
?
59. ќпределить степень диссоциации и концентрацию ионов [OHЦ] в 0,01Ќ растворе NH4OH, если ƒ =  .
.
60. онцентраци€ насыщенного при t= 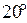 C раствора сероводородной кислоты H2S составл€ет 0,13 моль/л. онстанта диссоциации по первой ступени ƒ =
C раствора сероводородной кислоты H2S составл€ет 0,13 моль/л. онстанта диссоциации по первой ступени ƒ =  . ќпределите концентрации ионов [H+] и [HSЦ].
. ќпределите концентрации ионов [H+] и [HSЦ].
61. ¬ычислите степень диссоциации  и [H+] в 0,1 ћ растворе хлорноватистой кислоты, если ƒ =
и [H+] в 0,1 ћ растворе хлорноватистой кислоты, если ƒ = 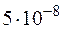 .
.






