–аздел химии, изучающий скорость и механизм химических реакций, называетс€ † химической кинетикой. † —коростью химической реакции †называетс€ изменение количества реа≠гирующего вещества за единицу времени в единице реакционного пространства. —корость химической реакции зависит от природы реагирующих веществ, их концентраций, температуры, давлени€ (в случае газообразных участников реакции) и присутстви€ катализатора.
«ависимость скорости от концентрации выражаетс€ основным законом химической кинетики Ц законом действи€ масс(дл€ простых реакций, протекающих в одну стадию в одном направлении в соответствии со стехиометрическим уравнением): при посто€нной температуре скорость химичес≠кой реакции пр€мо пропорциональна произведению концентраций реагирую≠щих веществ, возведенных в степени, равные их стехиометрическим коэф≠фициентам.
¬ общем случае дл€ реакции вида
а ј + b ¬ +... → m M + n N +...
математическое выражение закона имеет вид
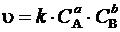 ,††††††††††††††††††††††††††††††††††† (10)
,††††††††††††††††††††††††††††††††††† (10)
где u Ц скорость химической реакции; k Ц коэффициент пропорциональ≠ности, называемый константой скорости реакции, который равен скорос≠ти реакции при единичных концентраци€х реагирующих веществ (т.е. при — A = — B = 1 моль/дм3, k = u); — A и
— B Ц концентрации реагентов, моль/дм3; а и b Ц стехиометрические коэффициенты.
онстанта скорости химической реакции k определ€етс€ природой реагирующих веществ и зависит от температуры и от присутстви€ катализатора. ¬ыражение (10) называетс€ кинетическим уравнением ре≠акции.
¬ химической кинетике реакцииклассифицируют по молекул€рности,т.е. по числу частиц, участвующих в элементарном взаимодействии, ипо пор€дку кинетического уравнени€ данной реакции (по пор€дку реакции). »з≠вестны одно-, двух- и трехмолекул€рные (моно-, би- и тримолекул€рные) реакции, например:
моно- †ј → ¬ + —; †† би- ††ј + ¬ → — †или †2ј → ¬ + —.
ѕор€дком химической реакции n называют сумму показателей степеней при концентраци€х реагентов в кинетическом уравнении. –азличают общий и частный (по каждому веществу) пор€дки реакции. ќбщий пор€док реакции есть сумма частных пор€дков. –еакции, скорость которых не зависит от концентрации, имеютнулевой пор€док.
ƒл€ реакции первого пор€дка уравнение дл€ расчета константы скорости реакции имеет вид
 , врем€-1,
, врем€-1,
где — Ц начальна€ концентраци€ вещества, моль/дм3; х Ц количество вещества, вступившего в реакцию к моменту времени τ.
«ависимость скорости гомогенной химической реакции от температуры определ€етс€ эмпирическим уравнением ¬ант-√оффа:
 ,
,
где u2 и u1 Ц скорости реакции при температурах “ 2 и T 1; γ Ц темпера≠турный коэффициент скорости реакции (дл€ большинства реакций †он лежит в пределах значений †2 Ц 4). ”казанна€ зависимость может быть выражена в виде следующего правила: при повышении температуры на каждые 10∞ скорость реак≠ции увеличиваетс€ в 2 Ц 4 раза, если реакци€ проводитс€ при температуре, близкой к комнатной.
|
|
|
«ависимость константы скорости реакции от температуры также может быть выражена уравнением јррениуcа:
 ,
,
где † ј Ц предэкспоненциальный множитель, не завис€щий от “ и концентрации; “ Ц абсолютна€ температура, ; ≈ ј Ц энерги€ активации, ƒж/моль.
Ёнерги€ активации равна тому избытку энергии, которым должны обладать молекулы реагентов по сравнению со средней энергией молекул при данной температуре, чтобы их столкновение приводило к химическому взаимодействию. ¬еличина ≈ ј химической реакции может быть рассчитана по уравнению јррениуса, если известны значени€ констант скоростей при разных температурах:
 ††††††††† †††††††††††††††(11)
††††††††† †††††††††††††††(11)
’имизм процесса окислени€ йодоводородной кислоты
пероксидом водорода
–еакци€ окислени€ йодоводородной кислоты пероксидом водорода выражаетс€ уравнением
2HI + Ќ2ќ2 Ѓ 2Ќ2ќ + I2.
оличество прореагировавшего пероксида водорода определ€етс€ эквивалентным количеством йода путем титровани€ последнего раствором тиосульфата натри€ †Na2S2ќ3:
I2 + 2Na2S2ќ3 †Ѓ 2NaI + Na2S4ќ6.
…одоводородную кислоту получают действием серной кислоты на йодиды, например KI или NaI:
2KI + H2SO4 Ѓ K2SO4 + 2HI.
“ак как в результате опыта концентрации KI и HI остаютс€ посто€нными, то скорость реакции в услови€х опыта зависит только от концентрации пероксида водорода. —ледовательно, дл€ вычислени€ константы скорости этой реакции можно применить уравнение первого пор€дка.
ѕор€док выполнени€ работы
ѕриборы и реактивы: термостат, секундомер, термометр, бюрет≠ка вместимостью 25 см3, колба мерна€ вместимостью 100 см3, колба кони≠ческа€ вместимостью 200 см3, пипетка ћора вместимостью 10 см3; растворы: серной кислоты — (H2SO4) = 1 моль/дм3; иодида кали€ или натри€ ω (KI; NaI) = 0,4 %; тиосульфата натри€ — (Na2S2ќ3) = 0,05 моль/дм3; пероксида водорода ω (H2ќ2) = l %; крахмала ω [(—6H10O5) x ] = 3 %; молибдата аммони€ C [(NH4)2Moќ4] = 0,1 моль/дм3.
’ о д ††р а б о т ы
1. ¬ коническую колбу вместимостью 250 см3 последовательно прилить следующие растворы:
а) 100 см3 раствора KI (раствор отмер€ют мерной колбой);
б ) 5 см3 раствора H2SO4 (раствор отмер€ют мерным цилиндром);
в) из бюретки прибавл€ют 1 см3 раствора Na2S2O3;
г) из капельницы внос€т 3 Ц 4 капли крахмала.
2. ¬ колбу поместить термометр и дождатьс€ момента, когда раствор в колбе примет заданное преподавателем значение температуры (если температура выше комнатной, то следует нагреть раствор на вод€ной бане, а если температура ниже комнатной, то необходимо охладить систему на лед€ной бане).
3. — помощью пипетки ћора к реакционной смеси прилить 10 см3 раствора Ќ2ќ2. —одержимое колбы перемешать. — последней каплей Ќ2ќ2 включить секундомер.
4. Ќе выключа€ секундомер, отметить текущее врем€ первого по€влени€ синего окрашивани€ раствора, записав его в таблицу формы 5.
5. раствору из бюретки снова прилить 1 см3 раствора Na2S2O3, смесь в колбе перемешать (окраска должна исчезнуть). ∆дать следующего по€влени€ синего окрашивани€ раствора.
6. Ќе выключа€ секундомер, снова отметить текущее врем€ по€влени€ синего окрашивани€ раствора и записать его в таблицу формы 5.
7. ѕрилить †ещЄ 1 см3 раствора Na2S2O3, перемешать и ждать следующего по€влени€ синего окрашивани€, отмеча€ врем€ по€влени€ окрашивани€ по часам. Ёти операции продолжать до тех пор, пока число измерений не станет равным 4 или 6 †в зависимости от температуры опы≠та (шесть раз при комнатной и при повышенной температурах, 4 раза при пониженной температуре).
|
|
|
8. ѕосле последнего по€влени€ синего окрашивани€ раствора отметить врем€ и выключить секундомер.
9. »з бюретки снова добавить 1 см3 раствора Na2S2O3 и 2 Ц 3 капли раствора молибдата аммони€, который €вл€етс€ катализатором данного процесса. —месь перемешать.
10. ѕолученный раствор оттитровать из бюретки раствором Na2S2O3 до †полного обесцвечивани€. «аписать общий объем тиосульфата натри€, пошедший на титрование в таблицу формы 5.
11. ѕолучить у преподавател€ †результаты титровани€ системы при другой температуре. ƒанные занести в таблицу формы 5.
‘орма 5
Ёкспериментальные и расчетные данные
| є опыта | “емпература опыта “, † | ќбъем Na2S2ќ3 х i , см3 | ќбщий объем Na2S2ќ3 V, см3 | ¬рем€ по€влени€ окрашивани€ от начала опыта, τ i | онстанта скорости реакции k, мин-1 | Ёнерги€ активации ≈ ј , кƒж/моль | ѕ, % | |||
| мин †и †с | мин | k i | 
| ≈ ј эксп | ≈ ј теор | |||||
| 1 2 | T 1 T 2 | x 1 = 1 x 2 = 2 x 3 = 3 Е. x 1 = 1 x 2 = 2 x 3 = 3 Е. | 55,0 | |||||||
ќбработка экспериментальных данных
1. ќтдельно дл€ каждого промежутка времени τ1, τ2, τ3 и т.д. с точностью до четвертого дес€тичного знака вычисл€ем константы скорости реакции по формуле

 , мин-1,
, мин-1,
где τ i Ц врем€ от начала опыта, мин; xi Ц объем раствора Na2S2ќ3, соответствующий τ i, см3; V Ц общий объем раствора Na2S2ќ3, пошедший на титрование, см3.
2. –ассчитываем среднее значение константы скорости данной реакции при заданной температуре опыта:
 ,
,
где m Ц †количество измерений времени по€влени€ синего окрашивани€ системы.
3. ѕо аналогии рассчитываем значение  †при другой температуре.
†при другой температуре.
4. ¬ычисл€ем энергию активации по формуле (11):
 .
.
5. ќпредел€ем относительную погрешность проведени€ опыта, счита€, что теоретическое значение энергии активации данной реакции 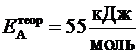 .
.
6. –асчетные данные заносим в таблицу формы 5.
7. ќформл€ем метрологическую карту средств измерени€ и формулируем выводы.
онтрольные задани€
¬ариант 1
1. ¬о сколько раз изменитс€ скорость гомогенной газовой реакции†
4HCl + O2 Ѓ 2H2O + 2Cl2,
если общее давление в системе увеличить в 3 раза?
2. ѕри какой температуре реакци€ закончитс€ за 45 мин, если при 293 на это требуетс€ 3 ч? “емпературный коэффициент скорости реакции прин€ть равным 3,2.
3. ѕри температуре 36 ∞— константа скорости распада пенициллина равна 6 Ј 10-6 †с-1, а при температуре 41 ∞— равна 1,2 Ј 10-5 †с-1. ¬ычислить энергию активации.
4. ¬ычислить константу равновеси€ реакции
Ќ2 + I2 Ђ2HI,
если до начала реакции в сосуде объемом 5 л содержалось 1 моль водорода и 2 моль йода, а к моменту равновеси€ образовалось 35 г HI.
¬ариант 2
1. ак измен€тс€ скорости реакций, если объем каждой из систем уменьшить в 4 раза?
а) Sтв + ќ2 Ѓ SO2 газ;
б) 2SO2 газ + ќ2 Ѓ 2SO3 газ.
2. ƒве реакции при 283 протекают с одинаковой скоростью. “емпературный коэффициент первой реакции равен †2,5, †а второй Ц 3,0. Ќайти соотношение скоростей данных реакций при температуре 350 .
3. ѕри 393 реакци€ заканчиваетс€ за 18 мин. „ерез какой промежуток времени эта реакци€ закончитс€ при 453 , если температурный коэффициент скорости реакции равен 3?
4. ¬ычислить константу равновеси€ реакции
Ќ2 + I2 Ђ2HI,
если до начала реакции в сосуде объемом 5 л содержалось 2 г водорода и 254 г йода, а к моменту равновеси€ образовалось 0,4 моль HI.
¬ариант †3
1. ¬о сколько раз следует увеличить концентрацию —ќ в системе, чтобы повысить скорость реакции ††2—ќ Ѓ —ќ2 + —тв в 4 раза?
|
|
|
2. ¬о сколько раз уменьшитс€ скорость реакции, если температуру понизить от 140 до 110 ∞—? “емпературный коэффициент скорости реакции прин€ть равным 3.
3. “емпературный коэффициент скорости реакции разложени€ йодоводорода по реакции
2HI = H2 + I2
равен 2. ¬ычислить константу скорости этой реакции при 684 , если при 629 константа скорости равна 8,9 Ј 10-5 л / (моль Ј с).
4. ¬ сосуд емкостью 0,2 л поместили 0,3 и 0,8 г водорода и йода. ѕосле установлени€ равновеси€ в сосуде обнаружено 0,7 г HI. ¬ычислить константу равновеси€ реакции.
¬ариант †4
1. ак изменитс€ скорость реакции
2NO + Cl2 Ѓ 2NOCl
при увеличении концентрации оксида азота в 2 раза и при увеличении концентраций обоих компонентов в 3 раза?
2. ѕри повышении температуры на 50 скорость реакции возросла в 1024 раза. ¬ычислить температурный коэффициент ¬ант-√оффа.
3. онстанта скорости реакции при температуре 9,4 ∞— равна 2,37 мин-1, а при температуре 14,4 ∞— составл€ет 3,204 мин-1. ¬ычислить энергию активации реакции.
4. —корость реакции
2NO + O2 → 2NO2
при концентраци€х NO и O2, равных 0,6 моль/дм3, составл€ет
0,18 моль/дм3 Ј мин. ¬ычислить константу скорости реакции.
¬ариант 5
1. —корость реакции при 40 ∞— равна 1 моль/(дм3 Ј c). ¬ычислить скорость этой реакции при 80 ∞—, если энерги€ активации реакции равна 74 кƒж/моль.
2. ак изменитс€ скорость реакции разложени€ карбоната кальци€ на оксид кальци€ и —ќ2 при уменьшении общего давлени€ в 4 раза?
3. Ќа сколько градусов необходимо повысить температуру, чтобы скорость реакции возросла в 90 раз? “емпературный коэффициент ¬ант-√оффа равен 2,7.
4. ¬ сосуде емкостью 8,5 л установилось равновесие
—ќ(г) + Cl2(г) ↔ —ќCl2(г).
—остав равновесной смеси (в г): —ќ Ц 11, Cl2 Ц 38, —ќCl2 Ц 42. ¬ычислить константу равновеси€ реакции.
¬ариант 6
1. Ќа сколько градусов нужно повысить температуру, чтобы увеличить скорость реакции в 64 раза, если температурный коэффициент реакции равен 2?
2. ак изменитс€ скорость реакции
2NO + Cl2 Ѓ 2NOCl
при уменьшении концентрации оксида азота в 3 раза и при уменьшении общего объема системы в 3 раза?
3. ѕри какой температуре реакци€ закончитс€ за 45 мин, если при 293 на это требуетс€ 3 ч? Ёнерги€ активации реакции равна 62 кƒж/моль.
4. «аписать выражение дл€ константы равновеси€ реакции
—ќ + Cl2 ↔ COCl2.
¬ариант 7
1. Ќа сколько градусов нужно повысить температуру, чтобы увеличить константу скорости реакции в 90 раз, если температурный коэффициент равен 2,7?
2. ¬ычислить скорость пр€мой реакции (моль/л Ј мин) при концентрации оксида азота (II) 0,6 моль/л и кислорода 0,5 моль/л, если константа скорости реакции
2Nќ + ќ2 = 2Nќ2
равна 0,56 л2/моль2 ∙ †мин.
3. Ёнерги€ активации реакции равна 103,5 кƒж/моль. ѕри 298 константа скорости данной реакции равна 0,00203 с-1. ¬ычислить константу скорости при температуре 288 .
4. ак изменитс€ скорость пр€мой реакции в системе
2SO2 + ќ2 → 2SO3 ,
если при “ = const увеличить давление в 3 раза?
¬ариант †8
1. ¬ычислить константу скорости реакции при 680 , если при 630 константа скорости данной реакции равна 8,9 ×
× 10-5 дм3/(моль Ј c) , а g = 2.
2. ак изменитс€ скорость пр€мого процесса при увеличении концентрации паров воды в 5 раз?
—ќ + Ќ2ќ(г) = Ќ2 + —ќ2.
3. ѕри повышении температуры на 27,8 ∞— скорость реакции возросла в 6,9 раза. ¬ычислить энергию активации этой реакции при температуре 300 .
|
|
|
4. ¬ какой из систем при повышении давлени€ скорость реакции возрастет в большее число раз?
а) N2 + O2 Ѓ 2NO;
б) 2NO + O2 Ѓ 2NO2.
¬ариант 9
1. онстанта скорости некоторой реакции при 273 и 298 равна, соответственно, 1,17 и 6,56 дм3/(моль Ј мин). Ќайти энергию активации реакции.
2. –авновесна€ концентраци€ оксида азота (II) в реакци膆†
N2 + ќ2 = 2Nќ
составл€ет 4 моль/л, а исходные концентрации азота и кислорода††† равны, соответственно, 6 и 5 моль/л. ќпределить равновесную концентрацию кислорода.
3. ѕри повышении температуры на 20 ∞— скорость реакции возросла в 9 раз. ¬ычислить температурный коэффициент скорости реакции и энергию активации этой реакции при температуре 300 .
4. ¬ какой из систем при повышении давлени€ скорость реакции возрастет в большее число раз?
а) N2 + O2 Ѓ 2NO;
б) 2NO + O2 Ѓ 2NO2.
¬ариант †10
1. ѕри 393 реакци€ заканчиваетс€ за 18 мин. „ерез сколько времени эта реакци€ закончитс€ при 453 , если энерги€ активации реакции равна 75 кƒж/моль?
2. ¬ каком направлении сместитс€ равновесие при увеличении концентрации паров воды в 10 раз?†
—ќ(г) + Ќ2ќ(г) ↔ Ќ2(г) + —ќ2(г).
3. ¬о сколько раз изменитс€ скорость реакции
2ј + ¬ → ј2¬,
если концентрацию вещества ј увеличить в 2 раза, а концентрацию вещества ¬ уменьшить в 2 раза?
4. ’имическа€ реакци€ при температуре 10 ∞C заканчиваетс€ за 16 мин. ѕри какой температуре она закончитс€ за 1 мин при температурном коэффициенте, равном 2?
¬ариант 11
1. ќпределить температурный коэффициент скорости реакции, если при понижении температуры на 45 реакци€ замедлилась в 25 раз.
2. ак изменитс€ скорость пр€мой реакции при уменьшении концентрации паров воды в 5 раз?†
—ќ(г) + Ќ2ќ(г) = Ќ2(г) + —ќ2(г).
3. онстанты скорости некоторой реакции при 288 и 325 равны, соответственно, 0,02 и 0,38 с-1. ќпределить энергию активации реакции.
4. ¬ычислить скорость пр€мой реакции (моль/л Ј мин) при концентрации оксида азота (II) 0,9 моль/л и кислорода 0,6 моль/л, если константа скорости равна 0,56 л2/моль2 ∙ мин:
2Nќ(г) + ќ2(г) = 2Nќ2(г).
¬ариант 12
1. ƒве реакции при температуре 293 протекают с одинаковой скоростью. “емпературный коэффициент первой реакции равен 2, а второй Ц 4. Ќайти соотношение скоростей данных реакций при температуре 500 .
2. «аписать выражение дл€ константы скорости реакции
N2 + 3Ќ2 ↔ 2NЌ3.
3. онстанта скорости реакции при 9,4 ∞— равна 2,37 мин-1, а при 14,4 ∞— составл€ет 3,204 мин-1. ¬ычислить энергию активации и температурный коэффициент скорости реакции.
4. ¬о сколько раз следует увеличить концентрацию —ќ в системе, чтобы повысить скорость реакции 2—ќ Ѓ —ќ2 + —тв в 8 раз?
¬ариант †13
1. Ќа сколько градусов необходимо повысить температуру, чтобы скорость реакции увеличилась в 50 и 100 раз, если температурный коэффициент скорости реакции равен 3?
2. ¬ каком направлении сместитс€ равновесие дл€ газовой реакции†
4HCl + O2 ↔ 2H2O + 2Cl2,
если общее давление в системе уменьшить в 3 раза?
3. ¬о сколько раз надо увеличить внешнее давление в системе, чтобы скорость пр€мой реакции ј(г) + 2¬(г) = —(г) увеличилась в 125 раз?
4. »сходные концентрации NO и Cl2 в гомогенной системе
2NO + Cl2 = 2NOCl
составл€ют, соответственно, 0,5 и 0,2 моль/дм3. ¬ычислить константу равновеси€, если к моменту равновеси€ прореагировало 35 % NO.
¬ариант 14
1. ¬ычислить температурный коэффициент скорости реакции разложени€ пероксида водорода в температурном интервале ††
25 Ц 55 ∞— при ≈а = 75,4 кƒж/моль.
2. ќпределить исходные концентрации NO и O2 и константу равновеси€ обратимой реакции
2NO + ќ2 Ђ2NO2,
если равновесие установилось при следующих концентраци€х реагирующих веществ (моль/дм3): [NO2] = 0,12; [NO] = 0,48; [O2] = 0,24.
3. ¬ системе —ќ + Cl2 = COCl2 концентрацию увеличили от 0,03 до 0,12 моль/л, а концентрацию хлора Ц от 0,02 до 0,06 моль/л. ¬о сколько раз возросла скорость пр€мой реакции?
4. ¬о сколько раз увеличитс€ скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70 ∞C, если температурный коэффициент скорости реакции равен 2?
¬ариант 15
1. ¬о сколько раз увеличитс€ скорость реакции, протекающей при температуре 298 , если энергию активации уменьшить на 4 кƒж/моль?
2. ¬ычислить среднюю скорость реакции
I2 + H2 Ѓ 2HI,
если в системе объемом 2 л †за 15 мин образовалось 0,12 г йодоводорода.
|
|
|
3. Ќа сколько градусов необходимо повысить температуру, чтобы скорость реакции увеличилась в 20 и 60 раз, если температурный коэффициент скорости реакции равен 2?
4. –еакци€ идет по уравнению
N2 + O2 → 2NO.
»сходные концентрации азота и кислорода равны 0,049 и 0,01 моль/дм3. ¬ычислить концентрации веществ, когда в системе образуетс€ 0,005 моль NO.
ѕ–»Ћќ∆≈Ќ»я
ѕриложение 1
“итульный лист
ћ»Ќ»—“≈–—“¬ќ ќЅ–ј«ќ¬јЌ»я » Ќј” » –ќ——»…— ќ… ‘≈ƒ≈–ј÷»»






