| Ќазвание индикатора | pK | ќбласть перемены окраски,pH | ќкраска | |
| »ндикатор-кислота | »ндикатор-основание | |||
| 1. ћетиловый-оранжевый | 3,7 | 3,0-4,4 | красный | жЄлта€ |
| 2. Ѕром-феноловый синий | 4,1 | 3,0-4,6 | жЄлта€ | сине-фиолетова€ |
| 3. онго красный | 4,2 | 3,0-5,2 | сине-фиолетова€ | красный |
| 4. ћетиловый красный | 5,1 | 4,4-6,2 | красный | жЄлта€ |
| 5. n-Ќитрофенол | 7,0 | 4,7-7,9 | бесцветна€ | жЄлта€ |
| 6. Ћакмус | 7,0 | 5,0-8,0 | красный | син€€ |
| 7. Ѕромтимоловый синий | 7,1 | 6,0-7,6 | жЄлта€ | син€€ |
| 8. “имоловый синий | 8,9 | 8,0-9,6 | жЄлта€ | син€€ |
| 9. ‘енолфталеин | 9,7 | 8,2-10,0 | бесцветна€ | малинова€ |
| 10.Ќейтральный красный | 7,3 | 6,8-8,0 | красный | €нтарно-жЄлта€ |
“аблица 3.
ѕроизведение растворимости некоторых соединений
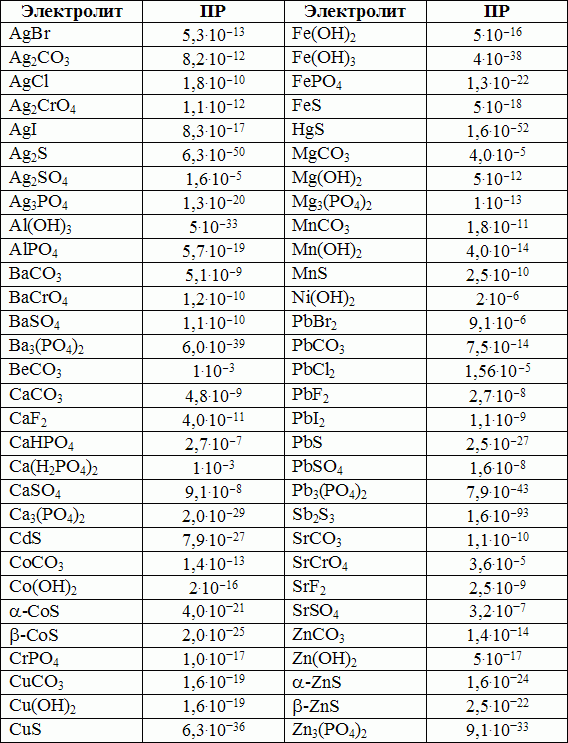
“аблице 4
—тандартные электродные потенциалы в водных растворах при 250—
| є п/п | электрод | реакци€ | φ0,¬ |
| Ёлектроды, обратимые относительно катиона | |||
| 1 | H+,H | H+ + ē = H | Ц2,106 |
| 2 | Al3+,Al | Al3+ + 3ē = Al | Ц1,662 |
| 3 | Zn2+,Zn | Zn2+ + 2ē = Zn | Ц0,763 |
| 4 | Fe2+,Fe | Fe2+ + 2ē = Fe | Ц0,440 |
| 5 | Cd2+,Cd | Cd2+ + 2ē = Cd | Ц0,403 |
| 6 | Ni2+,Ni | Ni2+ + 2ē = Ni | Ц0,250 |
| 7 | Sn2+,Sn | Sn2+ + 2ē = Ni | Ц0,136 |
| 8 | Pb2+,Pb | Pb2+ + 2ē = Pb | Ц0,126 |
| 9 | Fe3+,Fe | Fe3+ + 3ē = Fe | Ц0,036 |
| 10 | H+,H2 | H+ + ē = ½H2 | 0,000 |
| 11 | Cu2+,Cu | Cu2+ + 2ē = Cu | 0,337 |
| 12 | Cu+,Cu | Cu+ + ē = Cu | 0,521 |
| 13 | Ag+,Ag | Ag+ + ē = Ag | 0,799 |
| 14 | Hg22+,Hg | ½ Hg22+ + ē = Hg | 0,798 |
| Ёлектроды, обратимые относительно аниона | |||
| 15 | O2, OHЦ | 1/2O2 + H2O + 2ē = 2OHЦ | 0,401 |
| 16 | Br2(ж),Br Ц | 1/2Br2 + ē = BrЦ | 1,065 |
| 17 | Cl2(г) ,Cl | 1/2Cl2 + ē = ClЦ | 1,360 |
| Ёлектроды второго рода | |||
| 18 | Al, Al(OH)3, OHЦ | Al(OH)3 +3ē = Al + 3OHЦ | Ц2,30 |
| 19 | Zn, Zn(OH)2, OHЦ | Zn(OH)2+ 2ē =Zn + 2OHЦ | Ц1,245 |
| 20 | Cd, Cd(OH)2, OHЦ | Cd(OH)2+ 2ē =Cd + 2OHЦ | Ц0,809 |
| 21 | Ag, AgCl, ClЦ | AgCl + ē= Ag + ClЦ | 0,222 |
| 22 | Hg, Hg2Cl2, ClЦ | 1/2Hg2Cl2 + ē = Hg + ClЦ | 0,268 |
| 23 | Ag, Ag2SO4, SO42Ц | Ag2SO4 + 2ē = Ag + SO42Ц | 0,654 |
| 24 | Pb, PbSO4, SO42Ц | PbSO4 + 2ē = Pb + SO42Ц | Ц0,359 |
| ќкислительноЦвосстановительные электроды | |||
| 25 | Sn4+, Sn2+(Pt) | Sn4+ + 2ē = Sn2+ | 0,15 |
| 26 | Cu2+, Cu+(Pt) | Cu2+ + ē = Cu+ | 0,153 |
| 27 | Fe3+, Fe2+(Pt) | Fe2+ Ц ē = Fe3+ | 0,771 |
“аблица 5.
онстанты нестойкости комплексных ионов.
| омплексный ион | н. |
| [Ag(NH3)2]+ | 9,3∙10Ц8 |
| [Cu(NH3)4]2+ | 2,1∙10Ц13 |
| [Zn(OH)4]2Ц | 3,6∙10Ц16 |
| [Fe(CN)6]3Ц | 1,0∙10Ц31 |
| [Fe(CN)6]4Ц | 1,0∙10Ц36 |
“аблица 6.
«начени€ констант диссоциации некоторых кислот
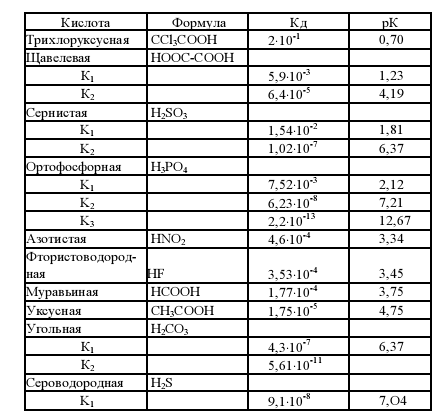

“аблица 7.
«начение р а некоторых органических соединений
|
|
|
| ислота | р а |
| ’лорна€ јзотна€ —ол€на€ —ерна€ Ѕензолсульфокислота “ринитрометан | <0 —ильные кислоты |
| ѕикринова€ “рихлоруксусна€ ўавелева€ —ерниста€ ‘осфорна€ ’лоруксусна€ јзотиста€ Ѕензойна€ ”ксусна€ ѕиридиний-катион Ћимонна€ —ероводородна€ Ѕорна€ јммоний-ион ‘енол Ќитрометан Ётилмеркаптан ¬ода Ётиловый спирт јцетон јнилин јммиак “олуол ћетан | 0,4 0,7 1,2 1,8 2,1 2,9 3,3 4,2 4,7 5,2 5,4 7,2 9,2 9,2 9,9 11,0 12,0 14,0 18,0 20,0 27,0 30,0 35,0 40,0 |
—ѕ»—ќ Ћ»“≈–ј“”–џ
- јналитическа€ хими€ и физико-химические методы анализа [“екст]: учебник дл€ студентов, обуч. ѕо хим.-технол. Ќаправлени€м и спец.: в 2т. “.1/ё.ћ. √лубоков [и др.]; под ред. ј.ј. »щенко. Ц ћ.: јкадеми€, 2010.-352с.: ил.-(¬ысшее профессиональное образование. ’имические технологии).
2. ѕопков ¬.ј. ќбща€ хими€ [Ёлектронный ресурс]: учебник/ ѕопков ¬.ј., ѕузаков —.ј. - ћ.: √Ёќ“ј– Ц ћедиа, 2010, 976 с. Ц –ежим доступа: http: //studmedlib.ru
3. —аенко ќ.≈. Ђјналитическа€ хими€ї [“екст]: учебник дл€ сред. спец. учеб. заведений/ќ.≈. —аенко.-»зд. 2-е допю и перераб.- –остов. н/ƒ. Ђ‘ениксї, 2011-288с.: ил.- (—реднее профессиональное оьразование).
4. ’аритонов ё.ј., √ригорьева ¬.ё. јналитическа€ хими€.[Ёлектронный ресурс] ѕрактикум. ачественный химический анализ: учеб. пособие/ ё.ј. ’аритонов, ¬.ё. √ригорьева. Ц ћ.: √Ёќ“ј– Ц ћедиа, 2009. -296с. - –ежим доступа: http: //studmedlib.ru
5. ’аритонов ё.ј., √ригорьева ¬.ё. ѕримеры и задачи по аналитической химии [Ёлектронный ресурс]: учеб. пособие/ ё.ј. ’аритонов, ¬.ё. √ригорьева. Ц ћ.: √Ёќ“ј– Ц ћедиа, 2009. -296с. - –ежим доступа: http: //studmedlib.ru
ƒЋя «јѕ»—≈…






