¬ариант є 4
1. ќпределите, во сколько раз увеличитс€ скорость реакции, если температура возрастет от 10о— до 50о—. “емпературный коэффициент равен 3.
ќтвет: скорость реакции увеличитс€ в 81 раз.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ продуктов реакции:
2SO2(г) + ќ2(г) ↔2Sќ3(г); ΔHо>0.
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мых реакций и химического равновеси€ и рассчитайте равн при превращении 20% исходных веществ:
а) NO(г) + NO2(г) + O2(г) ↔2N2O5(т) †
б) CO(г) + Cl2(г) ↔—ќCl2(г)
в) Cl2(г) + H2(г) ↔ 2HCl(г)
¬ариант є 5
1. ќпределите, во сколько раз увеличитс€ скорость реакции, если температура возрастет от 10о— до 50о—. “емпературный коэффициент равен 4.
ќтвет: скорость реакции увеличитс€ в 256 раз.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ продуктов в реакции и рассчитайте равн при превращении 40% исходных веществ:†
MgO(к) + CO2(г) ↔MgCO3(к); ΔHо<0.
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мых реакций и химического равновеси€:
а) 2CO(г) ↔CO2(г) + C(к)
б) 2NO(г) + Cl2(г) ↔2NOCl (г)
в) 2SO2(г) + ќ2(г) ↔2Sќ3(г)
¬ариант є 6
1. ќпределите, на сколько градусов необходимо увеличить температуру, чтобы скорость реакции увеличилась в 64 раз. “емпературный коэффициент равен 2.
ќтвет: температуру необходимо увеличить на 60о—.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ продуктов реакции:†
—S2(г) + 2H2S(г) ↔ CH4(г) + 4S(т); DHо <0
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мых реакций и химического равновеси€ и рассчитайте равн при превращении 30% исходных веществ:
а) CO2(г) + C(к) ↔2CO(г)
б) 2Ќ2(г) + O2(г) ↔2Ќ2O(г)
в) 3H2(г) + N2(г) ↔ 2NH3(г)
¬ариант є 7
1. –ассчитайте, температурный коэффициент химической реакции, если при увеличении температуры на 40о— скорость реакции увеличилась в 81 раз.
ќтвет: температурный коэффициент равен 3.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ исходных веществ в системе: NH3(г) + HCl(ж) ↔ NH4Cl(ж); DHо>0
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мых реакций и химического равновеси€ и рассчитайте равн при превращении 20% исходных веществ:
а) 2NO(г) + SO2(г) ↔ N2O(г) + SO3(г)
б) Br2(г) + H2(г) ↔2HBr(г)
в) —(тв) + 2Ќ2(г) ↔—Ќ4(г)
¬ариант є 8
1. ќпределите, во сколько раз увеличитс€ скорость реакции, если температура возрастет от 10о— до 30о—. “емпературный коэффициент равен 4.
ќтвет: скорость реакции увеличитс€ в 16 раз.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ продуктов реакции:
2NO(г) + SO2(г) ↔N2O(г) + SO3(г); DHо<0
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мых реакций и химического равновеси€ и рассчитайте равн при превращении 50% исходных веществ:
|
|
|
а) NH3(г) + HCl(ж) ↔NH4Cl(ж)
б) Fe3O4(к) + 4Ќ2(г) ↔3Fe(к) + 4Ќ2ќ(г)
в) 2NO(г) + O2(г) ↔2NO2(г)†
¬ариант є 9
1. ќпределите, во сколько раз увеличитс€ скорость реакции, если температура возрастет от 20о— до 50о—. “емпературный коэффициент равен 2.
ќтвет: скорость реакции увеличитс€ в 8 раз.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ продуктов в реакции:†
2SO2(г) + O2(г) ↔ 2SO3(г); ΔHо<0.
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мых реакций и химического равновеси€ и рассчитайте равн при превращении 30% исходных веществ:
а) 2NO(г) + O2(г) ↔2NO2(г)†
б) —S2(г) + 2H2S(г) ↔CH4(г) + 4S(т)
в) 2NH3(г) ↔N2(г) + 3H2(г)
¬ариант є 10
1. ќпределите, во сколько раз увеличитс€ скорость реакции, если температура возрастет от 10о— до 50о—. “емпературный коэффициент равен 3.
ќтвет: скорость реакции увеличитс€ в 81 раз.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ продуктов в реакции:†
MgO(к) + CO2(г) ↔MgCO3(к); ΔHо<0.
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мых реакций и химического равновеси€ и рассчитайте равн при превращении 40% исходных веществ:
а) 2NO(г) + SO2(г) ↔N2O(г) + SO3(г)
б) Br2(г) + H2(г) ↔2HBr(г)
в) —(тв) + 2Ќ2(г) ↔—Ќ4(г)
ќбразец выполнени€ письменных заданий:
1. ќпределите, на сколько градусов была повышена температура некоторой реакции, если известно, что скорость реакции увеличилась в 16 раз, а температурный коэффициент равен 2.
–ешение:
†¬ уравнение ¬ант-√оффа
†††††††††††††††††††††††††††††††††††††††† 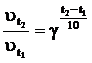
подставим известные значени€ и рассчитаем изменение температуры:

ќтвет: температура увеличитс€ на 40o—.
2. ќбоснуйте, при изменении каких факторов равновесие можно сместить в сторону образовани€ продуктов в реакции:†
—(т) + Ќ2ќ(г) ↔Ќ2(г) + —ќ(г); DЌо>0
ќтвет:
¬ соответствии с принципом Ће Ўателье равновесие можно сместить в сторону образовани€ продуктов реакции при:
1) †повышении температуры, т.к. пр€ма€ реакци€ €вл€етс€ эндотермической (DЌо>0);
2) †понижении давлени€, т.к. в результате пр€мой реакции число газообразных частиц возрастает;
3) †повышении концентрации исходного вещества Ќ2ќ или понижении концентрации одного из продуктов реакции Ќ2 или —ќ.
3. Ќапишите выражение закона действующих масс дл€ скорости пр€мой реакции и химического равновеси€:
CuO(к) + H2(г) ↔Cu(к) + H2O(г)
ќтвет:
ƒл€ скорости реакции Ц V = k∙C(H2)
ƒл€ химического равновеси€ Ц 
††††††††††††††††††††††††††††††††††††††††††††††††††††††††
“ема 4.
–астворы, способы выражени€ состава растворов.
ѕриготовление растворов с заданным содержанием растворенного вещества.
¬опросы дл€ самосто€тельной внеаудиторной подготовки к зан€тию:
1. ќбщие пон€ти€: раствор, растворитель, растворенное вещество.
2. –астворимость. Ќазовите факторы, от которых зависит растворимость веществ.
3. ѕроцесс растворени€ веществ. »з каких стадий состоит процесс растворени€? „то называетс€ тепловым эффектом растворени€?
4. „то называетс€ насыщенным, ненасыщенным и пересыщенным растворами? аковы услови€ их получени€? ћожет ли быть насыщенный раствор разбавленным, а концентрированный Ц ненасыщенным? ѕриведите примеры.
|
|
|
5. Ќазовите известные вам способы выражени€ количественного состава растворов.
»зучив эти вопросы, выполните письменно следующие задани€:
¬ариант є 1
1. раствору массой 250 г с w(соли) = 10% добавили эту же соль массой 15 г. –ассчитайте массовую долю соли в полученном растворе.
ќтвет: 15,09 %.
2. —мешали раствор массой 200 г с w(щелочи) = 1% с раствором массой 50 г с w(щелочи) = 4%. ¬ычислите массовую долю щелочи в полученном растворе.†††
ќтвет: 1,6%.
3. –ассчитайте объем воды, который необходимо добавить к раствору объемом 500 мл с w(NaOH) = 40% (r = 1,43 г/мл) дл€ приготовлени€ раствора с w(NaOH) = 10%.
ќтвет: 2,15 л.
¬ариант є 2
1. раствору массой 300 г с w(ZnSO4) = 5% добавили сульфат цинка массой 20 г. –ассчитайте массовую долю ZnSO4 в полученном растворе.†††
ќтвет: 10,94%.
2. —мешали раствор массой 150 г с w( ќЌ) = 5% с раствором массой 200 г с w( ќЌ) = 10%. ¬ычислите массовую долю щелочи в полученном растворе.††††
ќтвет: 7,86%.
3. –ассчитайте объем воды, который необходимо добавить к раствору объемом 0,5 л с массовой долей серной кислоты 20% (r = 1,143 г/мл) дл€ приготовлени€ раствора с w(H2SO4) = 12%.†††††††††††††††††††††††
ќтвет: 381 мл.
¬ариант є 3
1. раствору массой 450 г с w(NaCl) = 3% добавили эту же соль массой 25 г. –ассчитайте массовую долю NaCl в полученном растворе.†††††
ќтвет: 8,10%.
2. —мешали раствор массой 300 г с массовой долей растворенного вещества 2% с раствором массой 140 г с массовой долей растворенного вещества 6%. ¬ычислите массовую долю этого вещества в полученном растворе.†††
ќтвет: 3,27%.
3. –ассчитайте объем воды, который необходимо добавить к раствору объемом 250 мл с w(HNO3) = 30% (r = 1,205 г/мл) дл€ приготовлени€ раствора с w(HNO3) = 25%.
ќтвет: 60,25 мл.
¬ариант є 4
1. раствору массой 150 г с w( ќЌ) = 10% добавили 5 г гидроксида кали€. –ассчитайте массовую долю ќЌ в полученном растворе.
ќтвет: 12,9%.
2. —мешали раствор массой 60 г с массовой долей растворенного вещества 2% с раствором массой 150 г с массовой долей растворенного вещества 5%. ¬ычислите массовую долю этого вещества в полученном растворе.†††
ќтвет: 4,14%.
3. акую массу воды нужно добавить к раствору массой 125г с w(NaCl) = 8%, чтобы получить раствор этой соли с массовой долей 5%?††
ќтвет: 75 г.
¬ариант є 5
1. —мешали раствор массой 300 г с w(NaCl) = 20% с раствором массой 500 г с w(NaCl) = 40%. ¬ычислите массовую долю хлорида натри€ в полученном растворе.†††
ќтвет: 32,5%.
2. –ассчитайте массу воды, которую надо добавить к раствору массой 20 г с w(Ќ2SO4) = 70% дл€ получени€ раствора с w(Ќ2SO4) = 3%.
ќтвет: 446,67 г.
3. акой объем раствора с w(ЌCl) = 5% (r = 1,023 г/мл) можно получить из раствора объемом 103,9 мл с w(ЌCl) = 30%
(r = 1,149 г/мл)?
ќтвет: 700,18 мл.
¬ариант є 6
1. акую массу воды нужно добавить к раствору серной кислоты массой 40 г с w(H2SO4) = 20%, чтобы получить раствор с w(H2SO4) = 8%?
ќтвет: 60 г.
2. акой объем раствора серной кислоты с w(H2SO4) = 90% (r = 1,82 г/мл) нужно вз€ть дл€ приготовлени€ раствора объемом 50 мл с w(H2SO4) = 50% (r = 1,40 г/мл)?
ќтвет: 21,37 мл.
3. ¬ растворе массой 500 г с w(CuSO4) = 4% растворили 25 г медного купороса (CuSO4∙5H2O). –ассчитайте массовую долю сульфата меди(II) в полученном растворе.
ќтвет: 6,86%.
†††††††
¬ариант є 7
1. ака€ масса Na2SO3 потребуетс€ дл€ приготовлени€ раствора объемом 5 л с w(Na2SO3) = 8% (r = 1,075 г/мл)?
ќтвет: 430 г.
2. акую массу кристаллогидрата FeSO4∙7H2O и какой объем воды надо вз€ть дл€ приготовлени€ раствора массой 500 г с массовой долей сульфата железа(II) 5%?
ќтвет: 45,73 г; 454,27 мл.
3. —мешали раствор массой 120 г с w( ќЌ) = 9% с раствором массой 380 г с w( ќЌ) = 12%. ¬ычислите массовую долю гидроксида кали€ в полученном растворе.
ќтвет: 11,28%.
¬ариант є 8
|
|
|
1. –ассчитайте массу железного купороса FeSO4∙7H2O, которую необходимо растворить в воде объемом 1 л (ρ = 1 г/мл), чтобы получить раствор с массовой долей FeSO4 20%?
ќтвет: 576,37г.
2. акую массу иодида кальци€ следует добавить к раствору объемом 500 мл с w(CaI2) = 12% (ρ = 1,107 г/мл) дл€ получени€ раствора с w(CaI2) = 30%?
ќтвет: 142,33 г.
3. акую массу соли следует растворить в 100 г воды дл€ получени€ раствора c массовой долей этой соли 15%?
ќтвет: 17,65 г.
¬ариант є 9
1. раствору массой 250 г с w(соли) = 10% добавили эту же соль массой 15 г. –ассчитайте массовую долю соли в полученном растворе.††
ќтвет: 15,09 %.
2. акой объем раствора серной кислоты с w(H2SO4) = 90% (r = 1,82 г/мл) нужно вз€ть дл€ приготовлени€ раствора объемом 50 мл с w(H2SO4) = 50% (r = 1,40 г/мл)?†††
ќтвет: 21,37 мл.
3. –ассчитайте массу железного купороса FeSO4∙7H2O, которую необходимо растворить в воде объемом 1 л (ρ = 1 г/мл), чтобы получить раствор с массовой долей FeSO4 20%?
ќтвет: 576,37 г.
¬ариант є 10
1. —мешали раствор массой 300 г с массовой долей растворенного вещества 2% с раствором массой 140 г с массовой долей растворенного вещества 6%. ¬ычислите массовую долю этого вещества в полученном растворе. ќтвет: 3,27%.
2. раствору массой 300 г с w(ZnSO4) = 5% добавили сульфат цинка массой 20 г. –ассчитайте массовую долю ZnSO4 в полученном растворе.†††
ќтвет: 10,94%.
3. ¬ растворе массой 500 г с w(CuSO4) = 4% растворили 25 г медного купороса (CuSO4∙5H2O). –ассчитайте массовую долю сульфата меди(II) в полученном растворе.
ќтвет: 6,86%.
ќбразец выполнени€ письменных заданий:
1. акой объем раствора с w(HNO3) = 86% (r = 1,48 г/мл) нужно вз€ть дл€ приготовлени€ раствора объемом 100 мл с w(HNO3) = 32% (r = 1,20 г/мл)?
–ешение:
1) –ассчитаем массу раствора с массовой долей HNO3 32%:

2) Ќайдем массу HNO3 в 32%-ном растворе:
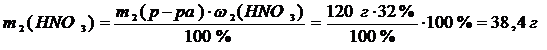
3) –ассчитаем массу раствора с массовой долей HNO3 86%:


4) Ќайдем объем раствора с массовой долей HNO3 86%:

ќтвет: 30,17 мл.
“ема 5.
Ёлектролитическа€ диссоциаци€. —лабые и сильные электролиты. ¬одородный показатель.
¬опросы дл€ самосто€тельной внеаудиторной подготовки к зан€тию:
1. „то называетс€ электролитической диссоциацией? Ёлектролиты и неэлектролиты. ѕриведите примеры. каким классам неорганических соединений относ€тс€ электролиты? Ќазовите основные положени€ теории электролитической диссоциации —. јррениуса.
2. ак вли€ет природа химической св€зи на диссоциацию веществ в растворах? ѕо€сните механизм процесса электролитической диссоциации, приведите примеры и схемы диссоциации в воде электролитов с ионным типом св€зи и ковалентной пол€рной св€зью. „то такое сольваты (гидраты)?
3. „то такое степень диссоциации? акие электролиты называютс€ сильными и слабыми? ѕриведите примеры.
4. «ависимость степени диссоциации от:
- от природы электролита и растворител€; роль диэлектрической проницаемости растворител€ в процессе диссоциации;
- концентрации электролита и изменени€ концентрации одно- именных ионов;
- температуры; термодинамический анализ процесса диссоциации.
5. онстанта электролитической диссоциации. ќт каких факторов она зависит? «акон разбавлени€ ќствальда дл€ слабых бинарных электролитов.
6. ƒайте определени€ кислоте, основанию и соли (средней, кислой, основной, двойной) согласно теории электролитической диссоциации.
7. »онное произведение воды. ¬одородный показатель Ц (рЌ); гидроксидный показатель Ц рќЌ. —умма рЌ и рќЌ. «начени€ концентрации —(Ќ+) и рЌ в различных средах.
»зучив эти вопросы, выполните письменно следующие задани€:
¬ариант є 1
|
|
|
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO4, Ca(OH)2, Al2(SO4)3, H3PO4, NaHSO3, MgOHCl, Kјl(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) Fе—l3 + NаќЌ Ѓ
2) Nа2—ќ3 + Ќ—l Ѓ
3) јgNќ3 + Nа3PO4 Ѓ
3. –ассчитайте рЌ раствора угольной кислоты с концентрацией 0,003 моль/л.
4. Ќайдите активную концентрацию ионов магни€ в растворе сульфата магни€ с концентрацией 0,05 моль/л.
¬ариант є 2
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HCl, Fe(OH)2, ZnSO4, H2Sќ3, (FeOH)2SO4, Ca(HSO4)2, (NH4)2Fe(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) AlCl3 + NаќЌ Ѓ
2) NаCl + AgNO3 Ѓ
3) HBr + Na2—ќ3 Ѓ
3. –ассчитайте рЌ раствора угольной кислоты с концентрацией 0,007 моль/л.
4. Ќайдите активную концентрацию ионов магни€ в растворе нитрата магни€ с концентрацией 0,05 моль/л.
¬ариант є 3
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO, OH, Nа2SO4, H2—ќ3, FeOHSO4, Mg(HSO4)2, Fe(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) †FeSO4 + NаќЌ Ѓ
2) †¬а(NO3)2 + 2SO4 Ѓ
3) †Ќ—l + 2—ќ3 Ѓ
3. –ассчитайте рЌ раствора уксусной кислоты с концентрацией 0,002 моль/л.
4. Ќайдите активную концентрацию ионов магни€ в растворе хлорида магни€ с концентрацией 0,07 моль/л.
¬ариант є 4
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO3, Ba(OH)2, CuSO4, H2S, AlOHSO4, Ca(H2PO4)2, NH4Fe(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) ¬аCl2 + Nа2SO4 Ѓ
2) —а—l2 + 2—ќ3 Ѓ
3) Sr(ќЌ)2 + ЌNќ3 Ѓ
3. –ассчитайте рЌ раствора сернистой кислоты с концентрацией 0,008 моль/л.
4. Ќайдите активную концентрацию ионов натри€ в растворе сульфата натри€ с концентрацией 0,05 моль/л.
¬ариант є 5
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HNO3, NaOH, Fe2(SO4)3, H3AsO4, NaHCO3, CaOHCl, NH4Fe(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) Ќ3PO4 + ќЌ Ѓ
2) Nа2Siќ3 + Ќ—l Ѓ
3) јgNќ3 + K—l Ѓ
3. –ассчитайте рЌ раствора синильной кислоты с концентрацией 0,002 моль/л.
4. Ќайдите активную концентрацию хлорид ионов в растворе хлорида магни€ с концентрацией 0,045 моль/л.
¬ариант є 6
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO3, Sr(OH)2, Na2SO4, H2S, (CaOH)2SO4, Mg(HSO4)2, (NH4)2Fe(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) †FeCl2 + NаќЌ Ѓ
2) †K3PO4 + AgNO3 Ѓ
3) †H—l + 2Siќ3 Ѓ
3. ”кажите кислотноЦосновные сопр€жЄнные пары в уравнени€х протолитических реакций:
¬ариант є 7
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO2, Ba(OH)2, Nа2SiO3, H2Sќ3, AlOHSO4, Ca(HSO4)2, Al(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) †CuSO4 + NаќЌ Ѓ
2) †¬а—l2 + 2SO4 Ѓ
3) †Ќ2SO4 + 2—ќ3 Ѓ
3. –ассчитайте рЌ раствора уксусной кислоты с концентрацией 0,006 моль/л.
4. Ќайдите активную концентрацию нитрат ионов в растворе нитрата алюмини€ с концентрацией 0,08 моль/л.
¬ариант є 8
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO, Ca(OH)2, ZnSO4, H2SiO3, CrOHSO4, Mg(H2PO4)2, NH4Fe(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) †FeCl3 + NаќЌ Ѓ
2) †—а(NO3)2 + 2—ќ3 Ѓ
3) †Ba(ќЌ)2 + ЌNќ3 Ѓ
3. –ассчитайте рЌ раствора метановой кислоты с концентрацией 0,002 моль/л.
4. Ќайдите активную концентрацию ионов алюмини€ в растворе сульфата алюмини€ с концентрацией 0,04 моль/л.
|
|
|
¬ариант є 9
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO4, Ca(OH)2, Al2(SO4)3, H3PO4, NaHSO3, MgOHCl, Kјl(SO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) †FeSO4 + NаќЌ Ѓ
2) †¬а(NO3)2 + 2SO4 Ѓ
3) †Ќ—l + 2—ќ3 Ѓ
3. –ассчитайте рЌ раствора сернистой кислоты с концентрацией 0,002 моль/л.
4. Ќайдите активную концентрацию нитрат ионов в растворе нитрата бари€ с концентрацией 0,07 моль/л.
¬ариант є 1 0
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HClO2, Ba(OH)2, Nа2SiO3, H2Sќ3, AlOHSO4, Ca(HSO4)2, Al(SO4)2. †Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
2. —оставьте молекул€рные, полные и сокращенные ионно-молекул€рные уравнени€ дл€ следующих реакций:
1) †Ќ3PO4 + ќЌ Ѓ
2) †Nа2Siќ3 + Ќ—l Ѓ
3) †јgNќ3 + K—l Ѓ
3. –ассчитайте рЌ раствора синильной кислоты с концентрацией 0,007 моль/л.
4. Ќайдите активную концентрацию ионов хрома в растворе сульфата хрома с концентрацией 0,04 моль/л.
ќбразец выполнени€ письменных заданий:
1. акие электролиты диссоциируют необратимо, а какие - обратимо? ѕокажите это на примерах следующих электролитов: HNO3, HNO2, LiOH, Mg(HSO4)2. Ќазовите все образующиес€ ионы по номенклатуре »ёѕј .
ќтвет: ††††††††† HNO3 Ѓ H+ + NO 
††††††††††††††††††††††††††††††††††††††††† ††††††††††††ион водорода нитрат-ион
††††††††††††††††† HNO2 ↔ †H+ + NO 
†††††††††††††††††††††††††††††††††††††††††† †††††††††††ион водорода ††††††нитрит-ион
LiOH Ѓ Li+ + OH─
†††††††††††††††††††††††††††††††††††††††† ††††††††††††††ион лити€ †††гидроксид-ион
Mg(HSO4)2 Ѓ Mg2+ + 2HSO 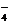
†††††††††††††††††††† ††††††ион магни€ гидросульфат-ион
2. —оставьте молекул€рное, полное и сокращенное ионно-молекул€рные уравнени€ дл€ следующей реакции:
†††††††† Fe(OH)2 + H2SO4Ѓ
ќтвет: Fe(OH)2 + H2SO4 Ѓ FeSO4 + 2H2O
†††††††††† Fe(OH)2 + 2H+ + SO †Ѓ Fe2+ + 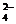
SO + 2H2O
†††††††††† Fe(OH)2 + 2H+ Ѓ Fe2+ + 2H2O
“ема 6.
–авновесные процессы в растворах электролитов.
“еории кислот и оснований. ѕроизведение растворимости.
√идролиз солей. Ѕуферные растворы.
¬опросы дл€ самосто€тельной внеаудиторной подготовки к зан€тию:
1. акие достоинства и недостатки имеет теори€ кислот и оснований —. јррениуса?
2. ƒайте определени€ кислоте и основанию с позиций протолитической теории. „то называетс€ кислотноЦосновной сопр€жЄнной парой?
3. акие достоинства и недостатки имеет протолитическа€ теори€ кислот и оснований?






