2NO(г) + O2 ↔ 2NO2?
ќтвет по€сните, вычислив DG0 и р пр€мой реакции.
–ешение:
2NO(г) + O2 ↔ 2NO2
ƒл€ ответа на вопрос следует вычислить DG0298 или 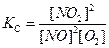 пр€мой реакции. ѕоследнее выражение и есть «ƒћ. «на€, что значени€ DG0f дл€ простых веществ, наход€щихс€ в устойчивых при стандартных услови€х агрегатных состо€ни€х, равны нулю, а значени€ DG0ƒ (в кƒж/моль): дл€ NO (86,6); NO2 (51,5).
пр€мой реакции. ѕоследнее выражение и есть «ƒћ. «на€, что значени€ DG0f дл€ простых веществ, наход€щихс€ в устойчивых при стандартных услови€х агрегатных состо€ни€х, равны нулю, а значени€ DG0ƒ (в кƒж/моль): дл€ NO (86,6); NO2 (51,5).
–ассчитываем DG0х.р.:
DG0х..р. = 2DG0ƒ,(NO2) - 2DG0ƒ, (NO) = 2∙51,5 - 2∙86,6 = -70,2 кƒж = -70,2∙103 ƒж
ѕосле этого вычисл€ем константу равновеси€:
∆GT = -RTlnK.
lnK = 70,2Ј103/(8,314∙298) = 27,9
K = 1,33∙1012
“о, что DG < 0, а Kр >> 1, указывает на возможность самопроизвольного протекани€ пр€мой реакции при T = 298 и равенстве давлений вз€тых газов 1,013×105 ѕа (760 мм рт.ст. или 1 атм.). —амопроизвольно при этих услови€х будет протекать пр€ма€ реакци€, т.к. дл€ нее DG = -70,2∙103 ƒж, а = 1,33∙1012.
ќтвет: -70,2∙103 ƒж, = 1,33∙1012
173. ѕри некоторой температуре равновесие в системе:
2NO2 ↔ 2NO+O2 установилось при следующих концентраци€х (в моль/л): [NO2] = 0,006, [NO] = 0,024, [O2] = 0,012. Ќайдите константу равновеси€ реакции и исходную концентрацию NO2. ак нужно изменить давление и температуру, чтобы сместить равновесие вправо?
–ешение:
2NO2 ↔ 2NO+O2
[NO2]р = 0,006 моль/л
[NO]р = 0,024 моль/л
[O2]р = 0,012 моль/л
р =? [NO2]исх =?
оличество образовавшегос€ NO равно количеству израсходованного NO2 = 0,024 моль, тогда исходна€ концентраци€ NO2равна: 0,006 + 0.024 = 0,03 моль/л.
[NO2]исх = [NO2] + 2[O2] = 0,006 + 2∙0,012 = 0,03 моль/л
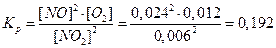
Ќаправление смещени€ равновеси€ определ€етс€ принципом Ће Ўателье: если на систему, наход€щуюс€ в равновесии, оказывать внешнее воздействие, то равновесие смещаетс€ в том направлении, которое ослабл€ет эффект внешнего воздействи€:
а) ƒанна€ реакци€ эндотермическа€, поэтому повышение температуры смещает равновесие в сторону продуктов реакции, т.е. вправо.
б) ¬ результате реакции происходит увеличение числа молей газообразных веществ, поэтому понижение давлени€ смещает химическое равновесие в сторону увеличени€ числа частиц, т.е. вправо, а увеличение давлени€ Ц влево.
ќтвет: 0,03 моль/л, 0,192
189. ƒл€ реакции в растворе 2Fe3+ + Sn2+ = 2Fe2+ + Sn4+ получены следующие данные:
| [Fe3+], моль/л-1 | 0,2 | 0,6 | 0,8 | 0,6 | 0,6 |
| [Sn2+] моль/л-1 | 0,2 | 0,2 | 0,2 | 0,4 | 0,6 |
| V, моль л-1 ×с-1 |
ћожет ли быть эта реакци€ простой? ¬ыведите кинетическое уравнение скорости; найдите константу скорости, пор€дки реакции в целом и по компонентам.
–ешение:
»з приведенных данных видно, что увеличение [Fe3+]0 в 2 раза при неизменной концентрации [Sn2+]0 приводит к увеличению скорости в 4 раза, следовательно, пор€док по железу равен 2. ”величение обеих концентраций в 2 раза приводит к увеличению скорости в 8 раз. “ак как пор€док по железу равен 2, такое изменение скорости соответствует первому пор€дку по олову. “огда общий пор€док равен 3. инетическое уравнение реакции:
|
|
|
υ = k[Fe3+]2Ј[Sn2+]
ќтвет: ѕор€док по Fe3+ Ц 2, Ц по Sn2+ Ц 1, общий Ц 3
198. –азложение озона 2O3 = 3O2 характеризуетс€ энергией активации 100 кƒж/моль. „ему равна константа скорости этой реакции при 1000C, если при 00 C она равна 2∙10-2? ¬ычислите температурный коэффициент этой реакции.
–ешение:
Ea = 100 кƒж/моль
t1 = 1000C
t2 = 0 0C
k2 = 2∙10-2
«аписываем уравнение јррениуса в общем виде дл€ двух констант скоростей:
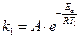 ;
; 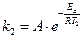
ƒл€ того чтобы избавитьс€ от неизвестной величины предэкспоненциального множител€ (ј), делим большую константу скорости (k2) на меньшую (k1):
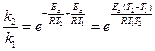 ;
;
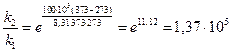
k1 = 1,5∙10-7
213. ¬о сколько раз надо увеличить концентрацию водорода, чтобы скорость реакции H2(газ) + I2(газ) = 2HI(газ) возросла в три раза?
–ешение:
H2(газ) + I2(газ) = 2HI(газ)
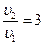
—корость пр€мой реакции равна:
υ1 = k∙[H2]∙[I2]
«ависимость скорости реакции от концентраций определ€етс€ законом действи€ масс: при посто€нной температуре скорость химической реакции пр€мо пропорциональна произведению мол€рных концентраций реагирующих веществ, вз€тых в степен€х, равных коэффициентам в уравнении реакций.
ќбозначим концентрацию реагирующих веществ:
[H2] = a, [I2] = b. —огласно закону действи€ масс скорость
(ν) реакции до изменени€ объема будет равна:
υ = ka∙b.
ѕосле увеличени€ концентрации водорода в х раз: [H2] = aх, [I2]= b.
ѕри этих концентраци€х скорость (ν) реакции примет значение:
υ` = k(aх) (b) = хkab;
ќткуда: 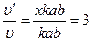 ; ќткуда х = 3.
; ќткуда х = 3.
ќтвет: 3
228. акие объемы 36 %-ного раствора Ќ—l (r = 1,18 г/мл) и воды необходимо вз€ть дл€ приготовлени€ 500 г 0,5 мол€льного раствора?
–ешение:
ћ(Ќ—l) = 36,5 г/моль.
ћол€льна€ концентраци€ Ц (мол€льность) определ€етс€ отношением количества вещества, содержащегос€ в растворе, к массе растворител€.
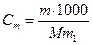 = (моль/кг),
= (моль/кг),
где m Ц масса вещества, содержащегос€ в растворе;
ћ Ц его мол€рна€ масса;
m1 Ц масса растворител€. ќтсюда: 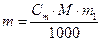 ;
;
ћасса кислоты равна: 0,5∙36,5∙500/1000 = 9,125 г.
Ќаходим объем 36 % раствора кислоты:
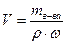 ; V(H3PO4) = 9,125/1,18∙0,36 = 21,48 мл.
; V(H3PO4) = 9,125/1,18∙0,36 = 21,48 мл.
ќбъем воды равен: 500 Ц 21,48∙1,18 = 500 Ц 25,35 = 474,65 г (=474,65 мл, т.к. плотность воды равна 1 г/мл).
(проверка: количество кислоты равно: 9,125/36,5 = 0,25 моль;
Cm (HNO3) = 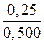 = 0,5 моль/кг Ќ2ќ.
= 0,5 моль/кг Ќ2ќ.
ќтвет: 474,65 мл
243. ƒл€ нейтрализации 20 мл 0,1 н. раствора кислоты потребовалось 8 мл раствора NaOH. —колько граммов NaOH содержит 1 л этого раствора?
–ешение:
—огласно закону эквивалентов при нейтрализации в точке эквивалентности действует равенство:
—Ќ1∙V1= —Ќ2∙V2
0,1∙20 = —Ќ2∙8
—Ќ2 = 0,25 н
ќпределим, сколько граммов NaOH содержит 1 л этого раствора:
m = Cн∙V∙Mr= 0,25∙1∙40 = 10 г
ќтвет: 10 г
258. „ему равно при температуре -7,5 0C осмотическое давление раствора, в 1,5 л которого содержитс€ 276 г глицерина —3Ќ8ќ3?
–ешение:
—огласно закону ¬ант-√оффа:
Pосм =—ћЈRЈT
Ќайдем, сколько г глицерина содержитс€ в 1 л раствора:
в 1,5 л раствора содержитс€ 276 г глицерина
|
|
|
1 л - x г,
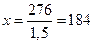 г/л, что составит
г/л, что составит 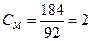 моль/литр = 2Ј103 моль/м3;
моль/литр = 2Ј103 моль/м3; 
(92 г /моль - мол€рна€ масса глицерина)
ќтсюда:
Pосм = 2Ј103 моль/м3Ј8,31 ѕаЈм3/моль Ј Ј265,5 = 4413Ј103 ѕа = 4413 кѕа.
ќтвет: 4413 кѕа
283. Ќапишите в молекул€рной и ионно-молекул€рной формах уравнени€ реакций:
а) бромид алюмини€ + нитрат серебра
б) сульфид натри€ + серна€ кислота
–ешение:
а) AlBr3 + 3AgNO3 → 3AgBr↓ + Al(NO3)3
Al3+ + 3Br- + 3Ag+ + NO3- → 3AgBr↓ + Al3+ + 3NO3-
Br- + Ag+ → AgBr↓
б) Na2S + H2SO4 → Na2SO4 + H2S↑
2Na+ + S2- + 2H+ + SO42- → 2Na+ + SO42- + H2S
S2- + 2H+ - → H2S ↑
298. —оставьте молекул€рные уравнени€ реакций, которым соответствуют ионно-молекул€рные уравнени€:
а) Pb2+ + CrO42- Ѓ PbCrO4¯
б) HCO3- + OH- Ѓ CO32- + H2O
–ешение:
а) Pb2+ + CrO42- Ѓ PbCrO4¯
Pb(NO3)2 + K2CrO4 Ѓ PbCrO4 + 2KNO3
Pb2+ + 2NO3Ц + 2K+ + CrO42Ц → PbCrO4 + 2K+ + 2NO3Ц
б) HCO3- + OH- Ѓ CO32- + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
Na+ + HCO3- + Na+ + OH- → 2Na+ + CO32- + H2O
313. —ущественно ли изменитс€ реакци€ среды, если растворить в воде такие соли, как: a) KCN, б) NH4CN, в) CH3COOK, г) CH3COONH4?
–ешение:
KCN Ц цианид кали€
KOH HCN
сильное слаба€
основание кислота
√идролизу подвергаетс€ слабый ион:
—окращенное ионное уравнение гидролиза:
CN- + H+OH‑ ↔ HCN + OH-
ѕолное ионное уравнение гидролиза:
K+ + CN- + H2O ↔ HCN + K+ + OH-
ћолекул€рное уравнение гидролиза:
KCN + H2O ↔ HCN + KOH
—оль, образованна€ сильным основанием и слабой кислотой подвергаетс€ гидролизу по аниону при этом среда щелочна€, т.е рЌ > 7,0
NH4CN цианид аммони€
NH4OH HCN
cлабые электролиты
NH4+ + H+OH- ↔ NH4OH + H+
CN- + H+OH- ↔ HCN + OH-
NH4+ + CN- + H2O ↔ NH4OH + HCN
NH4CN + H2O ↔ NH4OH + HCN
диссоциации NH4OH = 1,8 ∙ 10-5 (1,76 ∙10-5)
диссоциации HCN = 7,9 ∙10-10 (6,2 ∙ 10-10)
дисс NH4OH > Kдисс HCN, то реакци€ раствора среды слабощелочна€.
CH3COOK ацетат кали€
слаба€ сильное
кислота основание
CH3COOH KOH
CH3COO- + H+OH- ↔ CH3COOH + OH- щелочна€ среда
CH3COO- + K+ + H2O ↔ CH3COOH + K+ + OH-
CH3COOK + H2O ↔ CH3COOH + KOH
CH3COONH4 ацетат аммони€
CH3COOH NH4OH
слабые электролиты
CH3COO- + H+OH- ↔ CH3COOH + OH-
NH4+ + H+OH- ↔ NH4OH + H+
CH3COO- + NH4+ + H≠2O ↔ CH3COOH + NH4OH
–еакци€ среды нейтральна€, т.к. диссоциации (NH4OH) = 1,8 ∙ 10-5 и диссоциации (—Ќ3—ќќЌ) = 1,8 ∙ 10-5
“.е. константа диссоциации кислоты равна константе диссоциации основани€.






