ѕри электролизе
’арактер процессов, происход€щих при электролизе, зависит от многих факторов, важнейшими из которых €вл€ютс€ природа электролита, материал анода, концентраци€ раствора электролита и режим электролиза (температура, напр€жение, плотность тока и др.).
”читыва€ вли€ние природы электролита на характер процессов электролиза, рассмотрим два принципиально различных варианта: электролиз расплава и электролиз раствора электролита.
9.2.1. Ёлектролиз расплава электролита
ѕри прохождении тока через расплав соли на катоде восстанавливаютс€ катионы металла, на аноде окисл€ютс€ анионы кислотного остатка соли.
Ёлектролизом расплавов солей и гидроксидов получают металлы, имеющие сильно отрицательные значени€ ≈ о  (Na, Al,Mg, Ca, Ni, Be и др.).
(Na, Al,Mg, Ca, Ni, Be и др.).
Ќапример, при электролизе расплавов NaCl и NaќЌ протекают следующие процессы:
2NaCl расплав
↑↓
(−) K (Pt)  2Na+ + 2Cl
2Na+ + 2Cl 
 (Pt) ј (+);
(Pt) ј (+);
(−) K: 2Na+ + 2 
 2Na (+) A: 2Cl
2Na (+) A: 2Cl 
 Cl2 + 2
Cl2 + 2  ;
;

2Na++2Cl  ↔ 2Na+Cl2.
↔ 2Na+Cl2.
4NaќЌрасплав
↑↓
(−) K (Pt)  4Na+ + 4ќЌ
4Na+ + 4ќЌ 
 (Pt) ј (+);
(Pt) ј (+);
(−) K: 4Na+ + 4 
 4Na (+) A: 4OH- ↔ 2Ќ2ќ + O2
4Na (+) A: 4OH- ↔ 2Ќ2ќ + O2  + 4
+ 4  ;
;
 |
4Na+ + 4ќЌ  ↔ 4Na + 2Ќ2ќ + ќ2.
↔ 4Na + 2Ќ2ќ + ќ2.
≈сли расплав состоит из нескольких солей, очередность разр€дки катионов и анионов определ€етс€ значени€ми их стандартных электродных потенциалов (см. прил., табл. 13). „ем больше величина стандартного электродного потенциала металла, тем выше окислительна€ способность ионов этого металла, тем легче разр€жаютс€ катионы. Ќапример, при одновременном присутствии в расплаве катионов Zn2+, Pb2+, Cu2+ в равных концентраци€х на катоде в соответствии со значени€ми их стандартных электродных потенциалов (≈ оZn2+/Zn =−0,76 B; ≈ оPb2+/Pb =−0,13 B; ≈ оCu2+/Cu = +0,34 B) сначала выделитс€ медь, затем Ц свинец и в конце процесса Ц цинк.
ќкисление на аноде протекает тем легче, чем ниже значение стандартного электродного потенциала аниона. Ќапример, при одновременном присутствии в расплаве анионов Cl-, J-, SO 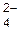 в равных концентраци€х (стандартные электродные потенциалы которых соответственно равны +1,36 ¬; +0,53 ¬; +2,05 ¬) первоначально будут окисл€тьс€ анионы J-, затем Ц Cl- и наконец Ц SO
в равных концентраци€х (стандартные электродные потенциалы которых соответственно равны +1,36 ¬; +0,53 ¬; +2,05 ¬) первоначально будут окисл€тьс€ анионы J-, затем Ц Cl- и наконец Ц SO 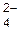 .
.
9.2.2. Ёлектролиз раствора электролита
ѕри электролизе водных растворов электролитов в процессе принимают участие не только молекулы электролитов, но и молекулы растворител€ Ц воды.
ѕротекание того или иного электрохимического процесса у электродов при электролизе прежде всего будет зависеть от относительных значений электродных потенциалов соответствующих электрохимических систем. »з нескольких возможных процессов преимуществом обладает тот, осуществление которого сопр€жено с минимальной затратой энергии. Ёто означает, что на катоде будут восстанавливатьс€ окисленные формы электрохимических систем с наибольшим значением электродного потенциала, а на аноде будут окисл€тьс€ восстановленные формы систем с наименьшим значением электродного потенциала.
|
|
|
атодные процессы. ѕри электролизе водного раствора электролита на катоде протекают два взаимно конкурирующих процесса:
1. ¬осстановление катионов металла:
ћеn+ + n  ↔ продукты.
↔ продукты.
2. Ёлектрохимическое разложение воды в соответствии с уравнением
2H2O + 2  ↔ H2
↔ H2  + 2OH
+ 2OH  (рЌ
(рЌ 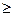 7), ≈
7), ≈ 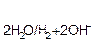 =−0,059рЌ.
=−0,059рЌ.
Ёлектрохимическое выделение водорода происходит из кислотных растворов (рЌ<7) вследствие разр€да ионов водорода в соответствии с уравнением
2Ќ+ + 2  ↔ H2
↔ H2  , ≈
, ≈  =−0,059рЌ.
=−0,059рЌ.
¬опрос о том, какой из катодных процессов обладает преимуществом, определ€етс€ величинами стандартных электродных потенциалов окисленных форм электрохимических систем, концентрацией раствора электролита, услови€ми электролиза (плотность тока, температура).
¬се окислители, которые восстанавливаютс€ на катоде при электролизе, по величине их стандартных потенциалов подраздел€ютс€ на три группы:
I группа Ц окислители, стандартный потенциал которых более положителен, чем потенциал стандартного водородного электрода (Cu2+, Ag+, Hg2+, Au3+, O2, J2, Br2, Cl2, PbO2, MnO4- и др.). ќни восстанавливаютс€на катоде в первую очередь в пор€дке уменьшени€ электродного потенциала. ¬осстановление ионов водорода или молекул воды не происходит.
II группа Ц окислители от (от Li+ до Al3+ включительно), стандартный потенциал которых более отрицателен, чем потенциал стандартного водородного электрода, не могут быть восстановлены электролизом из растворов солей, на катоде в этом случае восстанавливаетс€ водород в кислотной среде, а в водных растворах в первую очередь восстанавливаютс€ молекулы воды.
III группа Ц окислители, имеющие стандартный электродный потенциал меньший, чем у водорода, но больший чем у алюмини€ (Mn2+, Zn2+, Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, Pb2+). ¬ зависимости от условий проведени€ электролиза (рЌ раствора, плотности тока, перенапр€жени€ и др.) возможно преимущественное восстановление молекул воды (в кислотных растворах ионов водорода) или этих окислителей, в противном случае протекает их одновременное восстановление на катоде.
III группа Ц окислители, имеющие стандартный электродный потенциал меньший, чем у водорода, но больший чем у алюмини€ (Mn2+, Zn2+, Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, Pb2+). ¬ зависимости от условий проведени€ электролиза (рЌ раствора, плотности тока, перенапр€жени€ и др.) возможно преимущественное восстановление молекул воды (в кислотных растворах ионов водорода) или этих окислителей, в противном случае протекает их одновременное восстановление на катоде.
| атодные процессы | ||
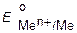 < < 
|  < <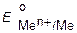 < < 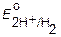
| 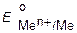 > > 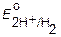
|
| Li+, K+, Na+, Mg2+, Al3+ и др. | Mn2+, Zn2+, Cr 3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, Pb2+ | Cu2+, Ag+ ЕAu3+, O2, J2, Br2, MnO4- |
2Ќ2ќ +2 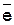 ↔H2↑+2OЌ-
(рЌ ↔H2↑+2OЌ-
(рЌ 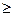 7);
2H+ + 2 7);
2H+ + 2 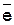 ↔ H2↑
(рЌ < 7) ↔ H2↑
(рЌ < 7)
|
ће ↔ Men+ + n 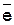 2Ќ2ќ +2
2Ќ2ќ +2 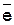 ↔H2↑+2OЌ-
(рЌ ↔H2↑+2OЌ-
(рЌ 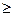 7);
2H++2 7);
2H++2 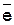 ↔ H2↑(рЌ < 7) ↔ H2↑(рЌ < 7)
|
ће ↔ Men+ + n 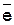 Ox + n
Ox + n 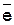 ↔ Red ↔ Red
|
≈сли водный раствор содержит катионы различных металлов в равных концентраци€х, то при электролизе выделение их на катоде будет протекать в пор€дке уменьшени€ величины стандартного электродного потенциала соответствующего металла. “ак, из смеси катионов Ag+, Cu2+, Fe2+ сначала будут восстанавливатьс€ катионы Ag+(≈O  =+0,80 B), затем Cu2+(≈O
=+0,80 B), затем Cu2+(≈O  = +0,34 B) и Fe2+ (≈O
= +0,34 B) и Fe2+ (≈O  =−0,44 B).
=−0,44 B).
|
|
|
јнодные процессы при электролизе растворов в значительной мере завис€т от материала анода. ѕри этом возможны два принципиально различных случа€: первый Ц анод выполнен из инертных материалов (уголь, графит, платина) Ц электролиз с нерастворимым анодом и второй Ц анод выполнен из материала, окисл€ющегос€ в ходе электролиза, Ц электролиз с растворимым анодом.
| јнодные процессы | |
| Ќерастворимый (инертный) анод | –астворимый анод |
| 1. ќкисление бескислородных анионов J-, Br-, Cl- | 1. –астворение анода
ће ↔ Men+ + n 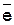
|
2. Ёлектрохимическое окисление воды в зависимости от характера среды
4ќЌ- ↔ 2 Ќ2ќ + ќ2↑ + 4 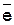 (рЌ (рЌ 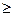 7)
2 Ќ2ќ ↔ ќ2 ↑+ 4Ќ+ + 4 7)
2 Ќ2ќ ↔ ќ2 ↑+ 4Ќ+ + 4 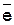 (рЌ < 7) (рЌ < 7)
| 2. Ёлектрохимическое окисление воды
в зависимости от характера среды
4ќЌ- ↔ 2 Ќ2ќ + ќ2↑ + 4 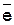 (рЌ (рЌ 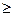 7)
2 Ќ2ќ ↔ ќ2 ↑+ 4Ќ+ + 4 7)
2 Ќ2ќ ↔ ќ2 ↑+ 4Ќ+ + 4 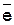 (рЌ < 7) (рЌ < 7)
|
| 3. ќкисление бескислородных анионов в пор€дке возрастани€ ≈о - J-, Br-, Cl- | |
4. ќкисление анионов SO 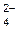 , NO , NO  , —O , —O 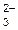
|
Ёлектролиз с нерастворимым анодом. ѕри электролизе водных растворов электролитов с нерастворимым анодом характер
анодного процесса определ€етс€ исход€ из значений стандартных электродных потенциалов анионов солей и электрохимического окислени€ воды с выделением кислорода.
Ёлектрохимическое окисление воды зависит от характера среды и протекает в соответствии с уравнени€ми:
2H2O ↔ O2 + 4H+ + 4  , (рЌ
, (рЌ 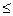 7); ≈
7); ≈  =1,23−0,59рЌ ¬.
=1,23−0,59рЌ ¬.
4ќЌ  ↔ O2 + 2H2O + 4
↔ O2 + 2H2O + 4  , (рЌ > 7); ≈
, (рЌ > 7); ≈  =1,23−0,59рЌ ¬.
=1,23−0,59рЌ ¬.
»з сопоставлени€ величин электродных потенциалов соответствующих электрохимических систем становитс€ очевидным
процесс электрохимического разложени€ воды.
–ассмотрим некоторые примеры электролиза водных растворов с нерастворимым анодом.
ѕример 1.
2NaCl + 2Ќ2ќ
↑↓
(−) K (Pt)  2Na+ + 2Cl
2Na+ + 2Cl 
 (Pt) ј (+);
(Pt) ј (+);
(−) : 2Ќ2ќ + 2  ↔ Ќ2
↔ Ќ2  +2ќЌ- (+) ј: 2Cl
+2ќЌ- (+) ј: 2Cl  ↔Cl2 +2
↔Cl2 +2  ;
;

2NaCl + 2Ќ2ќ ↔ Ќ2  + Cl2 + 2NaќЌ.
+ Cl2 + 2NaќЌ.
ѕример 2.
2SO4 + Ќ2ќ
↑↓
(−) K (Pt)  2K+ + SO42
2K+ + SO42 
 (Pt) ј (+);
(Pt) ј (+);
(−) : 2Ќ2ќ +2  ↔ Ќ2
↔ Ќ2  + 2ќЌ- (+) ј: 2Ќ2ќ ↔ O2
+ 2ќЌ- (+) ј: 2Ќ2ќ ↔ O2  + 4H++ 4
+ 4H++ 4  ;
;

2Ќ2ќ ↔ 2Ќ2  + O2
+ O2  .
.
ѕример 3.
4 OH + Ќ2ќ
↑↓
(−)K (Pt)  4K+ + 4OH
4K+ + 4OH 
 (Pt) ј (+);
(Pt) ј (+);
(−) : 4Ќ2ќ + 4  ↔ Ќ2
↔ Ќ2  +4ќЌ- (+) ј: 4OH- ↔2Ќ2ќ + O2
+4ќЌ- (+) ј: 4OH- ↔2Ќ2ќ + O2  + 4
+ 4  ;
;

2Ќ2ќ ↔ 2Ќ2  + O2
+ O2  .
.
јналогично происходит электролиз водных растворов NaOH, Na2SO4, NaNO3 и кислородосодержащих кислот. ѕри электролизе разлагаетс€ вода:
2Ќ2ќ ↔ 2Ќ2  + O2
+ O2  .
.
ѕример 4.
Ќ2SO4 + Ќ2ќ
↑↓
(−) K (Pt)  2Ќ+ + SO
2Ќ+ + SO 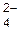
 (Pt) ј (+);
(Pt) ј (+);
(−) : 4Ќ+ + 4  ↔ 2Ќ2
↔ 2Ќ2  (+) ј: 2Ќ2ќ ↔ O2
(+) ј: 2Ќ2ќ ↔ O2  + 4H++ 4
+ 4H++ 4  ;
;

2Ќ2ќ ↔ 2Ќ2  + O2
+ O2  .
.
ѕример 5.
ZnSO4 + Ќ2ќ
↑↓
(−) K (Pt)  Zn2+ + SO
Zn2+ + SO 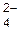
 (Pt) ј (+);
(Pt) ј (+);
(−) : Zn2+ + 2  ↔ Zn (+) ј: 2Ќ2ќ ↔O2
↔ Zn (+) ј: 2Ќ2ќ ↔O2  +4H++ 4
+4H++ 4  ;
;
2Ќ2ќ + 2  ↔ Ќ2
↔ Ќ2  + 2ќЌ-
+ 2ќЌ-

ZnSO4 + 2Ќ2ќ ↔ Zn + 2Ќ2  + O2
+ O2  + H2SO4.
+ H2SO4.
ѕример 6.
CuSO4 + Ќ2ќ
↑↓
(−) K (Pt)  Cu2+ + SO
Cu2+ + SO 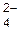
 (Pt) ј (+);
(Pt) ј (+);
(−) : Cu2+ + 2  ↔Cu (+) ј: 2Ќ2ќ ↔O2
↔Cu (+) ј: 2Ќ2ќ ↔O2  + 4H++ 4
+ 4H++ 4  ;
;

2CuSO4 + 2Ќ2ќ ↔ 2Cu + O2  + 2H2SO4.
+ 2H2SO4.
ѕример 7.
HCl + Ќ2ќ
↑↓
(−) K (Pt)  H+ + Cl
H+ + Cl 
 (Pt) ј (+);
(Pt) ј (+);
(−) : 2Ќ++ 2  ↔ Ќ2
↔ Ќ2  (+) ј: 2Cl
(+) ј: 2Cl  ↔ Cl2 +2
↔ Cl2 +2  ;
;

2HCl ↔ Ќ2  + Cl2.
+ Cl2.
ѕри высоких плотност€х тока на катоде идет выделение Cl2, при малых Ц ќ2↑.
Ёлектролиз с растворимым анодом. ¬ этом случае источником электронов, поступающих с анода во внешнюю цепь, может быть металл, из которого выполнен анод.
ѕереход электронов с анода во внешнюю цепь смещает вправо равновесие, существующее между металлом Ц электродом и раствором:
ћео электрод 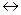 ћеn+ раствор + n
ћеn+ раствор + n  внешн€€ цепь,
внешн€€ цепь,
благодар€ чему анод раствор€етс€.
“аким образом, число конкурирующих окислительных процессов возрастает до трех:
1) электрохимическое окисление воды с выделением кислорода;
|
|
|
2) окисление аниона электролита;
3) электрохимическое окисление металла − материала анода (анодное растворение металла).
»з этих возможных процессов будет осуществл€тьс€ энергетически наиболее выгодный.
Ќапример, в случае электролиза раствора хлорида меди, осуществл€емого с медным анодом, возможны следующие процессы:
2—l 
 Cl
Cl  + 2
+ 2  ; ≈о =+1,36 ¬,
; ≈о =+1,36 ¬,
2H2O  O2 + 4H+ + 4
O2 + 4H+ + 4  ; ≈о =+1,23 ¬,
; ≈о =+1,23 ¬,
—uо  —u2+ + 2
—u2+ + 2  ; ≈о =+0,34 ¬.
; ≈о =+0,34 ¬.
»з сопоставлени€ величин электродных потенциалов соответствующих электрохимических систем можно сделать вывод о преимущественном протекании процесса окислени€ меди из общего числа рассматриваемых. “аким образом, при электролизе раствора хлорида меди, проводимом с медным анодом, происходит растворение меди на аноде и выделение ее на катоде:
CuCl2 + Ќ2ќ
↑↓
(−) K (Cu)  Cu2+ + 2 Cl
Cu2+ + 2 Cl 
 (Cu) A (+);
(Cu) A (+);
(−) : Cu2+ + 2  ↔ Cu (+) ј: Cu ↔ Cu2+ + 2
↔ Cu (+) ј: Cu ↔ Cu2+ + 2  .
.






