| є п\п | онтролируемые темы (в соответствии с √ќ— ¬ѕќ) | оличество тестовых заданий |
| 1. | ќсновные пон€ти€, концепции и законы химии. | |
| 2. | —троение атома. ѕериодичность изменени€ свойств атомов и свойств их соединений. | |
| 3. | ’имическа€ св€зь | |
| 4. | лассы неорганических соединений | |
| 5. | ’имическа€ термодинамика. Ёнергетика химических процессов. | |
| 6. | ’имическое и фазовое равновесие. инетика химических реакций. | |
| 7. | –астворы.–астворимость. онцентраци€ растворов. | |
| 8. | оллигативные свойства растворов. ќсмотическое давление. «акон –аул€. | |
| 9. | –астворы электролитов. | |
| 10. | »онное произведение воды. √идролиз солей. | |
| 11. | ќкислительно-восстановительные реакции. | |
| 12. | √етерогенные ќ¬–. ’имические свойства металлов. Ёлектрохими€. | |
| 13. | ’ими€ минералов. | |
| ¬сего: |
Ќаправление Ц130101.65 Ђѕрикладна€ геологи€ї
—пециализаци€: √еологическа€ съемка, поиски и разведка месторождений полезных ископаемых. є 1-300
ћетодика проведени€ контрольного зан€ти€
по проверке итоговых базовых знаний по всей дисциплине
(в рамках аттестационных меропри€тий):
| оличество оценок | |
| Ќазвани€ оценок | удовлетворительно, хорошо, отлично |
| ѕороги оценок (количество правильных ответов) | 32 Ц 40 Ђотличної; 22 - 32 Ђхорошої; 12 - 22 Ђудовлетворительної |
| ѕредел длительности всего контрол€ | 2 часа |
| ѕредел длительности ответа на каждый вопрос | 3 мин |
| ѕоследовательность выбора тем | последовательна€ |
| ѕоследовательность выборки вопросов из каждой темы | случайна€ |
| ѕредлагаемое количество вопросов из каждой темы: | 2-3 |
| ¬сего вопросов: | |
| –ежим формировани€ журнала | по средней оценке |
¬ыбор одного из многих:
1.1. ”кажите параметры "нормальные услови€" дл€ газов:
P=105 ѕа, T=273 K;
P=105 ѕа, T=298 K;
P=1 ѕа, T=273 K;
P=10 ѕа, T=273 K.
1.2. ¬ каких единицах измер€етс€ количество вещества в химии:
в килограммах;
в литрах;
в мол€х;
в граммах.
1.3. ’имический эквивалент веществ Ц это:
количество вещества, реагирующее с 1 моль газообразного Ќ2;
количество вещества, реагирующее с 1г ќ2;
количество вещества, реагирующее с 1г Ќ2 ;
количество вещества, реагирующее с 1моль Ќ+.
1.4. „ему равна масса 2 молей H2SO4 (ћ=98 г/моль):
196 г; 98 г; 49 г; 980 г.
1.5. акое количество вещества (в мол€х) содержитс€ в 80 граммах
гидроксида натри€ NaOH (ћ=40 г/моль):
1 моль; 40 моль; 22,4 моль; 2 мол€.
1.6. —колько молей вещества содержитс€ в 11,2 литрах любого газа
при нормальных услови€х:
1 моль; 0,5 моль; 22,4 моль; 2 моль.
1.7. акой объем занимает 1 моль любого газа при "нормальных услови€х":
V=22,4 л; V=1 л; V=1 м3; V=22,4 м.3
1.8. акое количество частиц (атомов или молекул) содержит 1 моль
любого вещества:
|
|
|
100; 1023; 1*1023; 6,02*1023.
1.10. акой объем при нормальных услови€х занимает 2,2г —ќ2:
22,4л; 11,2л; 2,24л; 1,12л.
1.11.»з перечисленных уравнений укажите уравнение ћенделеева- лапейрона:
- PR = (m/M)VT;
- PT = (m/M)RV;
- PV = (m/M)RT
- PV = (mM)RT.
1.12. акое уравнение св€зывает основные параметры идеального газа:
- уравнение ћенделеева- лапейрона;
- уравнение √есса;
- уравнение ¬ант-√оффа;
- уравнение јррениуса.
1.13.—месь 2г Ќ2 и 16г ќ2 при н.у. занимает объем:
22,4л; 11,2л; 33,6л; 44,8л.
1.14. ѕорци€ ортофосфата кальци€, содержаща€ 1,8 ∙ 1024 катионов, отвечает количеству вещества:
0,5моль; 1моль; 3моль; 0,3моль.
1.15.—колько молекул содержитс€ в 1 мл водорода при нормальных услови€х:
2,61∙1019; 2,65 ∙ 1020; 2,69 ∙ 1019;2,65 ∙ 1022.
1.16. ћол€рна€ масса эквивалента H2SO4 равна:
98г/моль; 49г/моль; 18г/моль;22,4г/моль.
1.17. Ёквивалентный объем кислорода равен:
11,2л; 5,6л; 22,4л; 18,6л.
1.18. —колько молекул содержитс€ в 1 л азота при нормальных услови€х:
2,61∙1019; 2,68 ∙ 1020; 2,68 ∙ 1019; 2,68 ∙ 1022.
1.19. ѕорци€ дигидрофосфата, натри€, содержаща€ 1,8∙1024 катионов, отвечает количеству вещества
0,3моль; 0,5моль; 1моль; 3моль.
1.20 Ёквивалентный объем водорода равен:
11,2л;5,6л; 22,4л; 18,6л.
2.1. Ёлектронна€ формула атома кислорода:
-1s22s2 2p5;
- 1s22s2 2p3;
- 1s22s2 2p4;
- 1s22s2 2p6.
2.2. Ёлектронна€ формула атома азота
- 1s22s2 2p5;
- 1s22s2 2p3;
- 1s22s2 2p1;
- 1s22s2 2p6.
2.3.јтом какого элемента второго периода имеет в невозбужденном состо€нии максимальное число неспаренных электронов:
B; O; N; F.
2.4.јтом какого элемента третьего периода имеет в невозбужденном состо€нии максимальное число неспаренных электронов:
Al; Si; P; S.
2.5.” какого из атомов наибольшее значение потенциала ионизации:
F; Na; Mg2+ ; Cl.
2.6. ” какого из атомов наименьшее значение потенциала ионизации:
F; Na; Mg2+ ; Cl.
2.7. јтом с самым высоким значением электроотрицательности:
F; Br; J ; Cl.
2.8. акой ион имеет наибольший радиус:
F-; Na+; Mg2+; Cl-.
2.9. акую степень окислени€ в соединени€х не про€вл€ет хром:
+2; +1; +6; +3.
2.10.¬ какой степени окислени€ соединени€ хрома про€вл€ют основные свойства:
+3; +4; +6; +2.
2.11. аковы валентность и степень окислени€ азота в HNO3:
- 4 и +5; - 5 и +5; - 4 и +3; - 5 и +3.
2.12.— повышением степени окислени€ центрального атома кислотные свойства гидроксидов:
усиливаютс€;
ослабевают;
не измен€ютс€;
зависит от природы атома.
2.13. — понижением степени окислени€ центрального атома кислотные свойства гидроксидов:
усиливаютс€;
ослабевают;
не измен€ютс€;
зависит от природы атома.
2.14. — повышением степени окислени€ центрального атома основные свойства гидроксидов:
усиливаютс€;
ослабевают;
не измен€ютс€;
зависит от природы атома.
2.15. — понижением степени окислени€ центрального атома основные свойства гидроксидов:
усиливаютс€;
ослабевают;
не измен€ютс€;
зависит от природы атома.
2.16. ƒл€ элемента с электронной формулой 3s1 характерны свойства:
металлические;
неметаллические;
- кислотные;
амфотерные.
2.17. ƒл€ элемента с электронной формулой 3s23р5 характерны свойства:
|
|
|
металлические;
неметаллические;
кислотные;
амфотерные.
2.18. √идроксид элемента с электронной формулой 3s1 обладает свойствами:
металлическими;
неметаллическими;
кислотными;
основными.
2.19. √идроксид элемента с электронной формулой 3s23р5обладает свойствами
металлическими;
неметаллическими;
кислотными;
основными.
2.20.√идроксид элемента с электронной формулой 3s23р3обладает свойствами
амфотерными;
неметаллическими;
кислотными;
основными.
3.1. ѕри образовании химической св€зи внутренн€€ энерги€ системы:
увеличиваетс€;
уменьшаетс€;
не измен€етс€;
может и увеличиватьс€ и уменьшатьс€.
3.2. “олько σ-св€зи в молекуле:
H2CO3; HCl; H2SO4; HCN.
3.3. π Ц св€зей нет в молекуле:
H2CO3; HCl; H2SO4; HCN.
3.4. σ - св€зи могут быть образованы:
только р-р орбитал€ми;
любыми орбитал€ми;
только s-s орбитал€ми;
р-, d- и f-орбитал€ми.
3.5. π - св€зи могут быть образованы:
только р-р орбитал€ми;
любыми орбитал€ми;
только s-s орбитал€ми;
р-, d- и f-орбитал€ми.
3.6 —ама€ высока€ степень ионности св€зи между элементами:
Si - S; C Ц N; Cs Ц F; Al Ц Cl.
3.7. —оединение, в котором ковалентные св€зи пол€рны:
O2; H2; H2O; Cl2.
3.8. —оединение, в котором ковалентные св€зи непол€рны:
SO2; HCl; H2O; Cl2.
3.9. —в€зь между атомом натри€ и кислотным остатком в молекуле Na2SO4:
ионна€;
ковалентна€ пол€рна€;
ковалентна€ непол€рна€;
донорно-акцепторна€.
3.10. —в€зь между молекулой аммиака и молекулой воды в молекуле NH4OH:
ионна€;
ковалентна€ пол€рна€;
ковалентна€ непол€рна€;
донорно-акцепторна€.
3.11. —в€зь между атомом водорода и кислотным остатком в молекуле Ќ2SO4:
ионна€;
ковалентна€ пол€рна€;
ковалентна€ непол€рна€;
донорно-акцепторна€.
3.12. —в€зь между атомом серы и кислородом в молекуле Na2SO4:
ионна€;
ковалентна€ пол€рна€;
ковалентна€ непол€рна€;
донорно-акцепторна€.
3.13. ѕрочность св€зи в р€ду HF ЦHCl Ц HBr - HI:
уменьшаетс€;
увеличиваетс€;
не измен€етс€;
зависит от давлени€.
3.14. ¬одородные св€зи образуютс€ между молекулами:
HF; HCl; HBr; HI.
3.15. ¬одородные св€зи образуютс€ между молекулами:
H2S; HCl; H2O; H2Te.
3.16. ѕол€ризуемость какого иона выше:
F-; Cl-; Br-; I-.
3.17. ѕол€ризуемость какого иона выше:
Li+; Na+; K+; Rb+.
3.18. —амым сильным пол€ризующим действием обладает ион:
Ca2+; Na+; Mg2+; Al3+.
3.19.ќпределение, неприменимое к металлической св€зи:
пол€рна€;
делокализованна€;
ненасыщенна€;
ненаправленна€.
3.20.ќпределение, применимое к металлической св€зи:
пол€рна€;
делокализованна€;
насыщенна€;
направленна€.
4.1. акое из приведенных оснований не может образовать основную соль:
CsOH; Cu(OH)2; Ca(OH)2; Al(OH)3.
4.2. ака€ из приведенных кислот не может образовать кислую соль:
HCl; H3PO4; H2SO4; H2CO3.
4.3. —ильное основание:
Mg(OH)2; KOH; NH4OH; Cu(OH)2.
4.4. ѕри равных концентрации в растворе сама€ сильна€ кислота:
HCl; HClO;HClO4; HClO2.
4.5. —лабое растворимое основание:
Mg(OH)2; KOH; NH4OH;Cu(OH)2.
4.6. ака€ из приведенных кислот не может образовать кислую соль:
H2S; H2SO4; HSCN; H2SO3.
4.7. ака€ из приведенных кислот может образовать кислую соль:
HNO3; HCl; HClO4;H2SO4.
4.8. акое из приведенных оснований не может образовать основную соль:
CsOH; Cu(OH)2; Ca(OH)2; Al(OH)3.
4.9. акое из приведенных оснований может образовать основную соль:
CsOH; Cu(OH)2;NaOH; NH4OH.
4.10. ѕравильное название соли Ca(HCO3)2:
дигидрокарбонат кальци€;
гидрокарбонат кальци€;
карбонат кальци€;
гидроксокарбонат кальци€.
4.11. ѕравильное название соли Fe(ќЌ)2Cl:
дигидроксохлорид железа;
гидроксохлорид железа;
хлорид железа;
- гидрохлорид железа.
4.12. —оль Ca(HCO3)2:
|
|
|
средн€€; кисла€; основна€; комплексна€.
4.13. —оль Fe(ќЌ)2Cl:
средн€€; кисла€; основна€; комплексна€.
4.14. јмфотерными свойствами обладает:
Mg(OH)2; Al(OH)3;NH4OH; Cu(OH)2.
¬ 4.15.јмфотерными свойствами обладает:
Mg(OH)2; Zn(OH)2;Fe(OH)2;Cu(OH)2.
4.16. —оль, про€вл€юща€ кислотные свойства:
¬a(NO)2;Ca(HCO3)2; Na2SO4; NaCl.
4.17. —оль, про€вл€юща€ основные свойства:
¬aCO3; Ca(HCO3)2; Na2SO4; Fe(ќЌ)2Cl.
4.18. ќксид кальци€ не взаимодействует с:
гидроксидом натри€;
сол€ной кислотой;
оксидом углерода (IY);
оксидом цинка.
4.19. ќксид углерода (IY) не взаимодействует с:
гидроксидом натри€;
сол€ной кислотой;
оксидом кальци€;
оксидом цинка.
4.20. ќксид углерода (II) не взаимодействует с:
гидроксидом натри€;
сол€ной кислотой;
оксидом кальци€;
химически инертен.
4.21. ќксид серы (YI) не взаимодействует с:
гидроксидом натри€;
сол€ной кислотой;
оксидом кальци€;
оксидом цинка.
5.1.”кажите параметры "стандартные услови€", используемые в термодинамике:
P=105 ѕа, T=273 K;
P=105 ѕа, T=298 K;
P=1 ѕа, T=273 K;
P=10 ѕа, T=273 K.
5.2. ‘изический смысл энтальпии:
особый вид энергии;
энергосодержание системы;
внутренн€€ энерги€ системы;
энерги€ взаимодействи€ составных частей системы.
5.3. ‘изический смысл энтропии:
мера неупор€доченности (хаоса) системы;
энерги€ взаимодействи€ составных частей системы;
энергосодержание системы;
внутренн€€ энерги€ системы.
5.4. Ёнтропи€ в самопроизвольно протекающих процессах:
остаетс€ неизменной;
уменьшаетс€;
увеличиваетс€;
проходит через максимум.
5.5. Ёндотермической называетс€:
реакци€, протекающа€ с выделением тепла;
реакци€, протекающа€ с поглощением тепла;
реакци€, протекающа€ с увеличением давлени€;
реакци€, протекающа€ с увеличением объема.
5.6.Ёкзотермической называетс€:
реакци€, протекающа€ с поглощением тепла;
реакци€, протекающа€ с выделением тепла;
реакци€, протекающа€ с увеличением давлени€;
реакци€, протекающа€ с увеличением объема.
5.7.“еплотой образовани€ называют:
количество теплоты, которое необходимо затратить на протекание химической реакции;
количество теплоты, которое выдел€етс€ при протекании химической реакции;
количество теплоты, которое выдел€етс€ при сгорании 1 кг вещества;
количество теплоты, которое затрачиваетс€ на разложение 1 мол€ сложного вещества на простые вещества.
5.8.ѕри расчете теплового эффекта химической реакции примен€ют:
закон ћенделеева- лапейрона;
закон Ѕойл€-ћариота;
закон √есса;
закон јррениуса.
5.9. ≈сли изменение энергии √иббса ΔG в химической реакции меньше нул€, то:
самопроизвольно может протекать и пр€ма€ и обратна€ реакции;
самопроизвольно может протекать обратна€ реакци€;
самопроизвольно может протекать пр€ма€ реакци€;
в системе наблюдаетс€ состо€ние равновеси€.
5.10. ≈сли изменение энергии √иббса ΔG в химической реакции больше нул€, то:
самопроизвольно может протекать пр€ма€ реакци€;
самопроизвольно может протекать обратна€ реакци€;
самопроизвольно может протекать и пр€ма€ и обратна€ реакци€;
в системе наблюдаетс€ состо€ние равновеси€.
5.11. ≈сли изменение энергии √иббса ΔG в химической реакции равно нулю, то:
самопроизвольно может протекать пр€ма€ реакци€;
самопроизвольно может протекать обратна€ реакци€;
самопроизвольно может протекать и пр€ма€ и обратна€ реакци€;
система находитс€ в состо€нии равновеси€.
5.12.»зменение энтропии в реакции NH4NO3(к) = N2O(г) + 2H2O(г):
больше нул€;
меньше нул€;
равно нулю;
|
|
|
зависит от пути процесса.
5.13. »зменение энтропии в реакции 2H2O(г) = O2(г) + 2H2(г):
больше нул€;
меньше нул€;
равно нулю;
- зависит от пути процесса.
5.14. »зменение энтропии в реакции O2(г) + 2H2(г) = 2Ќ2ќ(г)
больше нул€;
меньше нул€;
равно нулю;
зависит от пути процесса.
5.15 ƒл€ реакции ј¬(к) + ¬2(г) = ј¬3(к), протекающей при 298о в пр€мом направлении, знаки ∆H, ∆S и ∆G:
∆H<0, ∆S<0, ∆G<0;
∆H>0, ∆S<0, ∆G>0;
∆H>0, ∆S>0, ∆G>0
∆H<0, ∆S>0, ∆G<0
5.16 ƒл€ процесса превращени€ графита в алмаз при 298о знаки ∆H, ∆S и ∆G:
∆H<0, ∆S<0, ∆G<0;
∆H>0, ∆S<0, ∆G>0;
∆H>0, ∆S>0, ∆G>0;
∆H<0, ∆S>0, ∆G<0.
5.17.¬озможно самопроизвольное протекание реакции при любой температуре,если:
∆H<0, ∆S<0, ∆G<0;
∆H>0, ∆S<0, ∆G>0;
∆H>0, ∆S>0, ∆G>0;
∆H<0, ∆S>0, ∆G<0.
5.18.Ќевозможно самопроизвольное протекание реакции при любой температуре, если:
∆H<0, ∆S<0, ∆G<0;
∆H>0, ∆S<0, ∆G>0;
∆H>0, ∆S>0, ∆G>0;
∆H<0, ∆S>0, ∆G<0.
5.19. ѕри соединении 2,1г железа с серой выделилось 3,77 кƒж. “еплота образовани€ сульфида железа равна:
∆Hо= -100,5кƒж/моль;
∆Hо= +100,5кƒж/моль;
∆Hо= 0 кƒж/моль;
∆H о = -184,5кƒж/моль.
5.20. ѕри полном сгорании 6г угл€ выделитс€ тепла (∆Hо  = -393,5кƒж/моль):
= -393,5кƒж/моль):
393,5кƒж; 196,8кƒж; 204,8кƒж; 39,4 кƒж.
6.1. —корость химической реакции определ€етс€ по формуле:
(C - концентраци€, t - врем€) Е
V = ΔC/Δt; V = C/Δt; V = ΔC/t; V = C/t.
6.2. ”кажите фактор, не вли€ющий на скорость химической реакции:
концентраци€ реагирующих веществ;
наличие катализатора;
массы реагирующих веществ;
температура системы.
6.3. ”кажите фактор, не вли€ющий на скорость химической реакции в растворе:
концентрации реагирующих веществ;
объем системы;
природа реагирующих веществ;
температура системы.
6.4. ”кажите фактор, не вли€ющий на скорость химической реакции:
концентрации реагирующих веществ;
наличие катализатора;
природа реагирующих веществ;
объемы реагирующих растворов.
6.5. ”кажите фактор, вли€ющий на скорость химической реакции:
массы реагирующих веществ;
объемы реагирующих веществ;
концентрации продуктов реакции;
температура системы;
6.6. Ёнерги€ активации процесса Ц это:
энерги€, котора€ выдел€етс€ при химической реакции;
энерги€, которую необходимо затратить, чтобы началась химическа€ реакци€;
энерги€, котора€ поглощаетс€ системой в ходе химической реакции;
энерги€, которую затрачивает атом дл€ преодолени€ энергетического барьера.
6.7. ак зависит скорость химической реакции от энергии активации
процесса?
чем больше энерги€ активации, тем выше скорость химической реакции;
чем больше энерги€ активации, тем меньше скорость химической реакции;
чем меньше энерги€ активации, тем труднее протекает химическа€ реакци€;
чем меньше энерги€ активации, тем меньше скорость химической реакции.
6.8. ”кажите фактор, вли€ющий на скорость химической реакции:
энерги€ активации процесса;
объемы реагирующих веществ;
концентрации продуктов реакции;
массы исходных веществ.
6.9.ѕравильное выражение закона действующих масс дл€ химической реакции A+2BЃC:
V=k[A][B]2; V=k[A]+[B]; V=[A][B]; V=k[A][B][C].
6.10.ѕравильное выражение закона действующих масс дл€ химической реакции 2A+BЃ2C:
V=k[A][B];V=k[A]2[B]; V=[A]2[B]; V=k[A]2[B][C]2.
6.11. ак изменитс€ скорость химической реакции, если температура в системе увеличитс€ на 20о—, а температурный коэффициент равен g = 2,0?
увеличитс€ в 20 раз;
увеличитс€ в 2 раза;
увеличитс€ в 4 разa;
увеличитс€ в 40 раз.
6.12.Kак изменитс€ скорость химической реакции, если температура в системе увеличитс€ на 50о—, а температурный коэффициент равен g = 2,0?
увеличитс€ в 2 раза;
увеличитс€ в 100 раз;
увеличитс€ в 50 раз;
увеличитс€ в 32 раза.
6.13. ћеханизм катализа:
катализатор пропускает реакцию через р€д промежуточных стадий с низкими значени€ми энергии активации;
катализатор повышает энергию активации;
катализатор снижает внутреннюю энергию системы;
|
|
|
катализатор смещает химическое равновесие в сторону образовани€ продуктов реакции.
6.14.«начение константы равновеси€ химической реакции
A+2BЂC+D при равновесных концентраци€х веществ в системе
[A] =[B] = [C] = [D] = 10 моль/л, равно:
1; 100;10; 0,1.
6.15. ѕовышение давлени€ в системе
2SO2 + O2 ↔ 2SO3
сместит химическое равновесие:
влево;
вправо;
не сместит;
возможно и влево и вправо.
6.16. ’имическое равновесие-это такое состо€ние системы:
когда скорости пр€мой и обратной реакций равны нулю;
когда скорость пр€мой реакции больше скорости обратной;
когда скорость пр€мой реакции меньше скорости обратной;
когда скорость пр€мой и обратной реакций равны.
6.17.”кажите фактор, не вли€ющий на смещение химического равновеси€:
наличие в системе катализатора;
повышение температуры системы;
уменьшение концентрации исходных веществ;
увеличение концентрации продуктов реакции.
6.18. онстанта равновеси€ реакции C+O2 = CO2 выражаетс€ уравнением:
р=  ; р=
; р=  ; р=
; р=  ; р=
; р=  .
.
6.19. онстанта равновеси€ реакции S+O2 = SO2 выражаетс€ уравнением:
р= 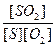 ; р =
; р = 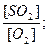 ; р=
; р= 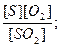 ; р =
; р =  .
.
6.20. ’имическое равновесие реакции 2Fe + O2= 2FeO смещаетс€ при:
добавлении железа;
добавлении оксида железа;
повышении давлени€;
уменьшении концентрации железа.
7.1. ака€ из перечисленных смесей не образует раствор:
вода + ацетон;
вода + кристаллы соли;
вода + бензол;
вода + газообразный аммиак.
7.2. ака€ из перечисленных ниже смесей образует раствор
лед + масло;
вода + бензол;
вода + кристаллы сахара;
вода + кристаллы нафталина.
7.3. –астворимость большинства солей возрастает с:
увеличением давлени€;
понижением температуры системы;
повышением температуры;
понижением давлени€.
7.4. ‘актор, который уменьшает растворимость большинства солей:
увеличение температуры системы;
понижение температуры системы;
повышение давлени€;
понижение давлени€.
7.5. –астворимость газов в воде увеличиваетс€ при:
повышении давлени€ и понижении температуры;
повышении давлени€ и повышении температуры;
понижении давлени€ и понижении температуры;
понижении давлени€ и повышение температуры.
7.6. »зменение давлени€ не вли€ет на растворимость:
хлористого водорода;
хлорида натри€;
сероводорода;
оксида углерода (IY).
7.7. »зменение давлени€ вли€ет на растворимость:
хлористого водорода;
хлорида натри€;
сульфата натри€;
серной кислоты.
7.8. оэффициент растворимости показывает:
массу вещества, образующую насыщенный раствор со 100г растворител€;
количество вещества (моль), образующее насыщенный раствор со 100г растворител€;
массу вещества, образующую 1л насыщенного раствора;
количество вещества (моль), образующую 1л насыщенного раствора;
7.9. –астворимость жидкости в воде не зависит от:
температуры;
природы химических св€зей в молекуле вещества;
давлени€;
строени€ молекулы.
7.10. »стинные растворы образуют вещества с размером частиц:
больше размеров молекулы;
меньше размеров молекулы;
равным размерам молекулы;
независимо от размеров молекулы.
7.11. Ќаиболее устойчивое агрегатное состо€ние у:
коллоидных растворов;
суспензий;
истинных растворов;
эмульсий.
7.12. ќбразование раствора сопровождаетс€:
увеличением энергии √иббса;
увеличением энтропии;
уменьшением энтропии;
увеличением внутренней энергии системы.
7.13. ѕрактически не раствор€етс€ в воде:
CO2; CH4; H2S; SO3.
7.14. ћассова€ дол€ вещества в растворе показывает:
массу вещества в граммах на каждые 1000 граммов раствора;
массу вещества в граммах в 1 литре раствора;
массу вещества в граммах на каждые 100 граммов растворител€;
массу вещества в граммах на каждые 100 граммов раствора.
7.15. ћол€рна€ концентраци€ раствора показывает
количество растворенного вещества (в мол€х) в 1 кг раствора;
массу растворенного вещества в граммах в 1 л раствора;
массу растворенного вещества в граммах в 1 кг раствора;
количество растворенного вещества (в мол€х) в 1 л раствора.
7.16 ћол€рна€ концентраци€ эквивалента раствора показывает
числов молей эквивалента вещества в 1 л раствора;
массу растворенного вещества в граммах в 1 л раствора;
массу растворенного вещества в граммах в 1 кг раствора;
- количество растворенного вещества (в мол€х) в 1 л раствора.
7.17. ћол€льна€ концентраци€ раствора показывает
число молей растворенного вещества в 1 кг растворител€;
массу растворенного вещества в граммах в 1 литре раствора;
массу растворенного вещества в граммах в 1 кг раствора;
количество растворенного вещества (в мол€х) в 1 литре раствора.
7.18.ћол€рна€ концентраци€ эквивалента раствора, содержащего 16г сульфата меди в 500мл, равна:
0,1н; 0,2н; 0,4н; 0,8н.
7.19.ћассова€ дол€ вещества в растворе, полученного при растворении 100граммов вещества в 400 граммах воды, равна:
25%; 20%; 50%; 5%.
7.20. ћол€рна€ концентраци€ 10% раствора Na2CO3 равна:
1моль/л; 2моль/л; 10моль/л; 0,5моль/л.
7.21. ћольна€ дол€ NaOH в 40% водном растворе равна:
0,40; 0,23; 0,75; 0,56.
7.22. ≈диницы измерени€ мол€льной концентрации
моль/л;моль/кг; моль/мл; моль/м3.
7.23. “итр 0, 2ћ раствора серной кислоты равен:
0,0196г/мл; 0,0196г/л; 0,0196кг/л; 0,0196кг/мл.
7.24. ћол€рна€ концентраци€ 2% раствора H2SO4 равна:
0,1моль/л; 0,2моль/л; 1моль/л; 0,5моль/л.
7.25. ћассова€ дол€ вещества в растворе, содержащего 40 грамм вещества в 60 граммах воды
60%; 10%; 40%; 100%.
7.26. ƒл€ приготовлени€ раствора с заданной массовой долей раствора нужно знать:
объем раствора;
массу воды;
массу растворенного вещества;
количество вещества.
7.27. ѕри 60о— массова€ дол€ насыщенного раствора KNO3 52,4%. оэффициент растворимости соли при этой температуре равен:
52,4г; 110г; 101г; 220г.
7.28. ћассова€ дол€ вещества в растворе, полученном смешением 300г 25% и 400г 40% растворов этого вещества равна:
33,6%; 22,4%; 28,2%; 65%.
7.29. »з 400г 20% раствора при охлаждении выделилось 50г растворенного вещества. ћассова€ дол€ вещества в оставшемс€ растворе равна:
8,6%; 12,4%; 10,5%; 18,4%.
7.30.ќбъем 1н раствора, в котором содержитс€ 49г серной кислоты, равен:
0,5л; 2л; 1л; 10л.
8.1. ќсмотическое давление раствора пр€мопропорционально:
массовой доле растворенного вещества;
мол€рной концентрации раствора;
мол€льной концентрации раствора;
не зависит от концентрации.
8.2. ѕри 0о— осмотическое давление раствора, содержащего 1моль глицерина в 1л Ќ2ќ, равно:
1,01∙ 102ѕа;
1,01 ∙ 105кѕа;
760мм.рт.ст.;
- 2,27 кѕа.
8.3. ќсмотические давлени€ (при 273о—) растворов, содержащих в 1л воды 20г глюкозы —6Ќ12ќ6 (–1)или 20г сахарозы —12Ќ22ќ11(–2), соотнос€тс€ между собой как:
–1 = –2; –1 < –2; –1 > –2;
8.4. ќсмотические давлени€ (при273о—) растворов, содержащих в 250 мл воды 5г спирта —2Ќ5ќЌ (–1) или 5г сахарозы —12Ќ22ќ11(–2), соотнос€тс€ между собой как:
–1 = –2; –1 < –2; –1 > –2; –1 ≈ –2.
8.5 100мл 0,5ћ водного раствора сахарозы —12Ќ22ќ11 прибавили 400мл воды. ќсмотическое давление полученного раствора:
не изменилось;
в 5 раз больше, чем исходного;
в 5 раз меньше, чем исходного;
в 2 раза меньше, чем исходного.
8.6.ќтношение масс формалина Ќ—Ќќ и глюкозы —6Ќ12ќ6, которые содержатс€ в равных объемах растворов, обладающих при данной температуре одинаковым осмотическим давлением, равно:
1:1; ћЌ—Ќќ : ћ с6н12о6; ћс6н12о6 : ћЌ—Ќќ; 2: 1.
8.7. ќтносительное понижение упругости паров растворител€ над раствором
пропорционально:
мольной доле растворител€;
массе растворител€;
мольной доле растворенного вещества;
массе растворенного вещества.
8.8. ѕри образовании раствора давление насыщенных паров растворител€:
понижаетс€;
повышаетс€;
не измен€етс€;
может и повышатьс€, и понижатьс€.
8.9. ƒавление насыщенных паров воды при температуре 373о и давлении 101,3кѕа
равно:
1,01∙102ѕа; 1,01∙105кѕа;1,01∙105ѕа; 133,3 ѕа.
8.10.≈сли сравнить температуру кипени€ раствора и температура кипени€
чистого растворител€, то температура кипени€ раствора:
всегда выше температуры кипени€ чистого растворител€;
всегда ниже температуры кипени€ чистого растворител€;
всегда равна температуре кипени€ чистого растворител€;
зависит от природы растворител€.
8.11. ≈сли сравнить температуры замерзани€ раствора и чистого растворител€, то температура замерзани€ раствора:
всегда выше температуры замерзани€ чистого растворител€;
всегда ниже температуры замерзани€ чистого растворител€;
всегда равна температуре замерзани€ чистого растворител€;
зависит от природы растворител€.
8.12. “емпература замерзани€ водного раствора, содержащего 3∙ 1023 молекул
неэлектролита в 250г воды, равна:
273о ;269,28о ; 271,4о ; 298о .
8.13. “емпературы кристаллизации 0,1% растворов формалина Ќ—Ќќ(t1) и глюкозы
—6Ќ12ќ6(t2) соотнос€тс€ как:
t1 > t2; t1 < t2; t1 = t2; t1 ≈ t2.
8.14. “емпературы кипени€ 10% растворов —Ќ3ќЌ(t1) и —2Ќ5ќЌ (t2) соотнос€тс€ между собой как:
t1 > t2; t1 < t2; t1 = t2; t1 ≈ t2.
8.15. ¬ 250г органического растворител€ содержитс€ m г растворенного электролита с молекул€рной массой ћ. риоскопическа€ константа растворител€ равна . акое выражение дл€ ∆tкрист правильно:
K∙ m/M; 4K∙ m/M; K ∙ m/4M; M/K ∙ m?
8.16. ¬ 250г органического растворител€ содержитс€ m г растворенного электролита с молекул€рной массой ћ. Ёбулиоскопическа€ константа растворител€ равна Ё. акое выражение дл€ ∆tкип правильно:
Ё∙ m/M; KЁ∙ m/4M; 4Ё∙ m/M; M/Ё ∙ m?
8.17.¬одный раствор неэлектролита кипит при 373,52о . ћол€льна€ концентраци€ этого раствора равна:
1моль/кгЌ2ќ; 0,1моль/кгЌ2ќ; 0,01моль/кгЌ2ќ; 10моль/кгЌ2ќ.
8.18.¬одный раствор неэлектролита кристаллизуетс€ при 1,86о—. ћол€льна€ концентраци€ этого раствора равна:
0,1моль/кгЌ2ќ; 0,01моль/кгЌ2ќ; 10моль/кгЌ2ќ; 1моль/кгЌ2ќ.
8.19.¬одный раствор неэлектролита кипит при 0,52о—. ћол€льна€ концентраци€ этого раствора равна:
1моль/кгЌ2ќ; 0,1моль/кгЌ2ќ; 0,01моль/кгЌ2ќ; 10моль/кгЌ2ќ.
8.20.¬одный раствор неэлектролита кристаллизуетс€ при -371,14о . ћол€льна€ концентраци€ этого раствора равна:
0,1моль/кгЌ2ќ; 0,01моль/кгЌ2ќ; 10моль/кгЌ2ќ; 1моль/кгЌ2ќ.
9.1. Ёлектролитами называют:
вещества, растворы которых не провод€т электрический ток;
вещества, которые провод€т электрический ток;
вещества, растворы которых провод€т электрический ток;
вещества, которые не провод€т электрический ток.
9.2. √руппа веществ, котора€ содержит только электролиты:
металлы, основани€, соли;
оксиды, кислоты, соли;
соли, основани€, оксиды;
кислоты, основани€, соли.
9.3. √руппа веществ, котора€ содержит только неэлектролиты:
кислоты, основани€, соли;
оксиды, кислоты, соли;
металлы, неметаллы, оксиды;
кислоты, основани€, соли.
9.4. ”кажите сильный электролит:
HClO; KOH; H2SO3; Fe(OH)2.
9.5. ”кажите сильный электролит:
H2S; HClO; H2SO3;NaNO3.
9.6. ”кажите сильный электролит:
NaOH; H2S; Fe(OH)2; Mg—ќ3.
9.7. ”кажите слабый электролит: KCl.
H2S; H2SO4; HNO3;
9.8. ”кажите правильное уравнение электролитической диссоциации H2SO4:
H2SO4 = 2H+ + SO42-;
H2SO4= H2+ + SO42-;
H2SO4= 2H+ + 4SO2-;
H2SO4= 2H+ + SO2 + 2O2-.
9.9. ”кажите правильное уравнение электролитической диссоциации K3PO4:
K3PO4 = 3K+ + PO43-;
K3PO4= K3+ + PO43-;
K3PO4= 3K+ + 4PO3-;
K3PO4= 3K+ + PO2 + 2O2-.
9.10. —колько анионов образуетс€ в результате электролитической диссоциации 5 молекул FeCl3?
10; 3; 15;20.
9.11. ¬ результате электролитической диссоциации 2 молекул Mg(NO3)2 образуетс€ ионов:
2; 3; 6;4.
9.12. ¬ результате электролитической диссоциации 3 молекул FeCl3 образуетс€ ионов:
20; 3; 5;12.
9.13. ¬ результате электролитической диссоциации 2 молекул Al2(SO4)3 образуетс€ ионов:
8; 6;10; -12.
9.14. ¬ результате электролитической диссоциации 5 молекул CaCl2 образуетс€ ионов:
15; 30; 25; 20.
9.15. „ему равна степень электролитической диссоциации a, если в растворе электролита на каждые 20 диссоциированных молекул приходитс€ 80 нелиссоциированных?
0,25; 1,0; 0,2; 0,8.
9.16. „ему равна степень электролитической диссоциации a, если в растворе электролита на каждые 8 лиссоциированных молекулы приходитс€ 12 недиссоциированных?
0,2; 0,25;0,75; 0,4.
9.17. „ему равна степень электролитической диссоциации a, если в растворе электролита на каждые 10 диссоциированных молекул приходитс€ 40 недиссоциированных?
0,25; 1,0; 0,20; 0,80.
9.18. —тепень диссоциации электролита не зависит:
от природы вещества;
от концентрации раствора;
от давлени€;
от температуры.
9.19.¬ыражение константы диссоциации не имеет смысла дл€:
водных растворов слабых электролитов;
водных растворов сильных электролитов;
растворов электролитов в непол€рных растворител€х;
разбавленных растворов неэлектролитов.
9.20.—оотношение степени диссоциации и константы диссоциации св€заны:
законом –аул€;
законом ћенделеева- лапейрона;
законом разбавлени€ ќствальда;
законом √есса.
10.1 ѕравильное уравнение диссоциации молекул воды:
Ќ2ќ → 2Ќ+ + ќ2-;
Ќ2ќ ↔ Ќ- + ќЌ-;
Ќ2ќ → Ќ2 + ќ;
Ќ2ќ → Ќ+ + ќЌ-.
10.2. »онное произведение воды выражаетс€ равенством:
[H+][OH-] = 10-14;
[2H+][OH-] = 10-14;
[H+]2[OH-] = 10-14;
[H+][OH-] = 10-16.
10.3. ƒл€ любого водного раствора справедливо:
рЌ = рќЌ;
рЌ > рќЌ;
рЌ < рќЌ;
рЌ +рќЌ= 14.
10.4. «начение рЌ равно:
[H+];
(-lg[H+]);
[OH-];
(-lg[OH-).
10.5. «начение рOЌ равно:
[H+];
(-lg[H+]);
[OH-];
(-lg[OH-).
10.6. «начение рЌ раствора характеризует:
концентрацию ионов металлов;
концентрацию ионов водорода;
концентрацию растворенных солей
концентрацию ионов кислотных остатков.
10.7. рЌ кислых растворов:
< 7; >7; =7; =14.
10.8. рЌ щелочных растворов:
< 7; >7; =7; =14.
10.9. pЌ в 0.01ћ растворе NaOH равно:
7; 2; 12; 10.
10.10. «начение pЌ в 0,001ћ растворе сол€ной кислоты равно:
-1; -3; -7; -11.
10.11. рЌ нейтральных растворов:
0; (-7); 14; 7.
10.12. онцентраци€ ионов водорода в растворе равна 10-5 моль/л; рЌ раствора равно:
(-5);5; 2; (-2).
10.13. онцентраци€ ионов водорода в растворе равна 10-2 моль/л; рЌ раствора равно:
0; 12; (-2); 2.
10.14. онцентраци€ ионов водорода в растворе равна 10-2 моль/л; рќЌ раствора равно:
0; 12; (-2); 2.
10.15. онцентраци€ ионов ќЌ- в в растворе равна 10-2 моль/л; рЌ раствора равно:
0; 12; (-2); 2.
10.16. онцентраци€ ионов ќЌ- в растворе равна 10-2 моль/л; рќЌ раствора равно:
0; 12; (-2); 2.
10.17. онцентраци€ ионов ќЌ- в растворе равна 10-12 моль/л; рЌ раствора равно:
0; 12; (-2); 2.
10.18.ѕроцесс, который протекает в растворе при гидролизе солей:
повышение температуры системы;
изменение величины рЌ раствора;
уменьшение объема системы;
изменение растворимости соли.
10.19. Ќе подвергаетс€ гидролизу:
соль, образованна€ сильной кислотой и сильным основанием;
соль, образованна€ слабой кислотой и слабым основанием;
соль, образованна€ слабой кислотой и сильным основанием;
соль, образованна€ сильной кислотой и слабым основанием.
10.20. «начение рЌ в растворе соли меньше 7:
соль образована сильной кислотой и сильным основанием;
соль, образована слабой кислотой и слабым основанием;
соль, образована слабой кислотой и сильным основанием;
соль, образована сильной кислотой и слабым основанием.
10.21. «начение рЌ в растворе соли больше 7:
соль образована сильной кислотой и сильным основанием;
соль, образована слабой кислотой и слабым основанием;
соль, образована слабой кислотой и сильным основанием;
соль, образована сильной кислотой и слабым основанием.
10.22. √идролизу не подвергаетс€ соль:
KCl; Cu(NO3)2; NaF; AgNO3.
10.23. √идролизу подвергаетс€ соль:
FeCl2; KCl; NaNO3; Na2SO4.
10.24. √идролизу подвергаетс€ соль:
KNO3; KCl; NaNO3;FeCl3.
10.25. √идролизу подвергаетс€ соль:
KCl;SnCl2; NaNO3; KNO3.
10.26. —реда в растворе в соли KNO2:
щелочна€;
кисла€;
нейтральна€;
солева€.
10.27. —реда в растворе в соли FeCl3
щелочна€;
кисла€;
нейтральна€;
солева€.
10.28. —реда в растворе в соли K2S
щелочна€;
кисла€;
нейтральна€;
солева€.
10.29. —реда в растворе в соли MgCl2
щелочна€;
кисла€;
нейтральна€;
солева€.
10.30. —реда в растворе в соли K2SO4
щелочна€;
кисла€;
нейтральна€;
солева€.
11.1. –езультат окислительно-восстановительной реакции:
образование осадка;
образование слабого электролита;
изменение степеней окислени€ атомов;
образование воды.
11.2. ’имическое равновесие ќ¬– смещено в сторону:
образовани€ более сильного окислител€:
образовани€ более слабых окислител€ и восстановител€;
образовани€ более сильного восстановител€;
образовани€ осадка.
11.3. ќкислителем называют вещество, атомы которого:
принимают электроны от других атомов;
отдают свои электроны;
перераспредел€ют свои электроны;
повышают свою степень окислени€.
11.4. ¬осстановителем называетс€ вещество, атомы которого:
принимают свои электроны;
отдают электроны;
перераспредел€ют свои электроны;
понижают свою степень окислени€.
11.5. ¬ процессе окислени€:
происходит отдача электронов;
происходит присоединение электронов;
происходит понижение степени окислени€ атомов или ионов;
происходит перераспределение электронов в атоме элемента.
11.6. ¬ процессе восстановлени€
происходит отдача электронов;
происходит присоединение электронов;
происходит повышение степени окислени€ атомов или ионов;
происходит перераспределение электронов в атоме элемента
11.7. “ипичные восстановители:
кислоты;
чистые неметаллы;
оксиды металлов;
чистые металлы.
11.8.“ипичные окислители:
чистые неметаллы;
чистые металлы;
основани€;
все соли.
11.9. —тепень окислени€ атома азота в HNO3:
+1; -5; 0; +5.
11.10. —тепень окислени€ атома Cl в KClO4:
+3; -1; +5; +7.
11.11. —тепень окислени€ атома Cr в K2—r2O7:
-6; +5;+6; +2.
11.12. –еакци€ 2Ќ2ќ2 = 2Ќ2ќ + ќ2 относитс€ к реакци€м:
межмолекул€рного окислени€- восстановлени€;
внутримолекул€рного окислени€- восстановлени€;
диспропорционировани€;
реакци€м ионного обмена.
¬ыбор одного из многих:
11.13. –еакци€ Ќ2Sќ3 +2 H2S = 3Ќ2ќ + 3S относитс€ к реакци€м:
межмолекул€рного окислени€- восстановлени€;
внутримолекул€рного окислени€- восстановлени€;
диспропорционировани€;
реакци€м ионного обмена.
¬ыбор одного из многих:
11.14. –еакци€ NЌ4Nќ2 = 2Ќ2ќ + N2 относитс€ к реакци€м:
межмолекул€рного окислени€- восстановлени€;
внутримолекул€рного окислени€- восстановлени€;
диспропорционировани€;
реакци€м ионного обмена.
11.15. ¬ окислительно-восстановительной реакции
K + HClќ3 Ѓ KClќ3 + Cl2 + H2O
восстановителем €вл€етс€ атом элемента:
Cl; K; H; O.
11.16. ¬ уравнении окислительно-восстановительной реакции
FeCl2 + Br2 + KOH Ѓ Fe(ќH)3 + KBr + H2O
окислителем €вл€етс€ атом элемента:
Fe; Br. Cl; K;
11.17. ¬ уравнении окислительно-восстановительной реакции
CrCl3 + Br2 + KOH Ѓ K2CrO4 + KBr + KCl+ H2O
восстановителем €вл€етс€ атом элемента:
Cr; Cl;Br; H.
11.18.¬ щелочной среде MnO4- восстанавливаетс€ до Mnќ42-. „исло эквивалента ћnO4- равно:
2; 5; 3; 1.
11.19.¬ кислой среде MnO4- восстанавливаетс€ до Mn2+. „исло эквивалента ћnO4- равно:
2;5; 3; 1.
11.20.ќкислительно-восстановительна€ реакци€ протекает в пр€мом направлении, если:
≈оокислител€ > ≈овосстановител€;
≈оокислител€ < ≈овосстановител€;
≈оокислител€ = ≈овосстановител€;
не зависимо от значений ≈оокислител€ и восстановител€.
12.1. —тандартный потенциал стандартного водородного электрода равен нулю,если;
–(Ќ2) = 101,3кѕа, рЌ=0;
–(Ќ2) = 202,6кѕа, [H+] = 1моль/л;
–(Ќ2) = 101,3кѕа, рЌ=1;
–(Ќ2) = 101,3кѕа, [Ќ+]=0;
12.2. «ависимость потенциала стандартного водородного электрода от рЌ выражаетс€ формулой:
≈ = 0,059рЌ;
≈ = -0,059рЌ;
≈ = 0,059/2 рЌ;
≈ = -0,059/2 рЌ.
12.3. онцентраци€ ионов металла в стандартной электрохимической системе равна:
1 моль/л;
1 моль-экв/л;
1%;
1моль/кг растворител€.
12.4. „ем больше значение стандартного потенциала, тем:
сильнее выражены восстановительные свойства электрохимической системы;
сильнее выражены окислительные свойства электрохимической системы;
сильнее выражены основные свойства металла;
ниже температура плавлени€ металла.
12.5. „ем меньше значение стандартного потенциала, тем:
сильнее выражены восстановительные свойства электрохимической системы;
сильнее выражены окислительные свойства электрохимической системы;
сильнее выражены основные свойства металла;
ниже температура плавлени€ металла.
12.6. ¬еличина стандартного потенциала металлического электрода не зависит:
энергии кристаллической решетки металла;
энергии ионизации атомов металла;
энергии гидратации ионов металла;
теплопроводности металла.
12.7. –€д напр€жени€ металлов составлен в пор€дке:
возрастани€ стандартных электродных потенциалов;
уменьшени€ стандартных электродных потенциалов:
возрастани€ восстановительной способности металла;
возрастани€ основных свойств гидроксидов металлов.
12.8. ѕотенциал водородного электрода при рЌ=10 равен:
-0,59¬; -0,30¬; 0,30¬; 0,59¬.
12.9. ѕотенциал цинкового электрода при разбавлении соли цинка в 10 раз:
возрастет на 59м¬;
уменьшитс€ на 59м¬;
возрастет на 30м¬;
уменьшитс€ на 30м¬.
12.10. ћеталл, который вытеснит металлическую медь из раствора ее соли;
натрий; железо; серебро; золото.
12.11. ћеталл, который вытеснит Ќ2 из разбавленного раствора H2SO4:
Zn; Cu; Ag; водород не выдел€етс€.
12.12. ћеталл, который вытеснит Ќ2 из разбавленного раствора HNO3:
Zn; Cu; Ag; водород не выдел€етс€.
12.13. ћеталл, который вытеснит Ќ2 из воды:
Zn; Cu; Ag; Mg.
12.14. √руппа, в которой пассивируютс€ концентрированной H2SO4 все металлы:
Fe, Mn, Cr;
Na, Ca, Mg;
Cu, Zn, Sn;
Al; Mg, Pb.
12.15. √руппа, в которой пассивируютс€ концентрированной H2SO4 все металлы:
Fe, Mg, K;
Na, Ca, Mg;
Cu, Zn, Al;
Ni; Sn, Pb.
12.16. √руппа, в которой все металлы обладают амфотерными свойствами:
Fe, Mg, K;
Na, Ca, Mg;
Sn, Zn, Al;
Ni; Li, Pb.
12.17. Ќе окисл€етс€ кислородом воздуха металл:
алюминий; золото; кальций; кобальт.
12.18. √азообразных продуктов из раствора c ω(HNO3) < 5% не выдел€ет:
Zn; Cu; Fe; Mg.
12.19. —умма коэффициентов в реакции Mg+HNO3 = Mg(NO3)2+ NH4NO3 + H2O равна:
5; 28; 19; 10.
12.20. —умма коэффициентов в реакции Zn+HNO3 = Zn(NO3)2+ NO2 + H2O равна:
5; 28; 19; 10.
12.21.√альванический элемент Ц это:
система, в которой химическа€ энерги€ преобразуетс€ в электрическую;
система, в которой электрическа€ энерги€ преобразуетс€ в химическую;
система, в которой химическа€ реакци€ протекает при наложении внешнего напр€жени€;
устройство, содержащее катод и анод и подключенное к источнику электрического тока.
12.22. ¬ гальваническом элементе катодом называетс€:
электрод с более положительным электродным потенциалом;
электрод с более отрицательным электродным потенциалом;
электрод с более активным металлом;
электрод с большей площадью поверхности.
12.23. ¬ гальваническом элементе анодом называетс€:
электрод с более положительным электродным потенциалом;
электрод с более отрицательным электродным потенциалом;
электрод с менее активным металлом;
электрод с большей площадью поверхности.
12.24. «ависимость электродного потенциала от различных факторов выражаетс€:
уравнением ћенделеева- лапейрона;
уравнением Ќернста;
уравнением ¬ант-√оффа;
уравнением √есса.
12.25. ¬ концентрационном гальваническом элементе катодом €вл€етс€ электрод:
с более высокой концентрацией электролита;
тот, у которого концентраци€ электролита ниже;
с более высоким значением рЌ;
с значением рЌ=7.
12.26. ¬ концентрационном гальваническом элементе анодом €вл€етс€ электрод:
с более высокой концентрацией электролита;
тот, у которого концентраци€ электролита ниже;
с более высоким значением рЌ;
с значением рЌ=7.
12.27. ¬еличина электродвижущей силы (Ёƒ—) в свинцово-медном гальваническом элементе (≈оPb= -0,14B, EoCu= +0,34B) при стандартных услови€х равна:
0,14 ¬; -0,48 ¬; 0,48 ¬; -0,20 ¬.
12.28. ¬еличина электродвижущей силы (Ёƒ—) в свинцово-серебр€ном гальваническом элементе (≈оPb= -0,14B, EoAg= +0,80B) при стандартных услови€х равна:
-0,94 ¬; 0,66 ¬;0,94 ¬; -0,66 ¬.
12.29. ¬еличина электродвижущей силы (Ёƒ—) в свинцово-золотом гальваническом элементе (≈оPb= -0,14B, EoAu= +1,50B) при стандартных услови€х равна:
1,64 ¬; 1,36 ¬; -1,36 ¬; 1,50 ¬.
12.30. ѕри работе гальванического элемента разрушаетс€:
катод;
анод;
разрушаютс€ оба электрода;
не разрушаетс€ ни один из электродов
12.31. ѕри электролизе растворов электролитов на катоде могут выдел€тьс€:
неметаллы и газообразный кислород;
металлы и газообразный водород;
только газообразный водород;
только газообразный кислород.
12.32. ѕри электролизе растворов электролитов на аноде могут выдел€тьс€:
неметаллы и газообразный кислород;
металлы и газообразный водород;
только газообразный водород;
только газообразный кислород.
12.33. Ќа катоде может протекать процесс:
окислени€ ионов металла;
восстановлени€ ионов металла;
окислени€ ионов неметалла;
восстановлени€ анионов.
12.34. Ќа аноде может протекать процесс:
окислени€ ионов металла;
восстановлени€ ионов металла;
окислени€ анионов;
восстановлени€ анионов.
12.35. Ќа катоде может протекать процесс:
выделени€ газообразного водорода;
диспропорционировани€ ионов неметалла;
восстановлени€ ионов неметалла;
окислени€ ионов неметалла;
12.36. Ќа аноде может протекать процесс:
выделени€ газообразного кислорода;
восстановлени€ ионов металла;
окислени€ ионов металла;
выделени€ газообразного водорода.
12.37. ѕри электролизе растворов или расплавов электролитов не разрушаетс€:
анод;
катод;
разрушаютс€ оба электрода;
в зависимости от условий разрушаетс€ либо катод, либо анод.
12.38. ѕроцесс электролиза нельз€ провести в:
растворе кислоты HCl;
растворе соли NaNO3;
растворе щелочи KOH;
расплав оксида CuO.
12.39. ѕроцесс электролиза нельз€ провести в:
растворе соли KNO3;
растворе щелочи NaOH;
расплаве соли CuSO4;
расплав чистой серы.
12.40. ѕроцесс электролиза можно провести в системе:
кристаллы соли NaNO3;
кристаллы щелочи KOH;
расплав соли 3–O4;
лед.
13.1 ћассова€ дол€ серы в халькопирите равна:
34,8%; 17,4%; 30,4%; 12,2%.
13.2 ћассова€ дол€ конституционной воды в серпентине равна:
34,8%; 17,5%; 30,4%; 13,0%.
13.3 онституционна€ вода представлена в минералах:
ионами ќЌ-;
входит в состав кристаллогидратов;
располагаетс€ в пустотах некоторых структур;
удерживаетс€ на поверхности дисперсных частиц под вли€нием
их силового пол€.
13.4 ристаллизационна€ в






