’»ћ»я
ћетодические указани€
дл€ самосто€тельной работы студентов
очной и заочной форм обучени€
„асть 2
‘акультеты: »—‘, ЁЁ‘, ‘ѕћ и »“, ‘Ё
ƒл€ всех направлений бакалавриата
¬ологда
”ƒ 620.1
’ими€: ћетодические указани€ дл€ самосто€тельной работы студентов очной и заочной форм обучени€. „асть 2. Ц ¬ологда: ¬о√“”, 2012, - 36 с.
¬тора€ часть методических указаний включает в себ€ контрольные вопросы и задачи по основным модул€м курса общей химии 2 части программы. ¬ каждом модуле предлагаетс€ 25 задач различной степени сложности. ¬ конце методических указаний приведена таблица с вариантами выполнени€ работ дл€ студентов-заочников.
”тверждено редакционно-издательским советом ¬о√“”
—оставители: “ихановска€ √.ј., канд. биол. наук, доцент
¬оропай Ћ.ћ., канд. хим. наук, доцент
ћальцева —.Ѕ., канд. техн. наук, доцент
‘окичева ≈.ј., канд. техн. Ќаук, доцент
≈рехинска€ ќ.ѕ., ассистент
–ецензент: Ћебедева ≈.ј. канд. техн. наук, доцент кафедры ¬и¬
¬ологодского государственного технического университета
ќЅў»≈ ћ≈“ќƒ»„≈— »≈ ” ј«јЌ»я
II часть методических указаний дл€ студентов очной и заочной форм обучени€ включает следующие об€зательные модул€ курса общей химии: окислительно-восстановительные процессы; гальванический элемент; процессы электролиза; коррози€ металлов; комплексные соединени€; хими€ элементов s, р, d-семейства; хими€ органических соединений.
¬ каждом модуле предлагаетс€ 25 задач различной степени сложности, которые рекомендуетс€ прорешать на выбор всем студентам.
ѕоследн€€ задача в контрольной работе дл€ студентов заочников различных специальностей даетс€ по выбору препода≠вател€ в соответствии с профессиональной подготовкой будущих специалистов.
ѕоэтому в методических указани€х представлено несколько задач под одинаковыми номерами (225-250).
¬ конце указаний приведена таблица с вариантами вы≠полнени€ контрольных работ дл€ студентов-заочников.
ќ »—Ћ»“≈Ћ№Ќќ-¬ќ——“јЌќ¬»“≈Ћ№Ќџ≈ ѕ–ќ÷≈——џ
1. «акончить уравнени€ реакций и расставить коэффициенты. ¬ каком направлении протекает реакци€?
Cu2S + HNO3 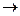 Cu(NO3)2 + H2SO4 + NO2 +...
Cu(NO3)2 + H2SO4 + NO2 +...
2. «акончить уравнени€ реакций и расставить коэффициенты. ¬ каком направлении протекает реакци€?
As2S3 + HNO3 + H2O 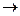 H3AsO4 + H2SO4 + NO.
H3AsO4 + H2SO4 + NO.
3. ћожет ли перманганат кали€ окислить в кислой среде производные —r (III) до Cr (VI)? ѕокажите на примере.
4. ћожет ли концентрированна€ азотна€ кислота окис≠лить свинец до PbO2; олово - до SnO2? ѕриведите при≠меры.
5. ћожно ли использовать PbO2 в качестве окислител€ дл€ осуществлени€ в стандартных услови€х реакций:
а) Mn2+ + 4H2O Ц 5e = MnO 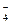 + 8H+;
+ 8H+;
б) 2Cr3+ + 7H2O Ц 6e = Cr2O  + 14H+.
+ 14H+.
6. ¬ каком направлении при стандартных услови€х проте≠кают реакции:
а) P2S3 + HNO3 конц .(+H2O?) 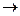 H3PO4 + H2SO4 + NO;
H3PO4 + H2SO4 + NO;
б) P2S5 + HNO3 конц .(+H2O?) 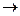 H3PO4 + H2SO4 + NO2.
H3PO4 + H2SO4 + NO2.
7. ¬ каком направлении при стандартных услови€х проте≠кают реакции:
|
|
|
а) NH4HS + HNO3 конц., изб. 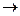 N2 + H2SO4 + NO;
N2 + H2SO4 + NO;
б) FeSO4 + HNO3 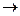 Fe(NO3)3 + NO2 + H2SO4 + H2O.
Fe(NO3)3 + NO2 + H2SO4 + H2O.
8. ¬ каком направлении при стандартных услови€х проте≠кают реакции:
а) FeS2 + HNO3 конц 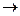 Fe(NO3)3 + NO + H2SO4 + H2O;
Fe(NO3)3 + NO + H2SO4 + H2O;
б) H2S + HNO3 конц., изб. 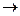 H2SO4 + NO + H2O.
H2SO4 + NO + H2O.
9. Ќапишите уравнени€ реакций взаимодействи€ между:
а) йодидом водорода и азотистой кислотой, при этом азотиста€ кислота восстанавливаетс€ до оксида азота (II);
б) медью и концентрированной азотной кислотой.
10. Ќапишите следующие уравнени€ реакций:
а) сульфида кадми€ с азотной кислотой, при этом об≠разуетс€ элементарна€ сера и оксид азота (II);
б) алюмини€ с дихроматом кали€, в сернокислой сре≠де, при этом дихромат кали€ восстанавливаетс€ до сульфата хрома (III).
11. «акончите уравнени€ реакций окислени€ - восстановле≠ни€ с участием KMnO4, учитыва€ при этом, что  в KMnO4 в кислой среде восстанавливаетс€ до
в KMnO4 в кислой среде восстанавливаетс€ до  , в щелочной - до
, в щелочной - до  .
.
а) H3PO3 + KMnO4 + H2SO4 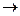 H3PO4 +...
H3PO4 +...
б) Na3AsO3 + KMnO4 + KOH 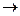 Na3AsO4 +...
Na3AsO4 +...
12. ѕо приведенным ниже электронно-ионным схемам ре≠акций составьте уравнени€ окислительно-восстанови≠тельных реакций (в молекул€рном виде):
а) 10Fe2+ Ц 10eЦ = 10Fe3+;
2MnO 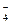 + 10eЦ + 16H+ = 2Mn2+ + 8H2O;
+ 10eЦ + 16H+ = 2Mn2+ + 8H2O;
б) 3Mg0 Ц 6eЦ = 3Mg2+;
SO  + 6eЦ + 8H+ = S0 + 4H2O;
+ 6eЦ + 8H+ = S0 + 4H2O;
13. акой из окислителей - MnO2, PbO2, K2Cr2O7 - €вл€ет≠с€ наиболее эффективным по отношению к Hcl при по≠лучении cl2?
14. ¬ каком направлении будет протекать реакци€?
—rCl3 + Br2 + KOH 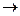 K2CrO4 + KBr + H2O
K2CrO4 + KBr + H2O
15. ћожно ли при стандартных услови€х окислить хлорид водорода до cl2 с помощью серной кислоты? ќтвет под≠твердите расчетом 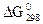 .
.
16. акой объем 2 Ќ Ќbr необходим дл€ взаимодействи€ с 0,25 моль K2Cr2O7:
Ќbr + K2Cr2O7 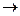 Kbr + CrBr3 + Br2 + H2O
Kbr + CrBr3 + Br2 + H2O
акой объем брома при этом выделитс€?
17. акую массу Al можно окислить с помощью 0,1 л 0,25 Ќ K2Cr2O7 по реакции: Al+K2Cr2O7+H2SO4 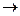 Al2(SO4)3+Cr2(SO4)3+K2SO4+H2O
Al2(SO4)3+Cr2(SO4)3+K2SO4+H2O
18. подкисленному раствору KJ добавлено 0,04 л 0,3 Ќ KNO2:
KJ + KNO2 + H2SO4 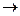 J2 + K2SO4 + NO + H2O
J2 + K2SO4 + NO + H2O
¬ычислите массу выделившегос€ йода и объем NO.
19. —мешаны подкисленные растворы: а) KNO3 и KMnO4; б) Fe2(SO4)3 и K2Cr2O7. ћежду какими из этих ве≠ществ будет протекать реакци€ и чем это определ€≠етс€?
20. ћогут ли одновременно существовать в растворе HJ и HClO3, Hbr и KMnO4?
21. Ѕудет ли азотиста€ кислота: а) окисл€тьс€ действием KMnO4 в нейтральной и кислой средах; б) восстанав≠ливатьс€ до NO сернистой кислотой? ƒл€ возможных случаев напишите уравнени€ реакций.
22. ¬ кислый раствор, содержащий смесь солей Kcl, Kbr и KJ добавлено достаточное количество KNO2. «аписать редокси-цепи, выражающие взаимодействие NO2-иона с каждым по отдельности галогенид-ионом (один из электродов NO  + 2H+/NO + H2O). —опоставлением электродных потенциалов установить, какой из галоге≠нид-ионов будет окисл€тьс€ до свободного состо€ни€ и какие не будут. ƒл€ окисл€ющегос€ галогенид-иона на≠писать молекул€рное уравнение реакции.
+ 2H+/NO + H2O). —опоставлением электродных потенциалов установить, какой из галоге≠нид-ионов будет окисл€тьс€ до свободного состо€ни€ и какие не будут. ƒл€ окисл€ющегос€ галогенид-иона на≠писать молекул€рное уравнение реакции.
23. ¬ подкисленный раствор смеси солей Kcl, Kbr и KJ прибавлен в достаточном количестве раствор KMnO4. «аписать редокси-цепи дл€ каждого галогенид-иона, обозначить электродные потенциалы, отметить знаки полюсов, направление перемещени€ электронов: вы≠числить Ёƒ— цепей. ¬се ли галогенид-ионы могут быть окислены до свободного состо€ни€ действием перман≠ганат-иона? Ќаписать соответствующие ионные уравне≠ни€ реакций окислени€-восстановлени€. ака€ из трех рассматриваемых реакций будет протекать наиболее и кака€ наименее интенсивно?
|
|
|
24. раствору сульфида натри€ прибавлена азотна€ кис≠лота. ∆идкость мутнеет вследствие образовани€ сво≠бодной серы. Ќаписать ионное уравнение реакции. «а≠писать редокси-цепь, отвечающую данному случаю. ”казать электрод-восстановитель и электрод-окисли≠тель, направление перемещени€ электронов и Ёƒ— цепи.
25. ћожно ли окислить Cr2(SO4)3 действием KMnO4 в кис≠лой среде с получением K2Cr2O7? «аписать электрон≠но-ионные уравнени€ фаз восстановлени€ и окислени€ (по типу ¬‘2ЦneЦ 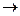 ќ‘2 и ќ‘1+neЦ
ќ‘2 и ќ‘1+neЦ 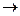 ¬‘1). «аписать редокси-цепь, указать знаки полюсов. ¬ывести моле≠кул€рное уравнение протекающей реакции.
¬‘1). «аписать редокси-цепь, указать знаки полюсов. ¬ывести моле≠кул€рное уравнение протекающей реакции.






