ТЕМА 11. СПЛАВИ КОЛЬОРОВИХ МЕТАЛІВ
План.
1. Сплави на основі міді, алюмінію та їх застосування.
2. Корозія металів і сплавів, захист від корозії.
Питання 1.
У сучасному машинобудуванні кольорові метали і сплави на їх основі займають важливе місце, а в електро-, радіотехніці, радіоелектроніці, авіації, космічній техніці вони є основними конструкційними матеріалами.
Мідні сплави
Мідними називають сплави., основним, компонентом, яких, є мідь. Найпоширенішими сплавами на основі міді є латуні та бронзи.
Латунями називають сплави міді з цинком та іншими легуючими елементами.
Легуючі елементи поліпшують властивості латуней.
Класифікація латуней.
Латуні класифікують за такими ознаками:
1. кількість легуючих елементів у сплаві,
2. способи виготовлення виробів зі сплавів.
1. За кількістю легуючих, елементів. Латуні поділяють на:
- прості;
- складні.
Прості латуні - це двокомпонентні сплави, які складаються лише з міді та цинку. Максимальний вміст цинку у латунях становить 45%. Чим більше цинку входить до складу латуні, тим вона має більшу міцність і меншу.пластичність. Найпластичнішими є латуні, які містять 30% цинку. Із збільшенням вмісту цинку до 42-45% збільшується міцність латуней, але збільшується крихкість. Саме тому латуні, які містять понад 45% цинку, на. практиці не використовують.
Складні латуні - це багатокомпонентні сплави, до складу яких крім міді та цинку входять легуючі елементи (нікель, олово, залізо, свинець, алюміній тощо). Легування впливає на механічні властивості! сплавів: збільшує міцність і зменшує пластичність. Свинець полегшує оброблення латуні різанням, алюміній, кремній, манган і нікель поліпшують її корозієстійкість.
2. За способом виготовлення виробів. Латуні поділяють на:
- деформівні;
- ливарні.
Деформівні латуні пластичні, а тому вироби з них виготовляють вальцюванням, волочінням тощо. Так отримують труби, дріт і т. ін.
Ливарні латуні мають добрі ливарні властивості. Саме тому вироби
з них отримують литтям у спеціальні, наперед виготовлені, форми.
Бронзи
Бронзами називають сплави, міді з Sn, Al, Be, Si, Mn, Pb тощо.
Бронзи мають добрі ливарні властивості. Серед бронз є пластичні та корозієстійкі. Із бронз в давнину виготовляли зброю, засоби праці тощо. Оскільки вони мають добрі ливарні властивості, з них виготовляли дзвони, гармати, ужиткові речі тощо.
У наш час бронзи використовують у машино- та приладобудуванні. Малий коефіцієнт тертя та стійкість до зносу роблять бронзи поки що незамінними для виготовлення вальниць, труб та інших деталей відповідальних і точних приладів.
За способом виготовлення виробів бронзи поділяють на:
1. ливарні;
2.деформівні.
З ливарних бронз вироби виготовляють литтям. З деформівних - тиском і різанням.
Відповідно бронзи поділяють на ливарні та деформівні. Найбільшого поширення набули олов'яні бронзи ливарні, які містять 6% олова та деформівні, вміст олова в яких більший. З них виготовляють пружини та інші деталі, які працюють за складних умов: великі навантаження та корозійні середовища. Олово - дорогий та дефіцитний метал.
Останнім часом усе ширше застосовують безолов'яні бронзи. До них належать сплави міді з алюмінієм, свинцем, нікелем, берилієм та іншими хімічними елементами. Ці бронзи порівняно з олов'яними мають кращі механічні властивості. Вони корозієстійкіші в агресивних середовищах. Так, алюмінієві бронзи корозієстійкі в морській воді та тропічній атмосфері, мають добрі механічні властивості, але гірші ливарні властивості, ніж олов'яні. Берилієві бронзи є міцнішими, пружнішими, повільніше окислюються на повітрі порівняно з іншими бронзами, саме тому з них виготовляють деталі для точних приладів, мембрани, пружини та інші пружні елементи. Це дорогі бронзи. Свинцеві бронзи мають добрі антифрикційні (фрикційний - від лат. - тертя) властивості та велику теплопровідність. З них виробляють складові вальниць ковзання.
Алюмінієві сплави
Алюмінієвими називають сплави, основним, компонентом, яких
є алюміній.
Щоб поліпшити властивості алюмінію, до нього додають Си, Мg,
Мn, Zп, Si, Ве, Ті тощо.
Для алюмінієвих сплавів характерні мала густина та велика питома міцність, яка для деяких марок сплавів наближається до питомої міцності дуже міцних сталей. Алюмінієві сплави використовують майже в усіх промисловостях, а найширше - в літако-, судно- та автомобілебудуванні, а також у будівництві.
За способом виготовлення виробів алюмінієві сплави поділяють на:
1. деформівні,
2. ливарні,
3. спечені.
Ці сплави є пластичними, добре зварюються, стійкі проти дії агресивних середовищ. Вироби з цих сплавів отримують штампуванням, пресуванням, волочінням, рідше - різанням та литтям.
Деформівні алюмінієві сплави поділяють на дві групи.
До першої групи належать сплави, які не зміцнюються термічною обробкою.
До другої групи належать сплави, міцність яких зростає після термічної обробки.
І. Алюмінієві сплави, які не зміцнюються термічною обробкою. Їх структура складається з кристалітів однорідного твердого розчину. Міцність алюмінію можна підвищити легуванням. Щоб отримати сплави, які не зміцнюються термічною обробкою, алюміній легують Мп або Мп і Мg. Отримані сплави мають більшу міцність, але меншу пластичність, ніж алюміній. Магній збільшує міцність сплавів, а манган - ще й корозієстійкість.
Із цих сплавів виготовляють баки для бензину, азотної та іншихкислот, труби. Їх використовують у літако- та суднобудуванні.
II. Алюмінієві сплави, які зміцнюються термічною обробкою. До
них належать дуралюміни, міцні, жароміцні, ковкі та інші сплавив Міцність цих сплавів підвищують термічною обробкою: гартуванням з подальшим старінням.
Старінням називають процес збільшення міцності сплавів під час нагрівання або після нього.
Відповідно старіння поділяють на природне та штучне. У процесі природного старіння міцність сплавів зростає після нагрівання та тривалого витримування на повітрі.
У процесі штучного старіння міцність сплавів зростає під часнагрівання.
1. Дуралюміни. Дуралюмінами (від лат. –твердий і алюміній) н азивають сплави алюмінію з міддю (2,2-4,8% Сu, магнієм (0,4-2,4% Мg) і манганом (0,4-0,8% Мп).
Типовим дуралюміном є сплав Д1. В основі маркування дуралюмінів лежить перша літера назви сплаву “Д”, після якої йдуть цифри, які означають умовний номер сплаву. Для з'ясування хімічного складу сплаву треба звернутися до довідкової літератури..
2. Міцні алюмінієві сплави. Ці сплави мають більшу міцність, але меншу пластичність, ніж дуралюміни. Їх використовують у літакобудуванні.
3. Жароміцні алюмінієві сплави. Їх використовують для виготовлення деталей, які працюють за температури 300°С. Це поршні, головки циліндрів, лопаті та диски компресорів турбореактивних двигунів тощо. Жароміцні сплави мають складніший порівняно з попередніми хімічний склад. Ці сплави досягають жароміцності за рахунок великої кількості Си, Мп та Ті.
4. Ковкі алюмінієві сплави. Ці сплави є пластичними. З них виготовляють деталі складної форми та середньої міцності для літаків. Вони добре зварюються контактним і аргонно-дуговим способами.
Ливарні алюмінієві сплави
Вироби з ливарних алюмінієвих сплавів отримують литтям, оскільки вони мають добрі ливарні властивості мають такі сплави, у структурі яких є евтектика. Саме тому кількість легуючих елементів у ливарних сплавах більша, ніж у деформівних. До ливарних сплавів належать сілюміни.
Сілюмінами називають сплави сіліцію з алюмінієм та іншими легуючими елементами.
Найчастіше використовують сілюміни, які містять 5-14% Si. Структура сілюмінів складається з твердого розчину і евтектики, яка містить 11,6% Si. Чим більше евтектики у сплаві, тим він має кращі ливарні властивості.
Крім сілюмінів добрі ливарні властивості мають сплави алюмінію з міддю, магнієм та іншими легуючими елементами
Алюмінієві сплави отримують спіканням порошків алюмінію та оксиду алюмінію або порошків алюмінію чи алюмінієвого сплаву з порошками легуючих елементів. Їх поділяють на:
1. спечені алюмінієві порошки;
2. спечені алюмінієві сплави.
1. Спечені алюмінієві порошки (САП). Ці сплави отримують спіканням порошків алюмінію та оксиду алюмінію.
Із збільшенням вмісту оксиду алюмінію зростають міцність і жароміцність сплавів. Вироби, отримані із сплавів САП, добре зварюються, мають вищу жаростійкість, ніж звичайні алюмінієві сплави. Вони можуть довгий час працювати за температур 350-500°С.
Сплави САП використовують у літако- та суднобудуванні, електротехніці, хемічній промисловості. З них виготовляють лопаті компресорів, теплообмінники тощо.
2. Спечені алюмінієві сплави (САС), Ці сплави отримують спіканням порошку алюмінію або порошку алюмінієвого сплаву (наприклад, дуралюміну) і порошків легуючих елементів (заліза, хрому, нікелю тощо).
За кімнатної температури САС мають вищу міцність, ніж САП. Із підвищенням температури навпаки. Вироби із сплавів САС витримують нагрівання до температур 350-400°С.
Магнієві сплави
Магнієвими називають сплави, основним компонентом яких є магній.
Магній - найлегший серед конструкційних матеріалів. Його густина дорівнює 1700 кг/м3. Він має незначні механічні властивості. Саме тому з чистого магнію не виготовляють конструкцій.
Для виготовлення конструкцій використовують сплави. На практиці використовують сплави магнію з алюмінієм, цинком, манганом та іншими елементами. Магнієві сплави легко ріжуться, добре зварюються мають порівняно велику пластичність і міцність, а також задовільні ливарні властивості. Істотний недолік цих сплавів - мала корозієстійкість.
Залежно від способу виготовлення виробів магнієві сплави поділяють на:
1. ливарні;
2. деформівні.
Із магнієвих сплавів виготовляють корпуси приладів, фотоапарати деталі літаків, двигунів тощо.
Для підвищення корозієстійкості, вироби з магнієвих сплаві оксидують. На оксидовану поверхню наносять лакофарбові покриття.
Нікелеві сплави
Нікелевими називають сплави., основним, компонентом, яких є нікель.
Нікель має велику міцність, пластичність і корозієстійкість. Відповідно ці властивості мають також сплави на його основі. Сплави, які містять понад 55% Nі, мають вищу жароміцність, ніж кращий жароміцні сталі. Вироби, виготовлені з них, витримують нагрівання до температур 800-1000°С.
Представниками нікелевих сплавів є ніхроми, німоніки, монель- метали тощо.
Ніхромами називають нікелеві сплави, основним легуючим елементом яких. є хром.
Ніхроми дуже жаростійкі. Тому з них виготовляють нагрівніелементи, які працюють без навантаження в окиснюючому середовищі.
Німоніками називають нікелеві сплави, до складу яких крім хрому, входять титан, алюміній, молібден, вольфрам тощо.
Із цих сплавів виробляють деталі газових турбін, які працюють за температур 650-850°С.
Монель- металами називають сплави нікелю з міддю, залізом та манганом.
Із них виготовляють монети, хірургічні інструменти.
Сплавами, які пам'ятають свою форму називають такі сплави, які в процесі нагрівання здатні відновлювати початкову форму виробів, виготовлених з них.
Першим сплавом, який «запам'ятав» свою форму, є нітинол. Цей сплав складається з 50% нікелю та 50% титану.
Суть ефекту «пам'яті форми» полягає у відновленні початкової форми виробу нагріванням. Отже, якщо виробу, виготовленому з такого сплаву, надати потрібної форми, а потім за нижчої температури змінити цю форму на іншу, то в процесі нагрівання виріб набуде початкової форми. Пам'ять - дуже цінна властивість сплавів.
Із нітинолу виготовляють пристрої для космічних апаратів та інші
вироби.
Щоб знизити температуру, за якої відновлюється «пам'ять», нітинол
легують 3-4% заліза.
Якщо з легованого нітинолу, який складається з 50% титану, 46-47% нікелю, 3-4% заліза, за кімнатної температури виготовити деталі, наприклад з'єднуючі муфти, заклепки тощо, і здеформувати їх у рідинному азоті, то, відігрівшись, вони «згадають» свою попередню форму і муфта охопить труби, герметичне з'єднавши їх. Як бачимо, легко можна уникнути таких операцій, як зварювання чи паяння. Крім того, отримане з'єднання надійніше,
За допомогою ефекту «пам'яті форми» встановлюють заклепки в труднодоступних місцях. Для цього заклепку з одного боку розрізають уздовж осі на певну глибину, кінці розводять і заклепку нагрівають. Потім за кімнатної температури кінці заклепки вирівнюють і встановлюють в отвір. Повторне нагрівання приводить до розведення кінців заклепки, унаслідок чого деталі з'єднуються.
Сплав нітинол застосовують у медицині, оскільки він має добру корозієстійкість, добру «пам'ять» і добру сумісність з живими тканинами організму. Його використовують у хірургії, при переломах кісток.
Науковці та інженери шукають нові сфери використання сплавів, які «пам'ятають» свою форму. Це і двигуни прямого перетворення теплоти на механічну енергію, і терморегулятори, і виконавчі механізми, наприклад, силова деталь приводу, виготовлена з нітинолу, випрямляючись у процесі нагрівання, може перемістити вантаж, замкнути електричні контакти, увімкнути автоматичний пристрій для гасіння пожежі тощо. А як зручно буде автомобілебудівникам або ремонтникам: пошкоджену деталь (наприклад, двері чи кузов) досить трохи нагріти, щоб повернути їй втрачену форму.
Проте широкому впровадженню сплавів з «пам'яттю форми» перешкоджає недосконалість технології отримання сплавів точного хімічного складу та структури.
Питання 2. Корозія металів і сплавів, захист від корозії
Метали та сплави на їх основі є основними конструкційними матеріалами. З них виготовляють найвідповідальніші деталі та механізми. Внаслідок взаємодії із зовнішнім середовищем деталі та механізми втрачають свою довговічність, що спричинює простоювання обладнання, втрату сировини, продукції, а часом навіть призводить до аварій з людськими жертвами.
Корозією називають руйнування виробів, виготовлених з металів і сплавів, під дією зовнішнього середовища.
Середовища, в яких руйнуються метали та сплави, називають агресивними або корозійними.
Прикладом цих середовищ є повітря, розчини солей, кислот, лугів, розплави металів, викидні та промислові гази, бензин, піт тощо. Ці середовища можуть розчинити метали та сплави або утворювати сполуки з ними:оксиди, нітриди тощо. Так, на поверхні виробів, виготовлених із сплавів на основі заліза (вугліцеві сталі, чавуни), утворюються оксиди у вигляді іржі бурого кольору.
На практиці мають місце випадки, коли на поверхні виробів неї утворюються продукти корозійного руйнування, тоді виявити пошкодження виробів дуже важко.
Корозійні середовища поділяють на:
§ електроліти;
§ неелектроліти.
Середовища-електроліти проводять електричний струм. До них належать розчини солей, кислот, лугів, морська вода тощо.
Середовища-неелектроліти не проводять електричного струму. Прикладом таких середовищ є викидні та промислові гази, спирт, бензин, мастила тощо.
Види корозії
У разі взаємодії корозійних середовищ з металами та сплавами спостерігається кілька видів корозії, які класифікують за такими ознаками як:
І.Механізм взаємодії,
ІІ.Умови взаємодії тощо.
І. За механізмом взаємодії. Залежно від механізму взаємодії зовнішнього середовища з металами та сплавами корозію поділяють на:
§ хімічну;
§ електрохімічну.
Хімічною корозією називають руйнування виробів, виготовлених, з металів і сплавів, у середовищах-неелектролітах.
Прикладом такого виду корозії є руйнування деталей нагрівних печей, казанів, турбін, двигунів внутрішнього згоряння, сопел реактивних
двигунів тощо. У разі взаємодії газового середовища (пічні та викидні гази) з металевими виробами на їх поверхні утворюються різні хімічні сполуки (наприклад, оксиди, сульфіди тощо) у вигляді плівок.
Чим вища температура середовища, тим інтенсивніше кородує метал, оскільки зростають швидкість дифузії газів через плівку до металу і зустрічна дифузія атомів металу. У разі утворення не дуже щільної та міцної плівки газове середовище може різко прискорити руйнування, виробів. Прикладом металів, на поверхні яких утворюється нещільна (крихка) оксидна плівка, є залізо, вуглецеві сталі та чавуни. Вони -надзвичайно швидко руйнуються під дією газових середовищ, оскільки їх оксидні плівки неміцні, а в разі незначної зміни температури або навантаження ці плівки відшаровуються. Поверхня виробу «оголюється» і кисень чи інший газ знову взаємодіє з металом виробу. З часом виріб тоншає, оскільки утворена плівка знову обсипається.
Отже, оксидні плівки, які утворюються на поверхні виробів, виготовлених з вуглецевих сталей і чавунів, не можуть захистити їх від корозійного руйнування. Те саме спостерігається з виробами, виготовленими з ніобію, молібдену, вольфраму тощо які працюють в атмосфері повітря чи кисню за температур 400-500°С.
Якщо на поверхні виробів утворюються міцні та щільні оксидні плівки, то корозійне руйнування сповільнюється. Прикладом таких металів є хром, алюміній та сплави на їх основі. Саме тому на практиці використовують леговані сталі, які витримують дію газових середовищ до 900°С, у той час як вуглецеві легко руйнуються за температур понад 500°С. Легування сталі хромом, алюмінієм, нікелем підвищує корозіє-стійкість сталей до температури 850-900°С.
Рідини-неелектроліти руйнують нафтогони й обладнання каталізного та термічного крекінгів нафтопродуктів та інші металеві вироби. Швидкість корозії в рідинах-неелектролітах (спирти, бензин, газ, нафта тощо) невелика, але зростає за наявності в них домішок, особливо сірки та кисню й підвищення температури середовища. Рідини неорганічного походження агресивні, тому важливо не помилитись у виборі матеріялу для виготовлення конструкцій або захисного покриття. Так, для рідин із вмістом брому придатне обладнання, виготовлене з танталу, а з вмістом сірки - з алюмінію.
Електрохемічною корозією називають руйнування виробів, виготовлених з металів і сплавів у середовищах-електролітах.
Це найпоширеніший вид корозії. Електрохемічна корозія характеризується протіканням електричного струму в електроліті, переходом атомів металу в йонізований стан та іншими електрохемічними процесами. Прикладом електрохемічної корозії є руйнування металевих конструкцій і виробів, які перебувають у середовищі вологого повітря, в морській та річковій воді тощо.
Якщо в контакті з електролітом перебувають два метали, то механізм корозії нагадує роботу гальванічного елемента, в якому метал із меншим електродним потенціалом (анод) безперервно розчиняється, а з більшим (катод) - відновлюється.
Запишемо ряд металів, розміщених у порядку зменшення їх електродних потенціалів:

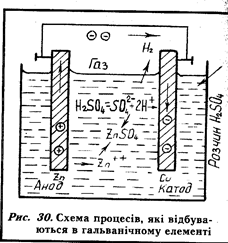
Якщо в розчин сірчаної кислоти (середовище-електроліт) помістити пластини, виготовлені з міді та цинку і з'єднати їх зовнішні кінці електричним привідником (рис. ЗО), то утвориться гальванічна елемент, в якому мідь, що має більший електродний потенціал (+0.34), ніж цинк (-0,76), не розчиняється, а є лише місцем нейтралізації йонів електроліту. Позитивно заряджені йони цинку (Zn  ) перейдуть в електроліт, а електрони потечуть по зовнішньому електричному провіднику до мідної пластинки, де нейтралізують позитивно заряджені йони водню (Н
) перейдуть в електроліт, а електрони потечуть по зовнішньому електричному провіднику до мідної пластинки, де нейтралізують позитивно заряджені йони водню (Н  ). Атоми водню з'єднуються в молекули (Н
). Атоми водню з'єднуються в молекули (Н  ) і у вигляді бульбашок виходять з розчину електроліту. Ця модель дає можливість пояснити причину руйнування поверхні металу, який має неоднорідну будову (різні компоненти, фази, неметалеві включення, зони з різними залишковими напруженнями тощо).
) і у вигляді бульбашок виходять з розчину електроліту. Ця модель дає можливість пояснити причину руйнування поверхні металу, який має неоднорідну будову (різні компоненти, фази, неметалеві включення, зони з різними залишковими напруженнями тощо).
Отже, поверхня металу - це множина мікроелементів (анодних і катодних ділянок), коротко замкнених через сам метал. Кожна ділянка має певний електродний потенціал.
|
Робота мікрогальванічних пар починається під час контакту з електролітом: ділянки сплаву з меншим потенціалом (аноди) руйнуються, а з більшим (катоди) - залишаються без зміни.
Однофазні сплави стійкіші в середовищах-електролітах, ніж багатофазні, але менш стійкі, ніж чисті метали.
Швидкість корозійного руйнування тим більша, чим далі стоять один від одного метали у ряді електродних потенціалів.
II. За умовами взаємодії. Залежно від умов, в яких працюють машини, агрегати та перебувають металеві конструкції, розрізняють кілька видів корозії:
§ газову,
§ атмосферну,
§ підземну,
§ біологічну,
§ корозію під дією струмів тощо.
Газова корозія спричинюється дією на металеві вироби викидних і промислових газів та теплоти, оскільки ці гази завжди нагріті до високих температур.
У разі атмосферної корозії агресивним середовищем є сконцентрована на поверхні металевого виробу волога, агресивність якої зростає із збільшенням у ній газів: О  , СО
, СО  , SO
, SO  тощо. Цей вид корозії найпоширеніший, оскільки близько 80 % металовиробів і конструкцій експлуатуються і зберігаються під «відкритим небом».
тощо. Цей вид корозії найпоширеніший, оскільки близько 80 % металовиробів і конструкцій експлуатуються і зберігаються під «відкритим небом».
У разі підземної (ґрунтової) корозії середовищем, яке руйнує металеві конструкції (труби, кабелі та інші підземні комунікації), є ґрунтова волога. Швидкість корозії зростає в торф'янистих і болотистих грунтах. Наявність мікроорганізмів і продуктів їх життєдіяльності руйнують навіть захисні покриття конструкцій.
Вивчення морських глибин, добування нафти з дна морів, створення потужного надводного та підводного морського флоту призводять до великих втрат металів у дуже агресивному середовищі, яким є морська вода. Вода крім хлоридів металів містить кисень та інші речовини, які спричинюють корозію.
Великих втрат завдає корозія під дією блукаючих струмів. Особливо небезпечним є постійний струм. Спостерігається цей вид корозії навколо трамвайних ліній і ліній електропоїздів. Під час руху трамваїв та електропоїздів частина електричного струму проникає в грунт, доходить до труб, якими транспортують нафту, воду, газ та інших підземних металевих конструкцій, анодні ділянки яких руйнуються. Це дуже небезпечний вид корозії: струм силою 1 А за рік «з'їдає» 9 кг заліза, 3 кг алюмінію, 11 кг цинку і міді, 34 кг свинцю. Радіус дії цього виду корозії досягає десятків кілометрів.
Види корозійного руйнування
Корозійне руйнування металів і сплавів починається з поверхні, тобто на межі металевий виріб - середовище, і поступово поширюється в глибину металу.
Найпоширенішими видами корозійного руйнування металів і сплавів є:
1.Суцільне,
2.Місцеве (рис. 31).
1. Суцільне руйнування. При суцільному корозійному руйнуванні середовище взаємодіє з металевими виробами по всій поверхні, але з різною швидкістю. Саме тому цей вид руйнування поділяють на:
§ Рівномірне;
§ Н ерівномірне.
У разі рівномірного руйнування (рис. 31,а) швидкість взаємодії середовища з металом однакова, а в разі нерівномірного (рис. 31,6) - різна на різних ділянках поверхні виробів. Відповідно середовище поширюється в глибину металу на однакову або різні відстані.
2. Місцеве руйнування. При цьому виді руйнування середовище взаємодіє з металами на окремих ділянках поверхні виробів.
Місцеве руйнування поділяють на:
§ плямисте,
§ виразкове,
§ точкове,
§ підповерхневе,
§ вибіркове,
§ міжкристалітне,
§ транскристалітне тощо.
Плямисте руйнування (рис. 31,в) спостерігається на виробах виготовлених із латуні, які перебували в морській воді. На поверхні латунних виробів утворюються плями. Глибина плям невелика.
Якщо середовище проникає на велику глибину, то кажуть, що має місце виразкове руйнування (рис. 31,г). Так руйнується сталь, вироби з якої довгий час перебували у грунті.

Точкове руйнування (рис, 31,д) характеризується утворенням вузьких кратероподібних (аж до наскрізних) заглиблень. Цей вид руйнування спостерігається на поверхні виробів, виготовлених із нержавіючої сталі, після дії на них морської води.
Підповерхневе руйнування (рис, 31,е) спостерігається тоді, коливироби покриті захисними покриттями (лаком, фарбою тощо). Продукт корозійного руйнування не можуть виноситися в середовище, оскільки поверхня виробу прикрита покриттям. Це спричиняє здуття покриття та розшарування металу.
Суть вибіркового руйнування (рис. 31,є) полягає в тому, що середовище взаємодіє з певними хімічними елементами або фазами матеріалів, з яких виготовлені вироби. Так, у сірих чавунах руйнується ферит і перліт, а графітовий каркас залишається; у латунях середовище взаємодіє із цинком і приповерхневий шар латунних виробів складається з губчатої міді.
Міжкристалітне руйнування (рис. 31,ж). Середовище взаємодіє спочатку з домішками, які перебувають на межах кристалітів, а потім приступає до розчинення металів. Це дуже небезпечний вид руйнування, який може спричинити раптову аварію. Це саме стосується також транскристалітного руйнування (рис. 31,з).
Корозієстійкість металів і сплавів
Корозієстійкістю металів і сплавів та інших конструкційних. матеріалів називають здатність їх, чинити опір дії зовнішніх. агресивних середовищ.
Корозієстійкість металів і сплавів оцінюють 2 методами:
1. Візуально;
2. Кількісно.
У разі візуального способу оцінки корозієстійкості вироби, які перебували під дією агресивного середовища, оглядають. Під час огляду визначають стан поверхні (блискуча чи тьмяна). Наявність на поверхні продуктів корозії, міцність з'єднання продуктів корозії з поверхнею виробів.
Кількісне визначення корозієстійкості грунтується на визначенні швидкості зміни маси виробів після перебування їх в агресивному середовищі, яку визначають з формули:

Корозієстійкість металів і сплавів можна визначити також за зміною їх механічних властивостей та електричного опору.






