» растворами щелочей
ѕри взаимодействии металлов с агрессивными средами металл выступает в качестве восстановител€. ’имическую активность (восстановительную способность) металла характеризует величина электродного потенциала.
—тандартным электродным потенциалом называют его электродный потенциал, возникающий при погружении металла в раствор собственной соли с концентрацией  =1 моль/л, измеренный по отношению к стандартному водородному электроду, потенциал которого при 25 0— условно принимаетс€ равным нулю.
=1 моль/л, измеренный по отношению к стандартному водородному электроду, потенциал которого при 25 0— условно принимаетс€ равным нулю.
„ем меньше значение  , тем большими восстановительными свойствами обладает данный металл.
, тем большими восстановительными свойствами обладает данный металл.
–асполага€ металлы в р€д по мере возрастани€ их стандартных электродных потенциалов, получаем р€д стандартных окислительно-восстановительных потенциалов металлов (табл. ѕ.6). ¬ этом р€ду все металлы условно дел€т на активные, средней активности и малоактивные:


 Li Rb K Cs Ba Sr Na Mg Be Al Mn Cr Zn Fe Cd Co Ni Sn Pb H2 Bi Cu Hg Ag Pt Au
Li Rb K Cs Ba Sr Na Mg Be Al Mn Cr Zn Fe Cd Co Ni Sn Pb H2 Bi Cu Hg Ag Pt Au
јктивные металлы —редней активности ћалоактивные
¬ роли окислител€ в растворах кислот, щелочей и в воде выступает среда (потенциалы в табл. ѕ.8). –еакции возможны, если потенциал окислител€ больше потенциала восстановител€.
¬ нейтральной и щелочной среде в роли окислител€ выступаетЌ2ќ:
2Ќ2ќ + 2 ē = Ќ2 + 2ќЌ Ч
¬ растворах разбавленных кислот (HCl, H2SO4) - окислитель Ќ+:
2Ќ + + 2 ē = Ќ2
¬ присутствии кислорода процесс восстановлени€ протекает с участием кислорода, так как он обладает бóльшими окислительными свойствами, чемЌ2ќ и Ќ+: O2 + 4 ē + 4Ќ + = 2Ќ2ќ (в кислой среде);
ќ2 + 4 ē + 2Ќ2ќ = 4ќЌ Ч (в щелочной и нейтральной средах).
¬ H2SO4 (конц.) и HNO3 (разб.), HNO3 (конц.) окислителем €вл€ютс€ анионы кислот. —тепень восстановлени€ анионов определ€етс€ активностью металла:
H2SO4 (конц.) + Me (активные) Ѓ сульфат ће + H2S + Ќ2ќ
H2SO4 (конц.) + Me (средней активности) Ѓ сульфат ће +S + Ќ2ќ
H2SO4 (конц.) + Me (малоактивные) Ѓ сульфат ће + SO2+ Ќ2ќ
HNO3 (разб.) + Me (активные) Ѓ нитрат ће + NH4NO3 + Ќ2ќ
HNO3 (разб.) + Me (средней активности) Ѓ нитрат ће +N2, N2O + Ќ2ќ
HNO3 (разб.) + Me (малоактивные) Ѓ нитрат ће + NO + Ќ2ќ
HNO3 (конц.) + Me (независимо от активности) Ѓ нитрат ће + NO2 + Ќ2ќ
¬нимание! “ри распространенных металла Ц Al, Cr, Fe Ц на холоде не раствор€ютс€ в H2SO4(конц.) и HNO3(конц.). ¬ этих кислотах они пассивируютс€, т. е. покрываютс€ тонкой прочной пленкой, предохран€ющей их от разрушени€. –еакции протекают только при повышенной температуре.
«адание к подразделу 4.2
»спользу€ потенциалы (табл. ѕ.6, ѕ.7, ѕ.8), допишите уравнени€ реакций (по две дл€ каждого варианта), составив к ним электронно-ионные схемы. ƒл€ реакций металлов с H2SO4 (конц.) и HNO3 значение потенциала окислител€ более 1 ¬. ќцените практическую устойчивость металлов в данной среде.
| 281. а) Pb + KOH+ H2O + O2 б) Cu + H2SO4 (конц.) | 291. а)Al + HNO3 (разб.) б) Cr + NaOH + ќ2 |
| 282. а)Al + H2O + O2 б) Mg + HNO3 (разб.) | 292. а)Al + NaOH + H2O б) Cu + HNO3 (разб.) |
283. а)Al + HNO3 (конц.)  б) Sn + NaOH + O2 + H2O
б) Sn + NaOH + O2 + H2O
| 293. а)Al + H2SO4 (конц.)  б) Sn + H2O + O2
б) Sn + H2O + O2
|
| 284. а)Al + NaOH + H2O + O2 б) Zn + H2SO4 (конц.) | 294. а)Cr + NaOH + H2O б) Be + HNO3 (разб.) |
285. а)Al+HNO3 (конц.)  б) Zn + NaOH + H2O + O2
б) Zn + NaOH + H2O + O2
| 295. а)Fe + H2SO4 (конц.)  Fe3+
б) Al + H2O Fe3+
б) Al + H2O
|
| 286. а)Mg + H2O б) Zn + H2SO4 (разб.) + O2 | 296. а)Zn + HNO3 (конц.) б) Al + KOH+ H2O |
| 287. а)Fe + HNO3 (разб.) б) Zn + H2O + O2 | 297. а)Zn + H2SO4 (конц.) б) Co + NaOH+ H2O + O2 |
288. а)HNO3(разб.)+ Fe  Fe3+
б) Zn + NaOH + H2O Fe3+
б) Zn + NaOH + H2O
| 298. а) Fe + HNO3(конц.)  Fe3+
б) Al + H2O + O2 Fe3+
б) Al + H2O + O2
|
| 289. а)Zn + H2O + O2 б) Cu + H2SO4 (конц.) | 299. а)Zn + NaOH + H2O б) Cu + HNO3 (конц.) |
| 290. а)Zn + NaOH + H2O + O2 б) Cd + HNO3 (разб.) | 310. а)Zn + HNO3 (разб.) б) Cu + NaOH+ H2O + O2 |
√альванические элементы
|
|
|
√альваническими элементами называют устройства, в которых энерги€ окислительно-восстановительных реакций преобразуетс€ непосредственно в электрическую.
ћетодика рассмотрени€ работы гальванических элементов:
Ј —оставл€ют схему гальванического элемента:
(Ц) Me1 / Me1n + // Me2 m+ / Me2 (+)
Ј ѕо уравнению Ќернста наход€т потенциалы электродов.
Ј ”казывают движение электронов во внешней цепи: от электрода с меньшим потенциалом к электроду с более высоким потенциалом.
Ј «аписывают уравнени€ электродных процессов, определ€ют характер этих процессов.
Ј —оставл€ют суммарное уравнение окислительно-восстановительной реакции, протекающей в гальваническом элементе.
Ј –ассчитывают величину Ёƒ— гальванического элемента как разность потенциалов положительного и отрицательного электродов.
ѕример 1. √альванический элемент с водородным электродом.
Ј —хема Zn / ZnSO4 // H2SO4, Ќ2 / Pt.
 1 моль/л,
1 моль/л,  1 моль/л, “ = 298 , P = 101,3 кѕa.
1 моль/л, “ = 298 , P = 101,3 кѕa.
Ј Ёлектродные потенциалы
 = 0 ¬,
= 0 ¬,  = - 0,76 ¬ (при
= - 0,76 ¬ (при  1 моль/л).
1 моль/л).
Ј Ќаправление движени€ электронов во внутренней цепи - от цинкового электрода к водородному, так как потенциал цинкового электрода меньше.
ē 

(Ц) Zn / ZnSO 4 // H2SO4, Ќ2 / Pt (+)
 | |||
 |
SO42 -
Ј ”равнени€ электродных процессов:
Zn (-): Zn - 2 ē = Zn 2+ - процесс окислени€;
Pt (+): 2Ќ ++ 2 ē = Ќ 2 ≠ - процесс восстановлени€.
Ј —уммарное уравнение:
Zn + 2Ќ + = Zn 2+ + Ќ 2 ≠ Zn + H2SO4 = ZnSO4 + Ќ 2 ≠
Ј –асчет величины Ёƒ—:
Ёƒ— = ≈ 0Ox - ≈ 0Red = 0 Ц (- 0,76) = 0,76 ¬.
ѕример 2. онцентрационный гальванический элемент
ќба электрода из одного металла, но растворы солей, в которые погружены электроды, разной концентрации.
Ј —хема гальванического элемента:
Ni / NiSO 4( = 10-4 моль/л)// NiSO 4 (
= 10-4 моль/л)// NiSO 4 ( =1моль/л) / Ni
=1моль/л) / Ni
—тандартный электродный потенциал  = - 0,25 ¬.
= - 0,25 ¬.
Ј ¬ычисление электродных потенциалов по уравнению Ќернста:
 =
=  +
+  Ј lg
Ј lg  = - 0,25 +
= - 0,25 +  Јlg 10 - 4 = - 0,309 B.
Јlg 10 - 4 = - 0,309 B.
 =
=  = - 0,25 B.
= - 0,25 B.
Ј Ќаправление движени€ электронов по внешней цепи от Ni1 электрода к Ni2, так как  >
> 
ē
 |
(-) Ni1 / NiSO4 (10 - 4 ћ) // NiSO4 (1 ћ) / Ni 2 (+)
 | |||
 |
SO42Ц
Ј ”равнени€ электродных полуреакций:
Ni1 (-): Ni - 2 ē = Ni 2+ - процесс окислени€;
Ni2 (+): Ni2+ + 2 ē = Ni - процесс восстановлени€.
Ј –асчет величины Ёƒ—:
|
|
|
Ёƒ— =  -
- 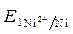 = - 0,25 - (- 0,309) = 0,059 ¬.
= - 0,25 - (- 0,309) = 0,059 ¬.
«адани€ к подразделу 4.3
ƒл€ предложенных гальванических элементов рассчитайте электродные потенциалы и Ёƒ—. ≈сли концентраци€ раствора не указана, потенциал примите стандартным (табл.ѕ.6). Ќапишите уравнени€ анодного и катодного процессов, молекул€рное уравнение токообразующей реакции, составьте схему и укажите направлени€ движени€ электронов и ионов.
301. Al / Al2(SO4)3, 0,005 M // NiSO4, 0,01 ћ / Ni
302. Ni / NiSO4, 0,1 M // H2SO4 / H2 (Pt)
303. Sn / SnSO4 // Cr2(SO4)3, 0,05 M / Cr
304. (Pt) H2 / H2SO4 // Al2(SO4)3, 0,005 M / Al
305. Cu / CuSO4, 0,1 M // H2SO4 / H2 (Pt)
306. Ag / AgNO3, 0,01 M // H2SO4 / H2 (Pt)
307. Co / CoSO4, 0,01 M // CoSO4 / Co
308. Zn / ZnSO4, 0,1 M // FeSO4, 0,01 M / Fe
309. Ag / AgNO3, 0,01 M // Zn(NO3)2 / Zn
310. (Pt) H2 / H2SO4 // ZnSO4, 0,01 M / Zn
311. Cd / Cd(NO3)2, 0,1 M // Cd(NO3)2, 0,001 M / Cd
312. Ni / NiSO4, 0,001 M // NiSO4 / Ni
313. Fe / FeCl2 // FeCl2, 0,01 M / Fe
314. Cr / Cr2(SO4)3, 0,005 M // ZnSO4 / Zn
315. Zn / Zn(NO3)2, 0,001 M // Zn(NO3)2 / Zn
316. Ag / AgNO3 // Cr(NO3)3, 0,005 M / Cr
317. Cd / CdCl2, 0,1 M // CuCl2, 0,1 M / Cu
318. Ti / Ti2(SO4)3, 0,5 M // CuSO4 / Cu
319. Sn / SnSO4, 0,01 M // Fe2(SO4)3 / Fe
320. Ag / AgNO3, 0,0001 M // Pb(NO3)2, 0,1 M / Pb






