ќЅў»≈ ” ј«јЌ»я –≈Ў≈Ќ»ё «јƒј„
1. ”казать основные законы и формулы, на которых базируетс€ решение, разъ€снить буквенные обозначени€ формул. ≈сли при решении задач примен€етс€ формула, полученна€ дл€ частного случа€, не выражающа€ какой-нибудь физический закон, или не €вл€юща€с€ определением какой-нибудь физической величины, то ее следует вывести.
2. ƒать чертеж, по€сн€ющий содержание задачи (в тех случа€х, когда это возможно).
3. —опровождать решение задачи краткими, но исчерпывающими по€снени€ми.
4. ѕолучить решение задачи в общем виде.
5. ѕодставить в правую часть полученной рабочей формулы вместо символов величин обозначени€ единиц, произвести с ними необходимые действи€ и убедитьс€ в том, что полученна€ при этом единица соответствует искомой величине.
6. ѕодставить в рабочую формулу числовые значени€ величин, выраженные в единицах одной системы.
7. ѕроизвести вычисление величин, подставленных в формулу, руководству€сь правилами приближенных вычислений, записать в ответе числовое значение и сокращенное наименование единицы искомой величины.
8. ќценить, где это целесообразно, правдоподобность численного ответа.
–»“≈–»» ќ÷≈Ќ»¬јЌ»я »Ќƒ»¬»ƒ”јЋ№Ќџ’ «јƒјЌ»…
¬ каждом модуле студент должен защитить 4 задачи. ќдна задача оцениваетс€ в 25 баллов.
| 22 - 25 баллов | «адача решена верно. ¬ оформлении присутствует дано, найти, чертеж. ”казаны основные законы и формулы, на которых базируетс€ решение, разъ€снены буквенные обозначени€ в формулах, получена расчетна€ формула. ѕроведена проверка единиц измерени€. —тудент отвечает на вопросы по решению задачи. |
| 18 - 21 баллов | ¬ решении отсутствуют разъ€снени€ обозначений, нет проверки единиц измерени€, при вычислении допущены арифметические ошибки, которые став€т под сомнение правдоподобность численного ответа. —тудент не всегда по€сн€ет ход решени€. |
| 14 - 17 баллов | ¬ решении имеютс€ недочеты, нет чертежа, нарушена логика решени€ задачи. —тудент затрудн€етс€ отвечать на отдельные вопросы. ¬ерно решенна€ задача, сданна€ повторно (в первый раз решение было не верно). |
| 10 - 13 баллов | ¬ решении присутствуют элементы верного решени€, но при выводе расчетной формулы допущены ошибки. ѕри решении используетс€ "готова€" формула. |
| 7 - 9 баллов | «адача решена правильно, но студент не может по€снить ход решени€ задачи Ц очевидно, что решение задачи Ц плод чужого труда. ѕравильно решенна€задача без Ђзащитыї. |
“≈ћџ «јƒј„
I. √ј«ќ¬џ≈ «ј ќЌџ (графическа€)
II. √ј«ќ¬џ≈ «ј ќЌџ (расчетна€)
III. “≈ѕЋќ≈ћ ќ—“№ » ¬Ќ”“–≈ЌЌяя ЁЌ≈–√»я √ј«ј
IV. —“ј“»—“» ј
V. “≈–ћќƒ»Ќјћ» ј
VI. ѕƒ “≈ѕЋќ¬џ’ ћјЎ»Ќ
ћќЋ≈ ”Ћя–Ќјя ‘»«» ј. “≈–ћќƒ»Ќјћ» ј
I. √ј«ќ¬џ≈ «ј ќЌџ
(графическа€ задача)
1) ѕостроить данный цикл на PT-, VT- диаграммах
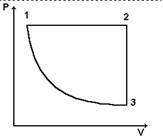
| 2) ѕостроить данный цикл на PT-, VT- диаграммах

|
3) ѕостроить данный цикл на PT-, VT- диаграммах

| 4) ѕостроить данный цикл на PT-, VT- диаграммах

|
5) ѕостроить данный цикл на PT-, VT- диаграммах

| 6) ѕостроить данный цикл на PT-, VT- диаграммах

|
7) ѕостроить данный цикл на PT-, VT- диаграммах

| 8) ѕостроить данный цикл на PT-, VT- диаграммах

|
9) ѕостроить данный цикл на PV-, VT- диаграммах

| 10) ѕостроить данный цикл на PV-, VT- диаграммах
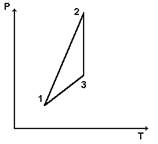
|
11) ѕостроить данный цикл на PV-, VT- диаграммах
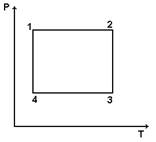
| 12) ѕостроить данный цикл на PV-, VT- диаграммах

|
13) ѕостроить данный цикл на PV-, VT- диаграммах

| 14) ѕостроить данный цикл на PV-, VT- диаграммах 
|
15) ѕостроить данный цикл на PV-, VT- диаграммах

| 16) ѕостроить данный цикл на PV-, VT- диаграммах

|
17) ѕостроить данный цикл на PV-, VT- диаграммах

| 18) ѕостроить данный цикл на PV-, PT- диаграммах

|
19) ѕостроить данный цикл на PV-, PT- диаграммах

| 20) ѕостроить данный цикл на PV-, PT- диаграммах

|
21) ѕостроить данный цикл на PV-, PT- диаграммах

| 22) ѕостроить данный цикл на PV-, PT- диаграммах

|
23) ѕостроить данный цикл на PV-, PT- диаграммах

|
24) ѕостроить данный цикл на PV-, PT- диаграммах

|
25) ѕостроить данный цикл на PV-, PT- диаграммах

| 26) ѕостроить данный цикл на PV-, PT- диаграммах

|
II. √ј«ќ¬џ≈ «ј ќЌџ
|
|
|
2.1. Ѕаллон объемом 20 литров заполнен азотом при температуре 400 . огда часть газа израсходовали, давление в баллоне понизилось на 200 кѕа. ќпределить массу израсходованного азота. ѕроцесс считать изотермическим.
2.2. ¬ баллоне объемом 15 литров находитс€ аргон под давлением 600 кѕа и температуре 300 . огда из баллона было вз€то некоторое количество газа, давление в баллоне понизилось до 400 кѕа, а температура установилась 260 . ќпределить массу аргона, вз€того из баллона.
2.3. ¬ычислить плотность азота, наход€щегос€ в баллоне под давлением 2 ћѕа и имеющего температуру 400 .
2.4. ќпределить плотность смеси 4 г гели€ и 32 г кислорода при температуре 300 и давлении 100 кѕа.
2.5. ¬ сосуде объемом 40 литров находитс€ кислород при температуре 300 . огда часть газа израсходовали, давление в баллоне понизилось на 100 кѕа. ќпределить массу израсходованного кислорода. ѕроцесс считать изотермическим.
2.6. ќдин баллон объемом 10 л содержит кислород под давлением 1,5 ћѕа, а другой баллон объемом 22 л содержит азот под давлением 0,6 ћѕа. огда баллоны соединили, оба газа смешались, образовав однородную смесь. Ќайти парциальные давлени€ обоих газов в смеси и полное давление смеси.
2.7. —месь водорода и азота общей массой 290 г при температуре 600 и давлении 2,46 ћѕа занимает объем 30 л. ќпределить массу водорода и массу азота.
2.8. ¬ баллоне объемом 22,4 л находитс€ водород при нормальных услови€х. ѕосле того как в баллон было дополнительно введено некоторое количество гели€, давление в баллоне возросло до 0,25 ћѕа, а температура не изменилась. ќпределить массу гели€, введенного в баллон.
2.9. —месь состоит из водорода с массовой долей 1/9 и кислорода с массовой долей 8/9. Ќайти плотность этой смеси при температуре 300 и давлении 0,2 ћѕа.
2.10. —месь кислорода и азота находитс€ в сосуде под давлением 1,2 ћѕа. ќпределить парциальные давлени€ газов, если массова€ дол€ кислорода в смеси равна 20%.
|
|
|
2.11. —месь азота с массовой долей 87,5% и водорода с массовой долей 12,5% находитс€ в сосуде объемом 20 л при температуре 560 . ќпределить давление смеси, если масса смеси равна 8 г.
2.12. ћанометр на баллоне со сжатым газом при температуре 291 показывает давление 8,4 ћѕа. акое давление он будет показывать, если температура понизитс€ до 250 ? »зменением емкости баллона вследствие охлаждени€ пренебречь.
2.13. √аз при давлении 99 кѕа и при температуре 293 имеет объем 164 см3. аков объем той же массы газа при нормальных услови€х?
2.14. ќпределить удельный объем азота при температуре 300 и давлении 49 кѕа.
2.15. »з баллона со сжатым водородом емкостью 10 л вследствие неисправности вентил€ утекает газ. ѕри температуре 280 манометр показывал 490 кѕа. „ерез некоторое врем€ при температуре 290 манометр показал такое же давление. —колько утекло газа?
2.16. ѕо газопроводной трубе идет углекислый газ при давлении 390 кѕа и температуре 280 . акова скорость движени€ газа в трубе, если за 10 мин. протекает 2 кг углекислого газа и если площадь сечени€ канала трубы 5 см2?
2.17. ѕредположим, что температура воздуха в атмосфере зависит от высоты таким образом, что плотность воздуха по всей толще атмосферы одинакова. Ќа каком рассто€нии по вертикали разность температур равна 1 ?
2.18. ¬ вертикальном закрытом сверху и снизу цилиндре находитс€ движущийс€ с ничтожным трением поршень. Ќад и под поршнем наход€тс€ одинаковые массы одного и того же газа при температуре 300 . ¬ес поршн€ уравновешиваетс€ разностью сил давлений газа, если объем нижней части цилиндра в 3 раза меньше объема верхней части. аково будет соотношение объемов, если температура повыситс€ до 400 ?
2.19. “ри баллона емкостью 3, 7 и 5 л наполнены соответственно кислородом (200 кѕа), азотом (300 кѕа) и углекислым газом (60 кѕа) при одной и той же температуре. Ѕаллоны соедин€ют между собой, причем образуетс€ смесь той же температуры. аково давление смеси?
2.20. ќпределить мол€рную массу газа, свойства которого соответствуют свойствам смеси 160 г кислорода и 120 г азота.
2.21. ќпределить плотность смеси 4 г водорода и 32 г кислорода при температуре 280 и давлении 89 кѕа.
2.22. “опочный газ имеет следующий состав: —ќ2 Ц 21,4%, Ќ2ќ Ц 6,8%, N2 Ц 71,8%. ќпределить удельный объем такого газа при давлении 100 кѕа и температуре 500 .
2.23. —месь азота с массовой долей 70% и водорода с массовой долей 30% находитс€ в сосуде объемом 100 л при температуре 500 . ќпределить давление смеси, если масса смеси равна 100 г.
2.24. ¬ баллоне вместимостью V=25 л находитс€ водород при температуре T=290 K. ѕосле того, как часть водорода израсходовали, давление в баллоне понизилось на Dp=0,4 ћѕа. ќпределить массу m израсходованного газа.
2.25. ƒва сосуда одинакового объема содержат кислород. ¬ одном сосуде давление 2 ћѕа и температура 800 , в другом давление 2,5 ћѕа и температура 200 . —осуды соединили трубкой и охладили наход€щийс€ в них кислород до температуры 200 . ќпределить установившеес€ в сосудах давление.
2.26. 6 г углекислого газа (—ќ2) и 5 г закиси азота (N2O) заполн€ют сосуд объемом 2×10-3 м. аково общее давление в сосуде при температуре 127∞— ?
III. “≈ѕЋќ≈ћ ќ—“№ » ¬Ќ”“–≈ЌЌяя ЁЌ≈–√»я √ј«ј
3.1. ¬ закрытом сосуде смесь азота массой m1=56 г и кислорода массой m2=64 г. ќпределить изменение внутренней энергии этой смеси, если ее охладили на 20∞C.
3.2. ислород массой 1 кг находитс€ при температуре 320 . ќпределить: 1) внутреннюю энергию молекул кислорода; 2) среднюю кинетическую энергию вращательного движени€ молекул кислорода. √аз считать идеальным.
3.3. Ќайти показатель адиабаты дл€ смеси газов, содержащей гелий массой 8 г и кислород массой 2 г.
3.4. ќпределить внутреннюю энергию водорода, а также среднюю кинетическую энергию молекулы этого газа при температуре 300 , если количество вещества этого газа равно 0,5 моль.
3.5. ¬ сосуде вместимостью 6 л находитс€ при нормальных услови€х двухатомный газ. ќпределить удельную теплоемкость cv этого газа при посто€нном объеме.
|
|
|
3.6. ¬ычислить удельную теплоемкость воздуха cp, счита€ в его составе 20% кислорода и 80% азота.
3.7. 2 киломол€ аргона нагревают при изобарном процессе на 57∞C. ќпределить изменение внутренней энергии газа.
3.8. ќдноатомный газ при нормальных услови€х занимает объем V=5 л. ¬ычислить теплоемкость cv этого газа при посто€нном объеме.
3.9. ќпределить удельную теплоемкость cv смеси газов, содержащей V1 =5 л водорода и V2 =3 л гели€. √азы наход€тс€ при одинаковых услови€х.
3.10. ќпределить удельную теплоемкость cp смеси кислорода и азота, если количество вещества n1 первого компонента равно 2 моль, а количество вещества n2 второго равно 4 моль.
3.11. ¬ баллоне наход€тс€ аргон и азот. ќпределить удельную теплоемкость cv смеси этих газов, если массовые доли аргона (w1) и азота (w2) одинаковы и равны w=0,5. (ћассовой долей компонента в смеси называетс€ безразмерна€ величина, равна€ отношению массы компонента к массе смеси).
3.12. —месь газов состоит из хлора и криптона, вз€тых при одинаковых услови€х и в равных объемах. ќпределить удельную теплоемкость cp смеси.
3.13. ќпределить удельную теплоемкость cv смеси ксенона и кислорода, если количества вещества газов в смеси одинаковы и равны n.
3.14. Ќайти показатель адиабаты дл€ смеси газов, содержащей гелий массой 6 г и водород массой 4 г.
3.15. —месь газов состоит из аргона и азота, вз€тых при одинаковых услови€х и в одинаковых объемах. ќпределить показатель адиабаты такой смеси.
3.16. ќпределить удельную теплоемкость cр смеси газов, содержащей V1 =10 л водорода и V2 =5 л гели€. √азы наход€тс€ при одинаковых услови€х.
3.17. Ќайти показатель адиабаты дл€ смеси газов, содержащей азот массой 8 г и кислород массой 6 г.
3.18. Ќайти показатель адиабаты смеси водорода и неона, если массовые доли обоих газов в смеси одинаковы и равны 0,5. (ћассовой долей компонента в смеси называетс€ безразмерна€ величина, равна€ отношению массы компонента к массе смеси).
3.19. Ќа нагревание кислорода массой 160 г на DT=12 было затрачено количество теплоты 1,76 кƒж. ак протекал процесс: при посто€нном объеме или посто€нном давлении?
3.20. ќпределить удельную теплоемкость cv смеси углекислого газа массой 10 г и гели€ массой 4 г.
3.21. ѕри адиабатном сжатии газа его объем уменьшилс€ в n=10 раз, а давление увеличилось в k=21,4 раза. ќпределить отношение Cp/Cv теплоемкостей газов.
3.22. ƒл€ некоторого двухатомного газа удельна€ теплоемкость при посто€нном давлении равна 3,5 кал/(г×—). „ему равна мол€рна€ масса этого газа?
3.23. „ему равны удельные теплоемкости сv и сp некоторого двухатомного газа, если плотность этого газа при нормальных услови€х равна 1,43 кг/м3?
3.24. Ќайти удельные теплоемкости сv и сp некоторого газа, если известно, что мол€рна€ масса этого газа равна m=0,03 кг/моль и отношение Cp/Cv=1,4.
3.25. Ќайти удельную теплоемкость при посто€нном давлении газовой смеси, состо€щей из 3 кмоль аргона и 2 кмоль азота.
3.26. ќпределить отношение Cp/Cv теплоемкостей дл€ газовой смеси, состо€щей из 8 г гели€ и 16 г водорода.
IV. —“ј“»—“» ј
4.1. ќпределить среднюю длину свободного пробега молекул углекислого газа при температуре 100∞— и давлении 0,1 мм рт. ст. ƒиаметр молекулы углекислого газа прин€ть равным 3,2×10-8 см.
4.2. Ќайти число столкновений в 1 сек молекул углекислого газа при температуре 100∞—, если средн€€ длина свободного пробега при этих услови€х равна 8,7×10-2 см.
4.3. ѕри температуре 0∞— и некотором давлении средн€€ длина свободного пробега молекул кислорода равна 9,2×10-6 см. „ему будет равно число столкновений в 1 сек молекул кислорода, если произвести разрежение в сосуде до 0,01 первоначального давлени€? “емпература остаетс€ посто€нной.
|
|
|
4.4. Ќайти число столкновений в 1 сек молекул некоторого газа, если средн€€ длина свободного пробега при этих услови€х равна 7×10-4 см и средн€€ квадратична€ скорость 500 м/сек.
4.5. ќпределить среднюю длину свободного пробега молекул гели€ при температуре 100∞— и давлении 760 мм. рт. ст., если при этих услови€х коэффициент внутреннего трени€ дл€ него равен 1,3×10-4 ѕа×c.
4.6. ќпределить среднюю длину свободного пробега молекул гели€, если плотность гели€ 2,1×10-2 кг/м3.
4.7. ѕри некоторых услови€х средн€€ длина свободного пробега молекул газа равна 160 нм и средн€€ арифметическа€ скорость его молекул равна 1,95 км/с. „ему будет равно среднее число столкновений в 1 сек молекул этого газа, если при той же температуре давление уменьшить в 1,27 раз?
4.8. ¬ колбе объемом 100 см3 находитс€ 0,5 г азота. ќпределить среднюю длину свободного пробега молекул азота при этих услови€х.
4.9. ¬ сосуде находитс€ углекислый газ, плотность которого r=1,7 кг/м3; средн€€ длина свободного пробега его молекул при этих услови€х равна <l>=79 нм. Ќайти диаметр d молекул углекислого газа.
4.10. ќпределить среднюю длину свободного пробега молекул азота при температуре 17∞— и давлении 10 кѕа.
4.11. ¬ысотна€ обсерватори€ расположена на высоте 3250 м над уровнем мор€. Ќайти давление воздуха на этой высоте. “емпературу воздуха считать посто€нной и равной 5∞—. ћол€рную массу воздуха прин€ть равной 0,029 кг/моль. ƒавление воздуха на уровне мор€ равно 760 мм. рт. ст.
4.12. Ќа какой высоте давление воздуха составл€ет 75% давлени€ на уровне мор€? “емпературу воздуха считать посто€нной и равной 5∞—.
4.13. ќпределить плотность воздуха: 1) у поверхности «емли; 2) на высоте 4 км от поверхности «емли? “емпературу воздуха считать посто€нной и равной 0∞—. ƒавление воздуха у поверхности «емли равно 100 кѕа.
4.14. ќпределить плотность разреженного кислорода, если средн€€ длина свободного пробега <l> молекул равна 3 см.
4.15. ѕылинки, взвешенные в воздухе, имеют массу m=10-18 г. ¬о сколько раз уменьшитс€ их концентраци€ n при увеличении высоты на Dh=10 м? “емпература воздуха T=300 K.
4.16. Ќа сколько уменьшитс€ атмосферное давление p=100 кѕа при подъеме наблюдател€ над поверхностью «емли на высоту h=100 м? —читать, что температура T воздуха равна 290 K и не измен€етс€ с высотой.
4.17. Ќа какой высоте h над поверхностью «емли атмосферное давление вдвое меньше, чем на ее поверхности? —читать, что температура T воздуха равна 290 K и не измен€етс€ с высотой.
4.18. Ѕарометр в кабине лет€щего вертолета показывает давление p=90 кѕа. Ќа какой высоте h летит вертолет, если на взлетной площадке барометр показывал давление p0=100 кѕа? —читать, что температура T воздуха равна 290 K и не измен€етс€ с высотой.
4.19. Ќайти изменение высоты Dh, соответствующее изменению давлени€ на Dp=100 ѕа, в двух случа€х:1) вблизи поверхности «емли, где температура T1=290 K, давление p1=100 кѕа; 2) на некоторой высоте, где температура T2=220 K, давление p2=25 кѕа.
4.20. Ќайти среднюю длину свободного пробега <l> молекул водорода при давлении p=0,1 ѕа и температуре T=100 K.
4.21. ѕри каком давлении p средн€€ длина свободного пробега <l> молекул азота равна 1 м, если температура T газа равна 300 K?
4.22. Ѕаллон вместимостью V=10 л содержит водород массой m=1 г. ќпределить среднюю длину свободного пробега <l> молекул.
4.23. ќпределить среднюю длину свободного пробега молекул водорода при температуре 67∞— и давлении 100 кѕа.
4.24. ћожно ли считать вакуум с давлением p=100 мкѕа высоким, если он создан в колбе диаметром d=20 см, содержащей азот при температуре T=280 K? (¬акуум считаетс€ высоким, если длина свободного пробега молекул в нем много больше линейных размеров сосуда)
4.25. ќпределить плотность r разреженного водорода, если средн€€ длина свободного пробега <l> молекул равна 1 см.
4.26. Ќайти среднее число <z> столкновений, испытываемых в течение t=1 c молекулой кислорода при нормальных услови€х.
V. “≈–ћќƒ»Ќјћ» ј
5.1. јзот массой 0,1 кг был изобарно нагрет от температуры 200 до 400 . ќпределить работу, совершенную газом, полученную им теплоту и изменение внутренней энергии азота.
5.2. ислород массой 250 г, имеющий температуру 200 , был адиабатно сжат. ѕри этом была совершена работа 25 кƒж. Ќайти конечную температуру газа.
5.3. ¬о сколько раз увеличитс€ объем водорода, содержащий количество вещества 0,4 моль, при изотермическом расширении, если при этом газ получит 800 ƒж тепла. “емпература водорода 300 .
|
|
|
5.4. ¬одород занимает объем 10 м3 при давлении 0,1 ћѕа. ≈го нагрели при посто€нном объеме до давлени€ 0,3 ћѕа. ќпределить изменение внутренней энергии газа, работу, совершенную им, и теплоту, сообщенную газу.
5.5. ислород при неизменном давлении 80 кѕа нагреваетс€. ≈го объем увеличиваетс€ от 1 м3 до 3 м3. ќпределить изменение внутренней энергии кислорода, работу, совершенную им при расширении, а так же теплоту, сообщенную газу.
5.6. 10,5 г азота изотермичеси расшир€етс€ при температуре 250 , причем его давление измен€етс€ от 250 кѕа до 100 кѕа. Ќайти работу, совершенную газом при расширении.
5.7. ¬ цилиндре под поршнем находитс€ азот, имеющий массу 0,6 кг и занимающий объем 1,2 м3 при температуре 560 . ¬ результате нагревани€ газ расширилс€ и зан€л объем 4,2 м3, причем температура осталась неизменной. Ќайти изменение внутренней энергии газа, совершенную им работу и теплоту, сообщенную газу.
5.8. 10 г кислорода наход€тс€ под давлением 300 кѕа и температуре 283 . ѕосле нагревани€ при посто€нном давлении газ зан€л объем 10 л. Ќайти количество теплоты, полученное газом, изменение внутренней энергии газа и работу, совершенную газом при расширении.
5.9. 6,5 г водорода, наход€щегос€ при температуре 300 , расшир€ютс€ вдвое при посто€нном давлении за счет притока тепла извне. Ќайти количество теплоты, полученное газом, изменение внутренней энергии газа и работу, совершенную газом при расширении.
5.10. 2 кмоль углекислого газа нагреваютс€ при посто€нном давлении на 50 . Ќайти количество теплоты, полученное газом, изменение внутренней энергии газа и работу, совершенную газом при расширении.
5.11. ƒвухатомному газу сообщено количество теплоты 2 кƒж. √аз расшир€етс€ при посто€нном давлении. Ќайти работу расширени€ газа.
5.12. ѕри изобарическом расширении двухатомного газа была совершена работа 156,8 ƒж. акое количество теплоты было сообщено газу?
5.13. 7 г углекислого газа была нагрета на 10 в услови€х свободного расширени€. Ќайти работу расширени€ газа и изменение его внутренней энергии.
5.14. √елий, наход€щийс€ при нормальных услови€х, изотермически расшир€етс€ от 1 л до 2 л. Ќайти работу, совершенную газом при расширении, и количество теплоты, сообщенное газу.
5.15. 200 г азота нагреваютс€ при посто€нном давлении от 293 до 373 . акое количество теплоты поглощаетс€ при этом? аков прирост внутренней энергии газа? акую внешнюю работу производит давление газа?
5.16. Ќекотора€ масса азота при давлении 100 кѕа имела объем 5 л, а при давлении 300 кѕа Ц объем 2 л. ѕереход от первого состо€ни€ ко второму был сделан в два этапа: сначала по изохоре, а затем по изобаре. ќпределить изменение внутренней энергии, количество теплоты и произведенную работу.
5.17. Ќекотора€ масса азота при давлении 100 кѕа имела объем 5 л, а при давлении 300 кѕа Ц объем 2 л. ѕереход от первого состо€ни€ ко второму был сделан в два этапа: сначала по изобаре, а затем по изохоре. ќпределить изменение внутренней энергии, количество теплоты и произведенную работу.
5.18. ѕроизводитс€ сжатие некоторой массы двухатомного газа один раз изотермически, другой раз адиабатно. Ќачальные температура и давление сжимаемого газа оба раза одинаковы. онечное давление в 2 раза больше начального. Ќайти отношение работ сжати€ при адиабатном и изотермическом процессах.
5.19. ¬ четырехтактном двигателе ƒизел€ засосанный атмосферный воздух в объеме 10 л подвергаетс€ 12-кратному сжатию. ѕредполага€ процесс сжати€ адиабатным, определить конечное давление, конечную температуру и работу сжати€, если начальное давление и температура равны 100 кѕа и 283 .
5.20. ¬о сколько раз увеличитс€ давление водорода, содержащий количество вещества 4 моль, при изотермическом расширении, если при этом газ получит 1000 ƒж тепла. “емпература водорода 300 .
5.21. ¬одород занимает объем 10 м3 при давлении 1 ћѕа. ≈го нагрели при посто€нном объеме до давлени€ 3 ћѕа. ќпределить изменение внутренней энергии газа, работу, совершенную им, и теплоту, сообщенную газу.
5.22. јзот при неизменном давлении 100 кѕа нагреваетс€. ≈го объем увеличиваетс€ от 10 м3 до 30 м3. ќпределить изменение внутренней энергии азота, работу, совершенную им при расширении, а так же теплоту, сообщенную газу.
5.23. 20 моль кислорода нагреваютс€ при посто€нном давлении на 150 . Ќайти количество теплоты, полученное газом, изменение внутренней энергии газа и работу, совершенную газом при расширении.
5.24. Ќекотора€ масса азота при давлении 100 кѕа имела объем 5 л, а при давлении 300 кѕа Ц объем 2 л. ѕереход от первого состо€ни€ ко второму был сделан в два этапа: сначала по адиабате, а затем по изохоре. ќпределить изменение внутренней энергии, количество теплоты и произведенную работу.
5.25. ѕри уменьшении объема кислорода с 20 до 10 л его давление возросло со 100 до 250 кѕа. Ѕыл ли этот процесс адиабатическим? аково изменение внутренней энергии газа?
5.26. ќпределить работу расширени€ 110 г углекислого газа при увеличении его объема в 5 раз, если температура газа посто€нна и равна 293 . акое количество тепла нужно при этом сообщить газу?
VI. ѕƒ “≈ѕЋќ¬џ’ ћјЎ»Ќ
6.1. »деальный газ, совершающий цикл арно, 70% количества теплоты, полученной от нагревател€, отдает холодильнику. оличество теплоты, получаемое от нагревател€, равно 5 кƒж. ќпределить: 1) термический ѕƒ цикла; 2) работу, совершенную при полном цикле.
6.2. »деальный газ, совершающий цикл арно, получил от нагревател€ количество теплоты, равное 5,5 кƒж и совершил работу 1,1 кƒж. ќпределить: 1) термический ѕƒ цикла; 2) отношение температур нагревател€ и холодильника.
6.3. »деальный газ совершает цикл арно. “емпература нагревател€ 500 , холодильника 300 . –абота изотермического расширени€ газа составл€ет 2 кƒж. ќпределить: 1) термический ѕƒ цикла; 2) количество теплоты, отданное газом при изотермическом сжатии холодильнику.
6.4. ћногоатомный идеальный газ совершает цикл арно, при этом в процессе адиабатического расширени€ объем газа увеличилс€ в 4 раза. ќпределить термический ѕƒ цикла.
6.5. –абочее тело - идеальный газ - теплового двигател€ совершает цикл, состо€щий из следующих процессов: изобарного, адиабатического и изотермического. ¬ результате изобарного процесса газ нагреваетс€ от 300 до 600 . ќпределить термический ѕƒ теплового двигател€.
6.6. »деальна€ теплова€ машина работает по циклу арно. ¬ результате теплового процесса газ совершил работу в 9,8×103 ƒж и отдал холодильнику количество теплоты, равное 4,19×104 ƒж. ќпределить ѕƒ цикла.
6.7. √аз совершает цикл арно. “емпература нагревател€ равна 100∞—. акова температура холодильника, если 3/4 теплоты, получаемой от нагревател€ газ отдает холодильнику?
6.8. »деальна€ теплова€ машина, работающа€ по обратному циклу арно, потребл€ет мощность, равную 50 л.с. ѕри этом она берет теплоту от тела с температурой Ц10∞— и отдает ее телу с температурой +17∞—. Ќайти: 1) ѕƒ цикла; 2) количество теплоты, отн€тое у холодильника за 1 сек; 3) количество теплоты, отданное нагревателю за 1 сек.
6.9. »деальна€ теплова€ машина, работающа€ по циклу арно, получает за каждый цикл от нагревател€ 500 кал. “емпература нагревател€ 400 , температура холодильника 300 . Ќайти работу, совершаемую машиной за один цикл, и количество теплоты, отдаваемое холодильником за один цикл.
6.10. »деальна€ теплова€ машина работает по циклу арно. ќпределить ѕƒ цикла, если известно, что за один цикл была произведена работа 300 ƒж и холодильнику было передано 13,4 кƒж.
6.11. »деальна€ теплова€ машина, совершающа€ цикл арно, 80% количества теплоты, полученной от нагревател€, отдает холодильнику. оличество теплоты, получаемое от нагревател€, равно 1,5 ккал. ќпределить: 1) термический ѕƒ цикла; 2) работу, совершенную при полном цикле.
6.12. »деальна€ теплова€ машина, работающа€ по обратному циклу арно, совершает за один цикл работу 37 кƒж, при этом она берет теплоту от тела с температурой -10∞— и отдает ее телу с температурой +17∞—. Ќайти: 1) ѕƒ цикла; 2) количество теплоты, отн€тое у холодильника за один цикл; 3) количество теплоты, отданное нагревателю за один цикл.
6.13. ¬ цикле арно газ получил от теплоотдатчика теплоту Q1=500 ƒж и совершил работу ј=100 ƒж. “емпература теплоотдатчика “1=400 . ќпределить температуру “2 теплоприемника.
6.14. ¬ результате кругового процесса газ совершил работу 1 ƒж и передал охладителю количество теплоты 4,2 ƒж. ќпределить термический ѕƒ цикла.
6.15. —оверша€ замкнутый процесс, газ получил от нагревател€ количество теплоты 4 кƒж. ќпределить работу газа при протекании цикла, если его термический ѕƒ=0,1.
6.16. »деальный двухатомный газ, содержащий количество вещества n=1 моль, совершает цикл, состо€щий из двух изохор и двух изобар. Ќаименьший объем Vmin=10 л, наибольший Vmax= 20 л, наименьшее давление pmin= 246 кѕа, наибольшее pmax=410 кѕа. ѕостроить график цикла. ќпределить температуру газа дл€ характерных точек цикла и его термический ѕƒ.
6.17. »деальный газ, совершающий цикл арно, 2/3 количества теплоты Q1, полученного от нагревател€, отдает охладителю. “емпература T2 охладител€ равна 280 K. ќпределить температуру T1 нагревател€.
6.18. »деальный газ совершает цикл арно. “емпература T2 охладител€ равна 290 K. ¬о сколько раз увеличитс€ ѕƒ цикла, если температура нагревател€ повыситс€ от 400 K до 600 K?
6.19. »деальный газ совершает цикл арно. “емпература T1 нагревател€ в три раза выше температуры T2 охладител€. Ќагреватель передал газу количество теплоты Q1=42 кƒж. акую работу A совершил газ?
6.20. »деальный газ совершает цикл арно. “емпература T1 нагревател€ равна 470 K, температура T2 охладител€ равна 280 K. ѕри изотермическом расширении газ совершает работу A= 100 ƒж. ќпределить термический ѕƒ цикла, а также количество теплоты Q2, которое газ отдает охладителю при изотермическом сжатии.
6.21. »деальный газ совершает цикл арно. “емпература T1 нагревател€ в четыре раза выше температуры T2 охладител€. акую долю количества теплоты, получаемого за один цикл от нагревател€, газ отдает охладителю?
6.22. »деальный газ, совершающий цикл арно, получив от нагревател€ количество теплоты Q1=4,2 кƒж, совершил работу A=590 ƒж. Ќайти термический ѕƒ этого цикла. ¬о сколько раз температура T1 нагревател€ больше температуры T2 охладител€?
6.23. »деальный газ совершает цикл арно. –абота A1 изотермического расширени€ газа равна 5 ƒж. ќпределить работу A2 изотермического сжати€, если термический ѕƒ цикла равен 0,2.
6.24. Ќаименьший объем V1 двухатомного газа, совершающего цикл арно, равен 153 л. ќпределить наибольший объем V3, если объем V2 в конце изотермического расширени€ и объем V4 в конце изотермического сжати€ равны соответственно 600 и 189 л.
6.25. »деальный двухатомный газ, содержащий количество вещества n=1 моль и наход€щийс€ под давлением p1=0,1 ћѕа при температуре T1=300 K, нагревают при посто€нном объеме до давлени€ p2 = 0,2 ћѕа. ѕосле этого газ изотермически расширилс€ до начального давлени€ и затем изобарно был сжат до начального объема V1. ѕостроить график цикла. ќпределить температуру T газа дл€ характерных точек цикла и его термический ѕƒ.
6.26. »деальный многоатомный газ совершает цикл, состо€щий из двух изохор и двух изобар, причем наибольшее давление газа в два раза больше наименьшего, а наибольший объем в четыре раза больше наименьшего. ќпределить термический ѕƒ цикла.






