молекулярной физики и термодинамики
Молекулярная физика – это раздел физики, в котором изучают структуру, свойства и агрегатное состояние веществ, исходя из молекулярно-кинетических представлений об их природе. Согласно этим представлениям все вещества состоят из атомов, молекул или ионов, которые находятся в непрерывном хаотическом тепловом движении.
В молекулярной физике используют два различных, но дополняющих друг друга метода: статистический и термодинамический. Первый лежит в основе молекулярно-кинетической теории газов и основан на использовании теории вероятностей и представления изучаемого объекта в виде ²идеального газа². Все процессы, происходящие в макроскопической системе, и ее свойства объясняются как совокупный эффект от взаимодействия большого числа микрочастиц (атомов или молекул). Поэтому молекулярно-кинетическую теорию называют еще и статистической физикой.
Термодинамический метод, в отличие от статистического, не рассматривает внутреннее строение изучаемых объектов и не изучает характер движения отдельных микрочастиц. он основан на анализе условий и закономерностей превращения различных видов энергии исследуемой системы при ее переходе из одного состояния в другое.
Прежде чем перейти к рассмотрению основ молекулярной физики необходимо дать несколько определений.
Термодинамическая система – это мысленно выделенная совокупность макроскопических тел, которые взаимодействуют и обмениваются энергией как между собой так и с внешней средой.
Состояние системы задается термодинамическими параметрами (параметрами состояния)–совокупностью физических величин, которые характеризуют свойства системы: удельный объем (v), давление (p), температура (Т).
Удельный объемv - это объем единицы массы, когда тело однородно, то есть его плотность r = const:
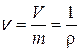 .
.
Поскольку при постоянной массе удельный объем пропорционален общему объему, то макроскопические свойства однородного тела можно характеризовать объемом тела.
Давлением называется физическая величина
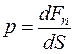 ,
,
где dFn – это модуль нормальной силы, действующий на малый участок поверхности тела.
Температура – это физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы. под равновесным состоянием понимают такое состояние термодинамической системы, при котором термодинамические параметры не меняются во времени.
В соответствии с решением XI Генеральной конференции по мерам и весам с 1960 г. можно применять только две температурные шкалы – термодинамическую и Международную практическую, градуированные соответственно в кельвинах (К ) и в градусах Цельсия (°С). В международной практической шкале в качестве реперных точек принята температура замерзания и кипения воды при давлении 1,013×105 Па. Термодинамическая температурная шкала определяется по одной реперной точке – это тройная точка воды – температура, при которой лед, вода и насыщенный пар при давлении 609 Па находятся в термодинамическом равновесии. Температура замерзания воды равна 273,15К. Термодинамическая температура Т и температура по Международной практической шкале t связаны соотношением:
Т = 273,15 + t.
Температура Т = 0 называется нулем Кельвина. Нормальными условиями (н.у.) принято считать температуру Т 0 = 273,15 К и давление р 0= 1,013×105 Па.
Параметры состояния системы могут изменяться. Любое изменение в системе, связанное с изменением хотя бы одного из ее термодинамических параметров, называют термодинамическим процессом.
В молекулярной физике массы атомов и молекул принято характеризовать не их абсолютными значениями, например в кг, а относительными безразмерными величинами - атомной (Аr) и молекулярной (Мr) массами. В качестве атомной единицы массы (а.е.м., mу) принимается 1/12 массы изотопа углерода 12С (mу = 1,66×10-27 кг). Относительная молекулярная масса Мг = m 0 / mу, где m 0- абсолютное значение массы молекулы.
В молекулярной физике также используется понятие количества вещества, которое выражается в молях. Моль равен такому количеству вещества, которое содержит столько же структурных элементов (атомов, молекул), сколько атомов содержится в 0,012 кг изотопа углерода 12С.Следовательно,1мольлюбого вещества содержит одинаковое число структурных элементов, которое называется постоянная Авогадро: 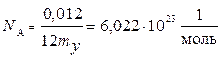 .
.
Например, N = 1025молекул водорода и N = 1025молекул кислорода являются одинаковыми количествами вещества, хотя они имеют разные массы: 3,34×10-2 кг и 0,531 кг соответственно.
В молекулярной физике используют также понятие молярная масса m, которая определяется как масса 1 моля вещества, то естьm = NА × m 0.






