ѕусть имеетс€ кубический сосуд с ребром длиной  и одна частица массой
и одна частица массой  в нЄм.
в нЄм.
ќбозначим скорость движени€  , тогда перед столкновением со стенкой сосуда импульс частицы равен
, тогда перед столкновением со стенкой сосуда импульс частицы равен  , а после Ч
, а после Ч  , поэтому стенке передаетс€ импульс
, поэтому стенке передаетс€ импульс  . ¬рем€, через которое частица сталкиваетс€ с одной и той же стенкой, равно
. ¬рем€, через которое частица сталкиваетс€ с одной и той же стенкой, равно  .
.
ќтсюда следует:

“ак как давление  , следовательно сила
, следовательно сила 
ѕодставив, получим: 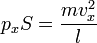
ѕреобразовав: 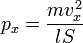
“ак как рассматриваетс€ кубический сосуд, то 
ќтсюда:
 .
.
—оответственно,  и
и  .
.
“аким образом, дл€ большого числа частиц верно следующее:  , аналогично дл€ осей y и z.
, аналогично дл€ осей y и z.
ѕоскольку  , то
, то  . Ёто следует из того, что все направлени€ движени€ молекул в хаотичной среде равноверо€тны.
. Ёто следует из того, что все направлени€ движени€ молекул в хаотичной среде равноверо€тны.
ќтсюда 
или  .
.
ѕусть  Ч среднее значение кинетической энергии всех молекул, тогда:
Ч среднее значение кинетической энергии всех молекул, тогда:
 , откуда
, откуда  .
.
ƒл€ одного мол€ выражение примет вид 
¬опрос 29:
“ермодинамическую температуру, как У физическую величину, характеризующую состо€ние термодинамического равновеси€ макроскопической системы Уќбщим в этих трех определени€х €вл€етс€ то, что термодинамическа€ температура определ€етс€ дл€ равновесной макроскопической системы, и что температура характеризует кинетическую энергию частиц этой системы.
ѕересчЄт температуры между основными шкалами из ÷ельси€
‘аренгейт (∞F) [∞F] = [∞C] × 9⁄5 + 32 [∞C] = ([∞F] − 32) × 5⁄9
ельвин (K) [K] = [∞C] + 273.15 [∞C] = [K] − 273.15
јбсолютный ноль температуры определен экспериментально и равен Ч273,15 ∞—. ќтсюда следует: температура плавлени€ льда по абсолютной шкале температур равна 273,15 . —оответственно температура кипени€ воды равна 373,15 .
‘изический смысл температуры
ќпыт: давление газа зависит от температуры -  и
и  .
.
»з основного уравнени€ ћ “ идеального газа:  . —ледовательно
. —ледовательно  .
.
≈сли мы установим, как мен€етс€ это выражение при переходе от одного состо€ни€ теплового равновеси€ к другому, то можно будет ввести пон€тие температуры и изучить ее свойства.
‘изическа€ величина, одинакова€ у любых тел при тепловом равновесии.
ќпыт показывает, что дл€ любых веществ 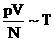 .
.
«амен€€ знак пропорциональности на знак равенства, получим:  ,
,
где k Ц коэффициент пропорциональности, называемый посто€нна€ Ѕольцмана, а “ Ц абсолютна€ термодинамическа€ температура.

јбсолютна€ температура.
 - абсолютна€ температура неотрицательна!
- абсолютна€ температура неотрицательна!
“.к. объем газа равен нулю быть не может, то температура равна нулю, если давление равно нулю, а значит, равна нулю скорость поступательного теплового движени€ (сохран€ютс€ т.н. нулевые колебани€).


≈диница температуры Ц ельвин ( ). ельвин равен 1/273,16 части термодинамической температуры трой≠ной точки воды. Ўкала строитс€ так, что  .
.
≈Ћ№¬»Ќ
1

¬опрос 30:
¬нутренн€€ энерги€
¬ну́тренн€€ эне́рги€ тела (обозначаетс€ как E или U) Ч это сумма энергий молекул€рных взаимодействий и тепловых движений молекулы. ¬нутренн€€ энерги€ €вл€етс€ однозначной функцией состо€ни€ системы. Ёто означает, что вс€кий раз, когда система оказываетс€ в данном состо€нии, еЄ внутренн€€ энерги€ принимает присущее этому состо€нию значение, независимо от предыстории системы. —ледовательно, изменение внутренней энергии при переходе из одного состо€ни€ в другое будет всегда равно разности между ее значени€ми в конечном и начальном состо€ни€х, независимо от пути, по которому совершалс€ переход.
|
|
|
¬нутреннюю энергию тела нельз€ измерить напр€мую. ћожно определить только изменение внутренней энергии:

где
І  Ч подведЄнна€ к телу теплота, измеренна€ в джоул€х
Ч подведЄнна€ к телу теплота, измеренна€ в джоул€х
І  [1] Ч работа, совершаема€ телом против внешних сил, измеренна€ в джоул€х
[1] Ч работа, совершаема€ телом против внешних сил, измеренна€ в джоул€х
Ёта формула €вл€етс€ математическим выражением первого начала термодинамики
ƒл€ квазистатических процессов выполн€етс€ следующее соотношение:

где
І 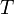 Ч температура, измеренна€ в кельвинах
Ч температура, измеренна€ в кельвинах
І  Ч энтропи€, измеренна€ в джоул€х/кельвин
Ч энтропи€, измеренна€ в джоул€х/кельвин
І  Ч давление, измеренное в паскал€х
Ч давление, измеренное в паскал€х
І  Ч химический потенциал
Ч химический потенциал
І  Ч количество частиц в системе
Ч количество частиц в системе
»деальные газы
—огласно закону ƒжоул€, выведенному эмпирически, внутренн€€ энерги€ идеального газа не зависит от давлени€ или объЄма. »сход€ из этого факта, можно получить выражение дл€ изменени€ внутренней энергии идеального газа. ѕо определению мол€рной теплоЄмкости при посто€нном объЄме,  . “ак как внутренн€€ энерги€ идеального газа €вл€етс€ функцией только от температуры, то
. “ак как внутренн€€ энерги€ идеального газа €вл€етс€ функцией только от температуры, то
 .
.
Ёта же формула верна и дл€ вычислени€ изменени€ внутренней энергии любого тела, но только в процессах при посто€нном объЄме (изохорных процессах); в общем случае  €вл€етс€ функцией и температуры, и объЄма.
€вл€етс€ функцией и температуры, и объЄма.
≈сли пренебречь изменением мол€рной теплоЄмкости при изменении температуры, получим:
 ,
,
где 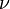 Ч количество вещества,
Ч количество вещества, 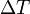 Ч изменение температуры.
Ч изменение температуры.
¬опрос 31:






