(учебно-методическое пособие)
—аратов 2002
ќбща€ теори€ поглощени€ света молекулами.
—ветова€ волна состоит из взаимно перпендикул€рных электрического и магнитного полей, амплитуды которых по мере распространени€ в пространстве измен€ютс€ по синусоиде. Ёнерги€ волны ≈ равна
 |
где h- посто€нна€ ѕланка, с- скорость света, l- длина волны, n- частота. огда волна сталкиваетс€ с молекулой, она может либо рассеиватьс€ (т.е. измен€ть направление еЄ распространени€), либо поглощатьс€ (т.е. еЄ энерги€ передаЄтс€ молекуле). ќтносительна€ веро€тность протекани€ того или иного процесса €вл€етс€ свойством той молекулы, с которой произошло столкновение. ≈сли произошло поглощение электромагнитной энергии света, о молекуле говор€т, что она возбуждена или перешла в возбужденное состо€ние.
ћолекула или часть молекулы, котора€ может быть возбуждена посредством поглощени€ света в видимой и ближней ”‘-области, называетс€ хромофором.
”льтрафиолетова€ область €вл€етс€ коротковолновой областью спектра, с одной стороны примыкающей к видимой еЄ части, а с другой переход€щей на рентгеновский спектр. ¬есь ”‘-спектр дел€т на ближний с длиной волны 400-300 нм, примыкающий к видимой области (400-800 нм), дальний ”‘ (300-200 нм) и вакуумный (200-50 нм). 1 нанометр=10-9м = 10Å).
јбсорбционна€ ”‘-спектроскопи€ изучает спектры поглощени€.
ѕоглощение энергии происходит с наибольшей веро€тностью только в том случае, если количество поглощенной энергии соответствует разности энергий квантованных состо€ний. “аким образом, свет с длиной волны l поглощаетс€ только тогда, когда
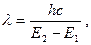 |
где ≈1- энергетический уровень молекулы до поглощени€, а ≈2- энергетический уровень, достигаемый в результате поглощени€.
»зменение энергетического состо€ни€ при испускании или поглощении кванта называетс€ переходом. ”прощенно переход между электронными энергетическими уровн€ми соответствует энергии, необходимой дл€ перемещени€ электрона с одной орбитали на другую. «ависимость веро€тности поглощени€ от длины волны называетс€ спектром поглощени€. «адача абсорбционной спектроскопии состоит в накоплении и анализе данных по поглощению.
»так, поглощение световой энергии в видимой и ”‘-области св€зано с различным типом электронных переходов. ќптические спектры атомов св€заны с квантовыми переходами электронов внешней электронной оболочки. ѕри объединении атомов в молекулу обобществленные (валентные) электроны образуют внешнюю оболочку и остаютс€ ответственными за оптические спектры.






